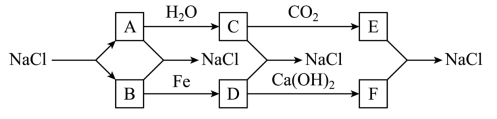
现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出)
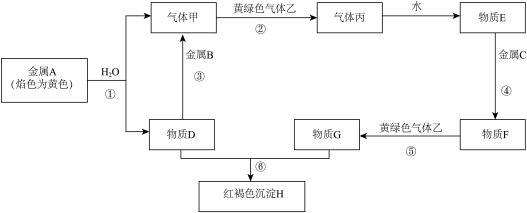
请回答下列问题:
(1)写出下列物质的化学式:B_______ 、丙_______ 、乙_______ 。
(2)写出下列反应的化学方程式:
反应①_______ ;反应⑤_______ ;反应⑥_______ 。

请回答下列问题:
(1)写出下列物质的化学式:B
(2)写出下列反应的化学方程式:
反应①
14-15高一上·江西鹰潭·期末 查看更多[3]
更新时间:2019/01/30 18:14:09
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
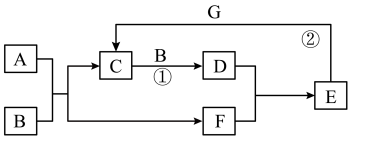
【推荐1】I.在如图所示的物质转化关系中,A是常见的气态氢化物,也是一种重要的化工产品、化工原料,B是能使带火星的木条复燃的无色、无味气体,E的相对分子质量比D的大17,合成A以及制取E的流程示意图如图所示,G是一种紫红色金属单质(反应条件和部分生成物未列出)。______ ,F的电子式为______ 。
(2)请写出在吸收塔中发生反应①的化学反应方程式_____ ,反应②的离子方程式_____ 。
Ⅱ.氨既是一种重要的化工产品,又是一种重要的化工原料。如图为合成氨以及氨氧化制硝酸的流程示意图。_____ ,其中还原剂与氧化剂的物质的量之比为_____ 。
(4)M是_____ (填写名称),向吸收塔中通入M的作用_____ 。
(5)E的浓溶液见光易分解,实验室保存时用棕色试剂瓶避光保存,请用化学方程式解释原因_____ 。
(2)请写出在吸收塔中发生反应①的化学反应方程式
Ⅱ.氨既是一种重要的化工产品,又是一种重要的化工原料。如图为合成氨以及氨氧化制硝酸的流程示意图。

(4)M是
(5)E的浓溶液见光易分解,实验室保存时用棕色试剂瓶避光保存,请用化学方程式解释原因
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】如图,A、B、C、D、E各代表水、铁、二氧化碳、硫酸铜溶液、氢氧化钡溶液中的一种物质,常温下,相连环物质间能发生反应,不相连环物质间不能发生反应,且B的摩尔质量大于D。请填空:
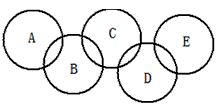
(1)写出下列物质的化学式:A_____________ ,B_____________ ,D______________ 。
(2)写出下列反应的化学方程式:
B+C:______________________________________ 。

(1)写出下列物质的化学式:A
(2)写出下列反应的化学方程式:
B+C:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】由两种元素组成的化合物A,按如下流程进行实验。气体B能使湿润的红色石蕊试纸变蓝;固体E可做光导纤维材料。
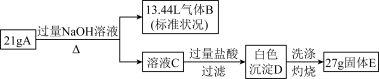
请回答:
(1)组成A的两种元素是___________ (用元素符号表示);
(2)写出A与 溶液反应的化学方程式
溶液反应的化学方程式___________ ;
(3)溶液C与过量盐酸反应的两个离子方程式是___________ 、___________ ;
(4)气体B与氧化铁在高温下反应,生成黑色粉末(纯净物),取适量黑色粉末加盐酸溶解,无气泡产生,再往溶液中滴加几滴 溶液,溶液变血红色,黑色粉末成分可能是
溶液,溶液变血红色,黑色粉末成分可能是___________ 。

请回答:
(1)组成A的两种元素是
(2)写出A与
 溶液反应的化学方程式
溶液反应的化学方程式(3)溶液C与过量盐酸反应的两个离子方程式是
(4)气体B与氧化铁在高温下反应,生成黑色粉末(纯净物),取适量黑色粉末加盐酸溶解,无气泡产生,再往溶液中滴加几滴
 溶液,溶液变血红色,黑色粉末成分可能是
溶液,溶液变血红色,黑色粉末成分可能是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】如图所示:
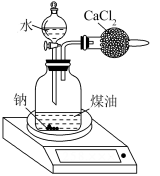
为了测定钠的相对原子质量,将装置放在电子天平上,读出的数据为254.843g。加入一小块钠后读数为258.293g,加入水后每隔相同时间读得电子天平的数据(装置+水+煤油+试样的质量)如表:(不考虑煤油的挥发)
回答以下问题:
(1)写出钠与水反应的化学方程式:____ 。
(2)计算钠的相对原子质量必须用到的数据是____ 。不必进行第6次读数的原因是____ 。
(3)去掉干燥管后所测得的钠的相对原子质量可能____ (填“偏大”“偏小”或“无影响”)。
(4)该实验与测定生成H2的体积来确定钠的相对原子质量的实验相比,其优点是____ 。

为了测定钠的相对原子质量,将装置放在电子天平上,读出的数据为254.843g。加入一小块钠后读数为258.293g,加入水后每隔相同时间读得电子天平的数据(装置+水+煤油+试样的质量)如表:(不考虑煤油的挥发)
| 读数次数 | 1 | 2 | 3 | 4 | 5 |
| 质量/g | 258.191 | 258.183 | 258.150 | 258.143 | 258.143 |
(1)写出钠与水反应的化学方程式:
(2)计算钠的相对原子质量必须用到的数据是
(3)去掉干燥管后所测得的钠的相对原子质量可能
(4)该实验与测定生成H2的体积来确定钠的相对原子质量的实验相比,其优点是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】元素周期表的一部分如图,其中字母代表对应的元素,请回答下列问题:
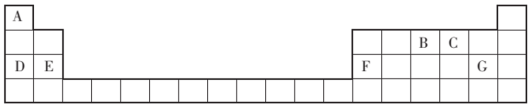
(1)图中出现的元素,金属性最强的是_______ (填元素符号),该元素的单质与水反应的离子方程式为_______ ,此反应产物中含有三种元素的化合物的电子式为_______ ,该化合物中含有的化学键类型为_______ 。
(2)A分别与B、C、G形成的最简单化合物中,最稳定的是_______ (填化学式,下同),水溶液显碱性的是_______ ,水溶液显酸性的是_______ 。
(3)F和G形成的化合物是_______ (填“离子”或“共价”)化合物,向其水溶液中逐滴滴入D的最高价氧化物对应水化物的溶液至过量,出现的现象是_______ 。写出该过程的化学方程式:_______ 。

(1)图中出现的元素,金属性最强的是
(2)A分别与B、C、G形成的最简单化合物中,最稳定的是
(3)F和G形成的化合物是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】如图所示为 (初中常见的物质)的转化关系.其中A是天然气的主要成分,D为碳不完全燃烧的产物,I、J、K为含同一金属元素的三种盐.
(初中常见的物质)的转化关系.其中A是天然气的主要成分,D为碳不完全燃烧的产物,I、J、K为含同一金属元素的三种盐.
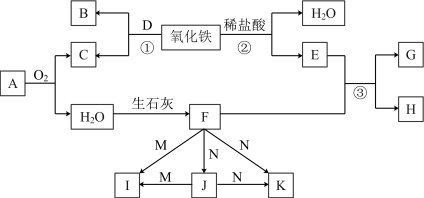
(1)M的化学式为____________ ,E的化学式为____________ ,生石灰的常见用途是_________________________ .
(2)写出反应①的化学方程式:_____________________________________________ .
(3)写出 反应的化学方式:
反应的化学方式:____________________________________________ .
(4)E与F的澄清溶液反应的离子方程式为________________________________ ,该反应属于____________ 反应(填基本反应类型).
 (初中常见的物质)的转化关系.其中A是天然气的主要成分,D为碳不完全燃烧的产物,I、J、K为含同一金属元素的三种盐.
(初中常见的物质)的转化关系.其中A是天然气的主要成分,D为碳不完全燃烧的产物,I、J、K为含同一金属元素的三种盐.
(1)M的化学式为
(2)写出反应①的化学方程式:
(3)写出
 反应的化学方式:
反应的化学方式:(4)E与F的澄清溶液反应的离子方程式为
您最近一年使用:0次
【推荐2】已知在下图转化关系(某些转化关系中的产物已略去)中都是中学化学常见的物质,物质A、D、G是单质,磁性黑色物质C是某金属矿物的主要成分,E是一种非氧化性酸,F是混合物,H是极易溶于水的碱性气体。
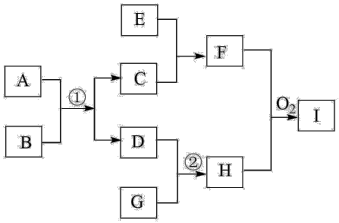
请回答下列问题:
(1)写出下列物质的化学式:A________ 、C__________ 、I__________
(2)写出反应①的化学方程式:________________________________ ;写出生成混合物F的离子方程式:__________________________
(3)在一定温度、压强和有催化剂存在的条件下将l mol G和2,5 mol D放入500mL密闭容器中。经过20min达到平衡,平衡后H的浓度为2mol/L,
①则用G表示20min内的平均反应速率为:____ 该温度下此反应的平衡常数K=______ ,D的转化率为__________
②如果保持温度不变,再向容器中同时充入1.5 mol G和1 mol H,D的转化率将______ (填“升高”、“不变”或“降低”),再次平衡后H的体积分数为___________ 。

请回答下列问题:
(1)写出下列物质的化学式:A
(2)写出反应①的化学方程式:
(3)在一定温度、压强和有催化剂存在的条件下将l mol G和2,5 mol D放入500mL密闭容器中。经过20min达到平衡,平衡后H的浓度为2mol/L,
①则用G表示20min内的平均反应速率为:
②如果保持温度不变,再向容器中同时充入1.5 mol G和1 mol H,D的转化率将
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】高铁酸盐在污水处理,水体消杀等方面用途广泛。高铁酸钾( )是一种重要的高铁酸盐。某学校化学学习小组通过下列装置制备
)是一种重要的高铁酸盐。某学校化学学习小组通过下列装置制备 。回答下列问题:
。回答下列问题:
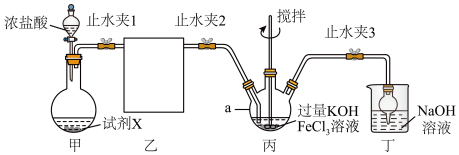
已知 的部分性质如下:
的部分性质如下:
(1)仪器a的名称是_____________ 。
(2)装置乙可选用下列_______ (填标号)。
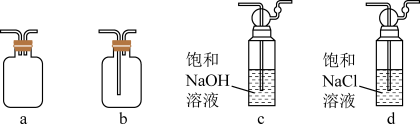
(3)写出装置丙中发生反应的化学方程式_____________ 。
(4)制备过程中,装置丙需采用冰水浴,目的是____________ 。
(5)该装置中以1.5molFeCl3为原料,完全转化为K2FeO4需要消耗KOH________ g。
(6)装置丁中反应的离子方程式:_____________ 。
 )是一种重要的高铁酸盐。某学校化学学习小组通过下列装置制备
)是一种重要的高铁酸盐。某学校化学学习小组通过下列装置制备 。回答下列问题:
。回答下列问题:
已知
 的部分性质如下:
的部分性质如下:| 溶解性 | 溶于水,微溶于浓KOH溶液,难溶于有机物 |
| 稳定性 | 温度为0~5℃或强碱性溶液中能稳定存在;酸性或中性溶液中放出O2 |
(2)装置乙可选用下列

(3)写出装置丙中发生反应的化学方程式
(4)制备过程中,装置丙需采用冰水浴,目的是
(5)该装置中以1.5molFeCl3为原料,完全转化为K2FeO4需要消耗KOH
(6)装置丁中反应的离子方程式:
您最近一年使用:0次

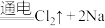 。现有如下转化关系:
。现有如下转化关系: