已知铷是37号元素。根据相关知识回答下列问题:
(1)请推测铷(Rb)在元素周期表的第___________ 周期第___________ 族。
(2)关于铷的结构和性质判断正确的是___________(填字母,下同)。
①与水反应比钠剧烈 ②它的原子半径比钠小
③它的氧化物暴露在空气中易吸收CO2 ④它的阳离子最外层电子数和镁相同
⑤它是还原剂
(3)氢化铷与水反应可放出氢气,则下列叙述正确的是___________。
(4)现有铷和另一种碱金属形成的合金50 g,当它与足量水反应时,放出标准状况下的氢气22.4 L,这种碱金属可能是________。
(1)请推测铷(Rb)在元素周期表的第
(2)关于铷的结构和性质判断正确的是___________(填字母,下同)。
①与水反应比钠剧烈 ②它的原子半径比钠小
③它的氧化物暴露在空气中易吸收CO2 ④它的阳离子最外层电子数和镁相同
⑤它是还原剂
| A.①③④ | B.①③⑤ | C.②③⑤ | D.②④ |
| A.氢化铷溶于水显酸性 |
| B.氢化铷与水反应时被还原为氢气 |
| C.氢化铷是离子化合物,其中氢离子最外层有2个电子 |
| D.氢化铷与水反应时,生成1mol H2将转移2mol e- |
| A.Li | B.Na | C.K | D.Cs |
23-24高一上·全国·课时练习 查看更多[1]
更新时间:2023-08-16 20:59:08
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】下表列出了①~⑩10种元素在周期表中的位置。
(1)上述元素中,金属性最强的是(填元素符号,下同)________ ,③④⑤三种元素的原子半径由大到小的顺序是____________ 。
(2)上述元素的最高价氧化物对应的水化物中酸性最强的是________ (填化学式)
(3)元素⑥的氢化物的电子式为____________ ,该氢化物与元素⑥的最高价氧化物对应的水化物反应的化学方程式为____________ 。
(4)比较⑥和⑦氢化物的稳定性由强到弱的顺序是____________ (填化学式)。
| 族 周期 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑤ | ⑥ | ⑩ | |||||
| 3 | ① | ③ | ④ | ⑦ | ⑧ | |||
| 4 | ② | ⑨ |
(1)上述元素中,金属性最强的是(填元素符号,下同)
(2)上述元素的最高价氧化物对应的水化物中酸性最强的是
(3)元素⑥的氢化物的电子式为
(4)比较⑥和⑦氢化物的稳定性由强到弱的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表为元素周期表的一部分,请参照元素①﹣⑩在表中的位置,回答下列问题:
(1)自然界物质种类最多的元素在周期表中的位置是______
(2)⑧⑨⑩的离子半径由大到小的顺序为______ (填化学用语).
(3)写出由⑥、⑧、⑩元素形成的一种离子化合物的电子式______
(4)根据斜线性质相似规则,②的最高价氧化物对应的水化物与盐酸反应的离子方程式____________
(5)③的氧化物,氢氧化物有两性,写出③的单质与⑧的最高价氧化物的水化物反应的化学方程式______
(6)已知W+X=Y+Z,W、X、Y、Z分别是由①⑤⑥三种元素形成的四种十电子粒子,写出该反应的离子方程式______ .
| IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ||
| 3 | ⑧ | ⑨ | ⑩ |
(1)自然界物质种类最多的元素在周期表中的位置是
(2)⑧⑨⑩的离子半径由大到小的顺序为
(3)写出由⑥、⑧、⑩元素形成的一种离子化合物的电子式
(4)根据斜线性质相似规则,②的最高价氧化物对应的水化物与盐酸反应的离子方程式
(5)③的氧化物,氢氧化物有两性,写出③的单质与⑧的最高价氧化物的水化物反应的化学方程式
(6)已知W+X=Y+Z,W、X、Y、Z分别是由①⑤⑥三种元素形成的四种十电子粒子,写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表是元素周期表的一部分, 回答下列问题:
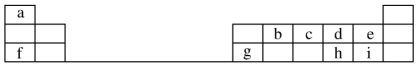
(1)元素e的负一价离子的结构示意图为____________ , e、f、g、h、i对应简单离子的半径由大到小的顺序为______________ (用具体微粒符号表示)。
(2)元素i的单质溶于水,生成一种具有漂白作用的化合物,该化合物的电子式为_____ 。
(3)以元素b的最简气态氢化物为燃料,以f的最高价氧化物对应的水化物为电解质溶液,请写出该燃料电池的负极反应方程式________________________________ 。

(1)元素e的负一价离子的结构示意图为
(2)元素i的单质溶于水,生成一种具有漂白作用的化合物,该化合物的电子式为
(3)以元素b的最简气态氢化物为燃料,以f的最高价氧化物对应的水化物为电解质溶液,请写出该燃料电池的负极反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】如下表所示为元素周期表的一部分,参照元素①~⑦在表中的位置,请回答下列问题:
(1)③、④、⑦的原子半径由大到小的顺序为______ (用元素符号表示)。
(2)⑥和⑦的最高价含氧酸的酸性强弱为_____________ (用酸的化学式表示)。
(3)①、②两种元素按原子个数之比为1:1组成的常见液态化合物,在酸性溶液中能将Fe2+氧化,写出该反应的离子方程式_________________________ ;
(4)由表中元素形成的物质可发生如图中的反应,其中B、C、G是单质,B为黄绿色气体,D溶液显碱性。
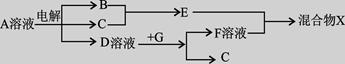
①写出D溶液与G反应的化学方程式_____________________________________ 。
②写出检验A溶液中溶质的阴离子的方法__________________________________ 。
③常温下,若电解1L0.1 mol·L-1的A溶液,一段时间后测得溶液pH为12(忽略溶液体积变化),则该电解过程中转移电子的物质的量为_________________ 。
④写出过量的E与F溶液中溶质反应的离子方程式_______________________ 。
(5)由②、④、⑥元素组成的化合物W(在酸性溶液中发黄,W还原性较强),在溶液中易被⑦的单质氧化,该反应的离子方程式为____________________________ 。
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ||||
(2)⑥和⑦的最高价含氧酸的酸性强弱为
(3)①、②两种元素按原子个数之比为1:1组成的常见液态化合物,在酸性溶液中能将Fe2+氧化,写出该反应的离子方程式
(4)由表中元素形成的物质可发生如图中的反应,其中B、C、G是单质,B为黄绿色气体,D溶液显碱性。

①写出D溶液与G反应的化学方程式
②写出检验A溶液中溶质的阴离子的方法
③常温下,若电解1L0.1 mol·L-1的A溶液,一段时间后测得溶液pH为12(忽略溶液体积变化),则该电解过程中转移电子的物质的量为
④写出过量的E与F溶液中溶质反应的离子方程式
(5)由②、④、⑥元素组成的化合物W(在酸性溶液中发黄,W还原性较强),在溶液中易被⑦的单质氧化,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知A、B、C、D、E、F、G都是元素周期表中短周期主族元素,它们的原子序数依次增大。A是元素周期表中原子半径最小的元素,D3B中阴、阳离子具有相同的电子层结构,B、C均可分别与A形成10电子分子,B、C属同一周期,两者可以形成许多种共价化合物,C、F属同一主族,B原子最外电子层的p能级上的电子处于半满状态,C的最外层电子数是内层电子数的3倍,E最外层电子数比最内层多1。请用具体的元素回答下列问题:
(1)E元素基态原子电子排布式为______________ 。
(2)F、G元素对应的最高价含氧酸中酸性较强的化学式为__________ 。
(3)A、C形成的一种绿色氧化剂X有广泛应用,X分子中A、C原子个数比为1∶1,X的电子式为____________ ,试写出Cu、稀硫酸与X反应制备硫酸铜的离子方程式___________________________________________ 。
(4)写出E与D的最高价氧化物对应的水化物反应的化学方程式____________ 。
(5)离子半径:D+______ B3-,电负性:C_______ F。(填“<”、“>”或“=”)
(1)E元素基态原子电子排布式为
(2)F、G元素对应的最高价含氧酸中酸性较强的化学式为
(3)A、C形成的一种绿色氧化剂X有广泛应用,X分子中A、C原子个数比为1∶1,X的电子式为
(4)写出E与D的最高价氧化物对应的水化物反应的化学方程式
(5)离子半径:D+
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】卤素都是典型的非金属元素,其单质(X2)都具有氧化性。
(1)卤素易形成X-的原因是___________ 。
(2)X2与H2化合的化学方程式是___________ ,其反应条件难易规律是___________ 。
(3)将氯气通入碘化钾溶液中反应的离子方程式是___________ 。
(4)举例说明氯气的氧化性比单质溴的氧化性强:___________ 。
(5)砹(At)属于卤族元素,下列关于砹(At)及其化合物具有的性质推测不正确的是___________(填字母)。
(1)卤素易形成X-的原因是
(2)X2与H2化合的化学方程式是
(3)将氯气通入碘化钾溶液中反应的离子方程式是
(4)举例说明氯气的氧化性比单质溴的氧化性强:
(5)砹(At)属于卤族元素,下列关于砹(At)及其化合物具有的性质推测不正确的是___________(填字母)。
| A.单质砹易溶于某些有机溶剂 |
| B.AgAt是难溶于水的有色固体 |
| C.HAtO4的酸性比HClO4的弱 |
| D.HAt难溶于水,且受热很难分解 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】卤族元素的单质能与H2反应
(1)卤族元素位于周期表中的______________ 族。
(2)用电子式表示HCl的形成过程______________ 。
(3)依据上表,可以推测出:随着原子序数的递增,___________ (填字母)。
a. 单质的熔沸点逐渐升高 b. 元素的非金属性逐渐减弱
c. 卤化氢的还原性依次减弱 d. 卤化氢的稳定性依次减弱
(4)不同卤素原子之间可形成卤素互化物,其性质与卤素单质相近。写出BrCl和SO2在水溶液中发生反应的化学方程式___________ 。
| H2+F2=2HF | 在暗处能剧烈化合并发生爆炸 |
| H2+Cl2=2HCl | 光照或点燃发生反应 |
| H2+Br2=2HBr | 加热至一定温度才能反应 |
| H2+I2=2HI | 不断加热才能缓慢反应,生成的HI会分解 |
(1)卤族元素位于周期表中的
(2)用电子式表示HCl的形成过程
(3)依据上表,可以推测出:随着原子序数的递增,
a. 单质的熔沸点逐渐升高 b. 元素的非金属性逐渐减弱
c. 卤化氢的还原性依次减弱 d. 卤化氢的稳定性依次减弱
(4)不同卤素原子之间可形成卤素互化物,其性质与卤素单质相近。写出BrCl和SO2在水溶液中发生反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】与硫同族的元素Te,最高价氧化物的水化物碲酸(H6TeO6)的酸性比H2SO4____ (选填“强”或“弱”),其氧化性比硫酸强。向碲酸中通入SO2气体,若反应中生成的TeO2与Te的物质的量之比为2:1,写出该反应的化学方程式______________ 。当6mol碲酸与一定量SO2恰好完全反应,所得溶液体积为20L,则所得溶液的pH为____________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在生产生活中,卤族元素(F、Cl、Br、I)的单质及化合物用途广泛。
(1)氯元素在周期表中的位置为_______ 。
(2)下列说法中正确的是_______
(3)已知:ICl(氯化碘)是红棕色液体,易水解。ICl 的水解反应方程式是_______ 。
(4)工业氢溴酸常带有淡淡的黄色,可能的原因是:①含 Fe3+,②含 Br2,③含 Fe3+和 Br2,只用下列一种试剂就能分析产生淡黄色的原因,该试剂是 _______(填写字母)。
(1)氯元素在周期表中的位置为
(2)下列说法中正确的是_______
| A.XeF2 分子中各原子最外层均满足 8e-结构 |
| B.食用碘盐中添加了 KIO3 |
| C.氟元素的非金属性强于氯元素,故氢氟酸的酸性强于盐酸 |
| D.还原性:Br->I- |
(4)工业氢溴酸常带有淡淡的黄色,可能的原因是:①含 Fe3+,②含 Br2,③含 Fe3+和 Br2,只用下列一种试剂就能分析产生淡黄色的原因,该试剂是 _______(填写字母)。
| A.KMnO4 溶液 | B.KSCN 溶液 | C.淀粉 KI 溶液 | D.CCl4 |
您最近一年使用:0次



