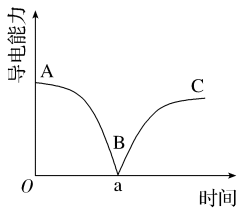
科学研究中观察到的宏观现象能反映微观本质。例如,我们可以通过测定溶液导电能力来探查溶液中自由移动的离子浓度。某小组向0.1 mol/L Ba(OH)2溶液中匀速滴加0.1 mol/L稀硫酸,测得溶液导电能力的变化如图所示,回答下列问题:
资料1:20 ℃时BaSO4溶解度为2.38×10-4 g。
资料2:下表为20 ℃蒸馏水和饱和BaSO4溶液的电导率。
注:电导率越大,溶液导电能力越强。
(1)Ba(OH)2的电离方程式是___________ 。
(2)A~B段发生反应的化学方程式是____________________ 。
(3)关于图中的说法正确的是___________(填字母)。
(4)BaSO4在水中的存在形式,同学们提出了不同的观点:
A.只以BaSO4固体形式存在
B.只以自由移动的SO 和Ba2+形式存在
和Ba2+形式存在
C.主要以BaSO4固体形式存在,同时存在极少量自由移动的SO 和Ba2+
和Ba2+
你支持观点___________ (填字母)证据是____________________ (用文字和数据说明);由此可知,物质在水中的存在形式决定了其在离子方程式中能否写为离子形式。
(5)次磷酸与醋酸相似,是一种易溶于水的一元酸,其分子式为H3PO2,与NaOH溶液反应的离子方程式为:H3PO2+OH-=H2PO +H2O,次磷酸在水中的存在形式是
+H2O,次磷酸在水中的存在形式是___________________ ,次磷酸的电离方程式是___________ 。

资料1:20 ℃时BaSO4溶解度为2.38×10-4 g。
资料2:下表为20 ℃蒸馏水和饱和BaSO4溶液的电导率。
| 蒸馏水 | 饱和BaSO4溶液 | |
| 电导率(S/m) | 1.52×10-3 | 4.58×10-4 |
(1)Ba(OH)2的电离方程式是
(2)A~B段发生反应的化学方程式是
(3)关于图中的说法正确的是___________(填字母)。
| A.AB段溶液的导电能力不断减弱,说明生成的BaSO4不是电解质 |
| B.B处溶液的导电能力约为0,说明溶液中几乎没有自由移动的离子 |
| C.BC段溶液的导电能力不断增大,主要是由于过量的Ba(OH)2电离出的离子导电 |
| D.a时刻Ba(OH)2溶液与稀硫酸恰好完全中和 |
A.只以BaSO4固体形式存在
B.只以自由移动的SO
 和Ba2+形式存在
和Ba2+形式存在C.主要以BaSO4固体形式存在,同时存在极少量自由移动的SO
 和Ba2+
和Ba2+你支持观点
(5)次磷酸与醋酸相似,是一种易溶于水的一元酸,其分子式为H3PO2,与NaOH溶液反应的离子方程式为:H3PO2+OH-=H2PO
 +H2O,次磷酸在水中的存在形式是
+H2O,次磷酸在水中的存在形式是
更新时间:2023-08-17 18:46:11
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】现有以下五种电解质溶液,回答下列问题:
①CH3COOH②NaOH③NH3•H2O④H2SO4⑤CH3COONa
(1)浓度均为0.1mol•L-1的五种溶液中导电能力最强的是______ (填序号)。
(2)pH=10的②③⑤三种溶液中由水电离出的氢离子浓度由大到小的排列顺序为______ (填序号)。
(3)等体积的pH=2的①④两种溶液分别与足量金属锌反应,产生氢气的质量较多的是_____ (填序号)。
(4)溶液①和溶液②混合后溶液呈中性,此时溶液中离子浓度由大到小的排列顺序为_____ 。
(5)室温下,pH=2的H2SO4溶液V1mL和pH=11的氢氧化钠溶液V2mL混合,恰好完全反应,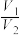 =
=_____ 。
①CH3COOH②NaOH③NH3•H2O④H2SO4⑤CH3COONa
(1)浓度均为0.1mol•L-1的五种溶液中导电能力最强的是
(2)pH=10的②③⑤三种溶液中由水电离出的氢离子浓度由大到小的排列顺序为
(3)等体积的pH=2的①④两种溶液分别与足量金属锌反应,产生氢气的质量较多的是
(4)溶液①和溶液②混合后溶液呈中性,此时溶液中离子浓度由大到小的排列顺序为
(5)室温下,pH=2的H2SO4溶液V1mL和pH=11的氢氧化钠溶液V2mL混合,恰好完全反应,
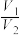 =
=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】完成下列问题
(1)下列物质中 ① ②Fe ③乙醇 ④
②Fe ③乙醇 ④ 胶体 ⑤熔融NaCl ⑥
胶体 ⑤熔融NaCl ⑥ 溶液 ⑦
溶液 ⑦ ⑧固态
⑧固态
A.属于电解质的是_______ 。(只填序号,下同)
B.属于非电解质的是_______ 。
C.所给状态下能导电的是_______ 。
D.既不是电解质,也不是非电解质的纯净物是_______ 。
(2)写出 在水中的电离方程式
在水中的电离方程式_______ 。
(3)请写出实验室中制备 胶体的化学反应方程式
胶体的化学反应方程式_______ 。
(1)下列物质中 ①
 ②Fe ③乙醇 ④
②Fe ③乙醇 ④ 胶体 ⑤熔融NaCl ⑥
胶体 ⑤熔融NaCl ⑥ 溶液 ⑦
溶液 ⑦ ⑧固态
⑧固态
A.属于电解质的是
B.属于非电解质的是
C.所给状态下能导电的是
D.既不是电解质,也不是非电解质的纯净物是
(2)写出
 在水中的电离方程式
在水中的电离方程式(3)请写出实验室中制备
 胶体的化学反应方程式
胶体的化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】现有下列物质:①铜;②冰醋酸(纯醋酸晶体);③熔融的KNO3;④稀盐酸;⑤CO2;⑥KHSO4晶体;⑦蔗糖;⑧Fe(OH)3胶体;⑨液氯;⑩BaSO4固体
(1)属于电解质的是___________ 。属于非电解质的是___________ ,既不是电解质也不是非电解质的是___________ 。
(2)写出⑥在水中的电离方程式___________ ;写出除去Na2CO3固体中的NaHCO3的化学方程式___________ ;在沸水中滴入饱和氯化铁溶液制备⑧的化学方程式是___________ 。
(3)等质量的CO和CO2物质的量之比为___________ ;氧原子个数之比为___________ ;V L Al2(SO4)3溶液中含Al3+ a mol,该Al2(SO4)3溶液的物质的量浓度为___________ mol/L(用含a的式子表示,下同),取出0.5V L再加入水稀释到4V L,则稀释后的溶液中SO 的物质的量浓度为
的物质的量浓度为___________ 。
(1)属于电解质的是
(2)写出⑥在水中的电离方程式
(3)等质量的CO和CO2物质的量之比为
 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】写出下列电离方程式或反应的离子方程式:
(1)硫酸铝电离的电离方程式__________________________________ ;
(2)向澄清石灰水中加硝酸__________________________________ ;
(3)用石灰石与盐酸反应制取二氧化碳__________________________________ ;
(4)锌粉加入硫酸溶液中__________________________________ ;
(5)向Na2CO3溶液中滴加几滴稀盐酸__________________________________ 。
(1)硫酸铝电离的电离方程式
(2)向澄清石灰水中加硝酸
(3)用石灰石与盐酸反应制取二氧化碳
(4)锌粉加入硫酸溶液中
(5)向Na2CO3溶液中滴加几滴稀盐酸
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下列九种物质:① 稀硝酸②CO ③NH3 ·H2O ④ 熔融NaHCO3 ⑤ CaO ⑥Cu⑦ 蔗糖 ⑧ Fe2(SO4)3 ⑨ 酒精
(1)用序号填空:属于电解质的是____________ ;属于碱的是_______________ ;
(2)写出③、⑧ 的电离方程式:③____________________________ ; ⑧ _________________________________________ 。
(3)写出①与④ 反应的离子反应方程式:________________________
(1)用序号填空:属于电解质的是
(2)写出③、⑧ 的电离方程式:③
(3)写出①与④ 反应的离子反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题。
I.已知:
(1)根据上表推测可能发生的反应是___________。
(2)浓度均为0.1mol/L的四种溶液中,pH最大的是___________。
II.将两种浓度均为0.10mol/L溶液等体积混合,忽略混合引起的体积变化,则:
(3)氨水-NH4Cl混合溶液(Kb(NH3.H2O)=1.8×10-5)微粒浓度从大到小排序为___________ 。
(4)H2C2O4-NaHC2O4混合溶液的电荷守恒关系式为___________ 。
(5)NaHCO3-Na2CO3混合溶液的物料守恒关系式为___________ 。
I.已知:
| 25℃ | CH3COOH | HCN | HClO |
| Ka | 1.8×10-5 | 6.2×10-10 | 4.0×10-8 |
| A.HCl+NaCN=NaCl+HCN |
| B.NaClO+HCN=HClO+NaCN |
| C.HClO+CH3COONa=CH3COOH+NaClO |
| D.CH3COOH+NaCN=CH3COONa+HCN |
| A.CH3COONa | B.NaCN | C.NaClO | D.NaCl |
II.将两种浓度均为0.10mol/L溶液等体积混合,忽略混合引起的体积变化,则:
(3)氨水-NH4Cl混合溶液(Kb(NH3.H2O)=1.8×10-5)微粒浓度从大到小排序为
(4)H2C2O4-NaHC2O4混合溶液的电荷守恒关系式为
(5)NaHCO3-Na2CO3混合溶液的物料守恒关系式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】根据水溶液的离子平衡知识,填写下题:
(1)下列物质中,属于强电解质的是________ (均填序号);属于弱电解质的是________ 。
①水②氨水③盐酸④冰醋酸⑤硫酸钡⑥氯化银⑦氯化钠⑧氢气⑨醋酸铵
(2)苏打水溶液显碱性原因(用离子方程式表示)_________________________________ 。
(3)醋酸溶液呈_____ (填“酸性”,“中性”或“碱性”),其电离方程式为:_____ ;
(4)常温下,0.lmol·L-1NaHCO3溶液的pH大于8,则溶液中c(H2CO3)_____ c(CO32-)(填“>”、“=”或“<”)。
(5)在25℃下,将amol·L-1的氨水与0.01mol·L-1的盐酸等体积混合,反应完成后溶液中c(NH4+)=c(Cl-),则溶液显__________ 性(填“酸”“碱”或“中”),a__________ 0.01mol·L-1(填“>”、“=”或“<”)。
(6)若分别将pH=2的盐酸和醋酸稀释100倍,则稀释后溶液的pH:盐酸_____ 醋酸(填“>”、“=”或“<”)。
(7)将100mL0.1mol•L-1的CH3COOH溶液与50mL0.2mol•L-1的NaOH溶液混合,所得溶液呈_____ 性,原因是_____ (用离子方程式表示)。
(1)下列物质中,属于强电解质的是
①水②氨水③盐酸④冰醋酸⑤硫酸钡⑥氯化银⑦氯化钠⑧氢气⑨醋酸铵
(2)苏打水溶液显碱性原因(用离子方程式表示)
(3)醋酸溶液呈
(4)常温下,0.lmol·L-1NaHCO3溶液的pH大于8,则溶液中c(H2CO3)
(5)在25℃下,将amol·L-1的氨水与0.01mol·L-1的盐酸等体积混合,反应完成后溶液中c(NH4+)=c(Cl-),则溶液显
(6)若分别将pH=2的盐酸和醋酸稀释100倍,则稀释后溶液的pH:盐酸
(7)将100mL0.1mol•L-1的CH3COOH溶液与50mL0.2mol•L-1的NaOH溶液混合,所得溶液呈
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】25℃时,有关物质的电离平衡常数如下:
(1)体积为10mLpH=2的醋酸溶液与亚硫酸溶液分别加蒸馏水稀释至1000mL,稀释后溶液的pH,前者________ 后者(填“>”、“<”或“=”);
(2)25℃时,pH之和为14的CH3COOH溶液与NaOH溶液混合,充分反应后溶液显中性,则所耗溶液的体积前者_______ 后者(填“>”、“<”或“=”);
(3)若用NaOH标准溶液滴定未知浓度的醋酸,选择的指示剂应为_______ ;
(4)下列离子CH3COO-、CO32-、HCO3-、HSO3-、SO32-在溶液中结合H+的能力由大到小的顺序为________ 。
| 化学式 | CH3COOH | H2CO3 | H2SO3 |
| 电离平衡常数K | K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.5×10-2 K2=1.02×10-7 |
(2)25℃时,pH之和为14的CH3COOH溶液与NaOH溶液混合,充分反应后溶液显中性,则所耗溶液的体积前者
(3)若用NaOH标准溶液滴定未知浓度的醋酸,选择的指示剂应为
(4)下列离子CH3COO-、CO32-、HCO3-、HSO3-、SO32-在溶液中结合H+的能力由大到小的顺序为
您最近一年使用:0次



