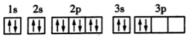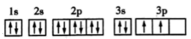阅读教材P17页内容,总结归纳元素的化合价与核外电子排布的关系。
①除Ⅷ族、ⅠB族的某些元素和0族元素外,元素的最高化合价_____ 它所在族的序数。
②一般来说,非金属元素的最高正化合价和它的最低负化合价的绝对值之和等于_____ (F无正价)。
③稀有气体元素的化合价在通常情况下为_____ 。
④过渡元素的价电子较多且所在轨道的能量相差不大,因此过渡元素具有_____ 价态。
①除Ⅷ族、ⅠB族的某些元素和0族元素外,元素的最高化合价
②一般来说,非金属元素的最高正化合价和它的最低负化合价的绝对值之和等于
③稀有气体元素的化合价在通常情况下为
④过渡元素的价电子较多且所在轨道的能量相差不大,因此过渡元素具有
更新时间:2023-08-25 16:15:48
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】《梦溪笔谈》有记:馆阁新书净本有误书处,以雌黄涂之。在中国古代,雌黄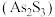 经常用来修改错字。
经常用来修改错字。
(1)S在元素周期表中的位置是第_______ 周期、第ⅥA族。
(2)写出S的最高价氧化物对应的水化物的化学式:_______ 。
(3)S的非金属性强于P的,用原子结构解释原因:S和P在同一周期,原子核外电子层数相同,_______ ,原子半径S小于P,得电子能力S强于P。
(4)在元素周期表中,砷( )位于第4周期,与P同主族。下列关于
)位于第4周期,与P同主族。下列关于 的推断中,正确的是
的推断中,正确的是_______ (填字母)。
a.原子的最外层电子数为5 b.原子半径: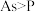 c.稳定性:
c.稳定性: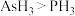
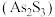 经常用来修改错字。
经常用来修改错字。(1)S在元素周期表中的位置是第
(2)写出S的最高价氧化物对应的水化物的化学式:
(3)S的非金属性强于P的,用原子结构解释原因:S和P在同一周期,原子核外电子层数相同,
(4)在元素周期表中,砷(
 )位于第4周期,与P同主族。下列关于
)位于第4周期,与P同主族。下列关于 的推断中,正确的是
的推断中,正确的是a.原子的最外层电子数为5 b.原子半径:
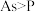 c.稳定性:
c.稳定性: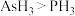
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】下表为元素周期表的一部分,表中a~f代表六种短周期主族元素。完成下列填空:
六种元素中,原子半径最大的是_________ (填元素编号) ;d、e、f三种元素的原子结构上的相同点是_______________________________ 。
| a | b | c |
| d | e | f |
六种元素中,原子半径最大的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】下表是元素周期表的一部分,表中字母分别代表一种元素。回答下列问题。
(1)表中所标元素,最活泼的金属元素形成简单离子符号为____ ;最不活泼的元素的原子结构示意图为 _____ ;其中一种元素的气态氢化物与其最高价氧化物的水化物可直接化合生成一种盐,该盐是_______ 。
(2)写出两种满足下列条件的物质______ (写化学式)。
①由c、x、e组成的;②含有共价键的离子化合物。
(3)g、x、y的气态氢化物,最稳定的是______ (填化学式)。
(4)表中元素的最高价氧化物的水化物中:酸性最强的是______ (填化学式,下同);碱性最强的是_______ ,这两种物质反应的离子方程式为_________ 。
(5)推测元素的非金属性:a______ g(填“>”或“<”)。利用图装置设计实验,证明推测结论。

①仪器A的名称为___________ ,干燥管D的作用是______________ 。
②填空。
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | a | b | c | d | ||||
| 3 | e | f | g | x | y | z |
(2)写出两种满足下列条件的物质
①由c、x、e组成的;②含有共价键的离子化合物。
(3)g、x、y的气态氢化物,最稳定的是
(4)表中元素的最高价氧化物的水化物中:酸性最强的是
(5)推测元素的非金属性:a

①仪器A的名称为
②填空。
| 装置内试剂 | C中发生反应的化学方程式 | ||
| A | B | C | |
| 稀硫酸 | 碳酸钠 | ||
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
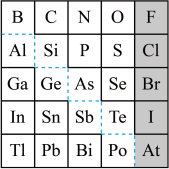
(1)元素Ga在元素周期表中的位置为:第________ 周期第________ 族。
(2)Sn的最高正价为________ ,Cl的最高价氧化物对应水化物的化学式为________ ,Bi的最高价氧化物为________ 。
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是________ 元素(填元素符号)。
②H3AsO4、H2SeO4的酸性强弱:H3AsO4________ (填“>”“<”或“=”)H2SeO4。
③氢化物的还原性:H2O________ (填“>”“<”或“=”)H2S。
④原子半径比较:N________ (填“>”“<”或“=”)Si。
(4)从下列试剂中选择最佳试剂组合,比较C、Si的非金属性强弱___________________ (可供选择的药品有:CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和Na2CO3溶液、硅酸钠溶液)

(1)元素Ga在元素周期表中的位置为:第
(2)Sn的最高正价为
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱:H3AsO4
③氢化物的还原性:H2O
④原子半径比较:N
(4)从下列试剂中选择最佳试剂组合,比较C、Si的非金属性强弱
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】某研究小组为探究元素周期表中元素性质的递变规律,设计了如下实验。
(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:___________ 与盐酸反应最剧烈,___________ 与盐酸反应产生的气体最多。
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为___________ 。
(3)NaH是离子化合物,能与水发生氧化还原反应生成H2,该反应的还原剂是___________ 。
(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为
(3)NaH是离子化合物,能与水发生氧化还原反应生成H2,该反应的还原剂是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】根据元素周期表中完整周期元素的性质,在下列空格中填上适当的元素符号。
(1)在第三周期中,第一电离能最小的元素是________ ,第一电离能最大的元素是________ 。
(2)在元素周期表中,电负性最大的元素是________
(3)第二周期,原子最外电子层中p能级半充满的元素是________ 。
(1)在第三周期中,第一电离能最小的元素是
(2)在元素周期表中,电负性最大的元素是
(3)第二周期,原子最外电子层中p能级半充满的元素是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】单晶边缘纳米催化剂技术为工业上有效利用二氧化碳提供了一条经济可行的途径,其中单晶氧化镁负载镍催化剂表现出优异的抗积碳和抗烧结性能。
(1)基态镍原子的核外电子排布式为___________ 。
(2)下列碳原子最外层电子排布图表示的状态中,能量最低的是___________ ;
A.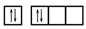 B.
B.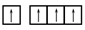 C.
C.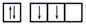 D.
D.
(3)氧化镁载体及镍催化反应中涉及到CH4、CO2和CH3OH等物质。元素Mg、O和C的第一电离能由小到大排序为___________ ;在上述三种物质的分子中碳原子杂化类型不同于其他两种的是___________ ,三种物质中沸点最高的是CH3OH,其原因是___________ 。
(1)基态镍原子的核外电子排布式为
(2)下列碳原子最外层电子排布图表示的状态中,能量最低的是
A.
 B.
B. C.
C. D.
D.
(3)氧化镁载体及镍催化反应中涉及到CH4、CO2和CH3OH等物质。元素Mg、O和C的第一电离能由小到大排序为
您最近一年使用:0次


 (选填“>”或“<”),下列事实与S、O非金属性比较无关的是
(选填“>”或“<”),下列事实与S、O非金属性比较无关的是 可与
可与 ,其最外层电子的轨道表示式是
,其最外层电子的轨道表示式是