配平下列氧化还原反应的方程式。
① HCl(浓)+ MnO2 Cl2↑+ MnCl2+ H2O
Cl2↑+ MnCl2+ H2O_____ 。
② KMnO4+ FeSO4+ H2SO4= K2SO4+ MnSO4+ Fe2(SO4)3+ H2O_____ 。
③ Na2SO3+ KIO3+ H2SO4= Na2SO4+ K2SO4+ I2+ H2O_____ 。
④ Au2O3+ Na2S2O3+ NaOH= Au2O+ Na2SO4+ H2O_____ 。
⑤ FeS+ O2= Fe2O3+ SO2_____ 。
⑥ KI+ KIO3+ H2SO4= I2+ K2SO4+ H2O_____ 。
① HCl(浓)+ MnO2
 Cl2↑+ MnCl2+ H2O
Cl2↑+ MnCl2+ H2O② KMnO4+ FeSO4+ H2SO4= K2SO4+ MnSO4+ Fe2(SO4)3+ H2O
③ Na2SO3+ KIO3+ H2SO4= Na2SO4+ K2SO4+ I2+ H2O
④ Au2O3+ Na2S2O3+ NaOH= Au2O+ Na2SO4+ H2O
⑤ FeS+ O2= Fe2O3+ SO2
⑥ KI+ KIO3+ H2SO4= I2+ K2SO4+ H2O
更新时间:2023-08-26 11:46:49
|
【知识点】 氧化还原反应方程式的配平解读
相似题推荐
【推荐1】H、C、N、O、Na、Cr是常见的六种元素。
(1)C位于元素周期表第____ 周期第___ 族;Cr的基态原子核外电子排布式为___________ ;C2H2分子中σ键与π键数目之比为____________ 。
(2)用“>”或“<”填空:
(3)25℃、101kPa下:①2Na(s)+1/2O2(g)=Na2O(s) ΔH=-414kJ·mol-1
②2Na(s)+O2(g)=Na2O2(s) ΔH=-511kJ·mol-1
写出Na2O2与单质钠化合成Na2O固体的热化学方程式_________________________ 。
(4)我国已经立法规定酒驾入刑。“酒精检测仪”中有红色CrO3和少量H2SO4,检测酒驾时产物有三价铬和CO2等,该反应的化学方程式为______________________________________ 。
(1)C位于元素周期表第
(2)用“>”或“<”填空:
| 电负性 | 键长 | 键的极性 | 沸点(同压) |
| C | C=C | N-H | 甲醇 |
②2Na(s)+O2(g)=Na2O2(s) ΔH=-511kJ·mol-1
写出Na2O2与单质钠化合成Na2O固体的热化学方程式
(4)我国已经立法规定酒驾入刑。“酒精检测仪”中有红色CrO3和少量H2SO4,检测酒驾时产物有三价铬和CO2等,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
名校
【推荐2】锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiClO4,溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。 回答下列问题:
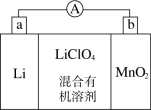
(1)外电路的电流方向是由________ 极流向________ 极(填字母)。
(2)电池正极反应式为___________________________________ 。
(3)是否可用水代替电池中的混合有机溶剂?________ (填“是”或“否”),原因是________________________________________________________________ 。
(4)MnO2可与KOH和KClO3在高温下反应,生成K2MnO4,反应的化学方程式为_______________________________________________ 。K2MnO4在酸性溶液中歧化,生成KMnO4和MnO2的物质的量之比为___________ 。

(1)外电路的电流方向是由
(2)电池正极反应式为
(3)是否可用水代替电池中的混合有机溶剂?
(4)MnO2可与KOH和KClO3在高温下反应,生成K2MnO4,反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某研究小组用黄铁矿(FeS2)、氯酸钠和硫酸溶液混合反应制备ClO2气体,再用水吸收该气体可得ClO2溶液。在此过程中需要控制适宜的温度,若温度不当,副反应增加,影响生成ClO2气体的纯度,且会影响ClO2的吸收率,具体情况如图所示。
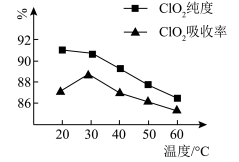
(1)据图可知,反应时需要控制的适宜温度是_____ ℃,要达到此要求需要采取的措施是_____ 。
(2)已知:黄铁矿中的硫元素在酸性条件下可被ClO 氧化成
氧化成 ,请写出FeS2、氯酸钠和硫酸溶液混合反应生成二氧化氯(ClO2)的离子方程式:
,请写出FeS2、氯酸钠和硫酸溶液混合反应生成二氧化氯(ClO2)的离子方程式:_____ 。
(3)CuSO4在酸性条件下能与FeS2反应生成难溶于水的Cu2S、 ,已知铁元素的化合价没有发生变化,写出该反应的离子方程式:
,已知铁元素的化合价没有发生变化,写出该反应的离子方程式:_____ 。
(4)实验室制备氯气的化学反应方程式为:_____ 。实验证明,很多物质都能与Cl-反应得到氯气,请写出重铬酸钾与盐酸反应生成Cr3+和氯气的离子方程式:_____ 。

(1)据图可知,反应时需要控制的适宜温度是
(2)已知:黄铁矿中的硫元素在酸性条件下可被ClO
 氧化成
氧化成 ,请写出FeS2、氯酸钠和硫酸溶液混合反应生成二氧化氯(ClO2)的离子方程式:
,请写出FeS2、氯酸钠和硫酸溶液混合反应生成二氧化氯(ClO2)的离子方程式:(3)CuSO4在酸性条件下能与FeS2反应生成难溶于水的Cu2S、
 ,已知铁元素的化合价没有发生变化,写出该反应的离子方程式:
,已知铁元素的化合价没有发生变化,写出该反应的离子方程式:(4)实验室制备氯气的化学反应方程式为:
您最近一年使用:0次



