为探究固体化合物X(仅含两种元素,100 g/mol<M<200 g/mol)的组成和性质,设计并完成如下实验:
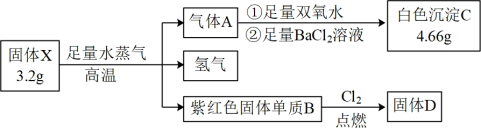
已知:气体A能使品红溶液褪色。请回答:
(1)固体D的化学式是___________ 。
(2)固体X的所含的元素是___________ 。(填元素符号)
(3)氢气是一种理想的绿色能源,点燃前须进行的操作是___________ 。
(4)写出气体A与双氧水反应的化学方程式___________ 。

已知:气体A能使品红溶液褪色。请回答:
(1)固体D的化学式是
(2)固体X的所含的元素是
(3)氢气是一种理想的绿色能源,点燃前须进行的操作是
(4)写出气体A与双氧水反应的化学方程式
更新时间:2023-07-17 10:18:38
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如下图所示(反应条件及其他物质已经略去):A B
B C
C D。
D。
(1)若A、D的水溶液均能使湿润的蓝色石蕊试纸变红,且D为强酸,则A、D分别为(填写化学式)A:___________ ,D:_________ .写出A→B转化的化学方程式:_______________ .
(2)若A的水溶液能使湿润的红色石蕊试纸变蓝,D的稀溶液能使蓝色的湿润石蕊试纸变红.则A为___________ ,写出A→B转化的化学方程式:_______________________ .
 B
B C
C D。
D。(1)若A、D的水溶液均能使湿润的蓝色石蕊试纸变红,且D为强酸,则A、D分别为(填写化学式)A:
(2)若A的水溶液能使湿润的红色石蕊试纸变蓝,D的稀溶液能使蓝色的湿润石蕊试纸变红.则A为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】从铜阳极泥分铜渣碱浸液中回收碲的工艺流程如图所示。 的形式存在;
的形式存在;
②Na2SO3可将Te(IV)还原为0价Te;
③TeO2与氧化铝的性质具有一定的相似性。
(1) 中Te的化合价为
中Te的化合价为_______ 价,“还原”中发生反应的离子方程式(该工艺条件下,Pb2+不沉淀)为_______ 。
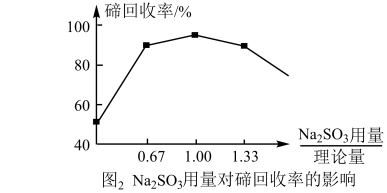
(2)“还原”过程中,反应温度、反应时间对碲回收率的影响如图1所示,工业上一般采取的条件为控制温度为75 °C ,反应时间为120 min,其原因是_______ 。_______ 。_______ 。
(5)加酸调pH时发生反应的化学方程式为_______ ,加入硫酸的量不宜过多,其原因是_______ 。

 的形式存在;
的形式存在;②Na2SO3可将Te(IV)还原为0价Te;
③TeO2与氧化铝的性质具有一定的相似性。
(1)
 中Te的化合价为
中Te的化合价为(2)“还原”过程中,反应温度、反应时间对碲回收率的影响如图1所示,工业上一般采取的条件为控制温度为75 °C ,反应时间为120 min,其原因是

(5)加酸调pH时发生反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同元素,它们可发生如图所示的转化反应(反应条件和部分产物已略去):甲 乙
乙 丙
丙
(1)若甲为目前使用最为广泛的金属,甲和丁的稀溶液反应生成无色气体。则丁的化学式为_______ , 检验乙溶液中的金属阳离子的方法为:_______ 。
(2)若甲为氯碱工业的产品,含丙的某种药品可用于治疗胃酸过多。则丁的化学式为_______ ,鉴别等浓度的乙溶液和丙溶液,可选用的试剂为_______ (填字母序号)。
A.NaOH溶液 B. CaCl2溶液 C.稀硫酸 D.澄清石灰水
(3)若甲为常用的净水剂,乙具有两性。则丁的化学式为_______ ,乙与丁反应生成丙的离子方程式为_______ 。
(4)若甲为臭鸡蛋气味的气体,丙为有刺激性气味的气体。则丁的化学式为_______ ,丙与甲反应生成乙的化学方程式为_______ 。
 乙
乙 丙
丙(1)若甲为目前使用最为广泛的金属,甲和丁的稀溶液反应生成无色气体。则丁的化学式为
(2)若甲为氯碱工业的产品,含丙的某种药品可用于治疗胃酸过多。则丁的化学式为
A.NaOH溶液 B. CaCl2溶液 C.稀硫酸 D.澄清石灰水
(3)若甲为常用的净水剂,乙具有两性。则丁的化学式为
(4)若甲为臭鸡蛋气味的气体,丙为有刺激性气味的气体。则丁的化学式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】海水是资源宝库,可利用海水提溴:
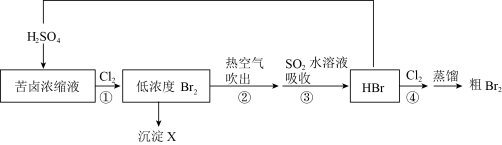
资料:常用提溴原料
(1)选用苦卤浓缩液而不是天然海水作为提溴原料的原因是___________ 。
(2)海水中溴元素的存在形式是Br—,从原子结构角度解释反应①能发生的原因:___________ 。
(3)步骤③反应的化学方程式是___________ 。
(4)在海水提溴生产工艺中,通常通过蒸馏法实现溴和水的分离(蒸馏是利用物质的沸点不同而实现分离的办法)。在蒸馏的过程中,温度应控制在80~90℃,温度过高或过低都不利于生产,请解释其原因___________ 。
(5)若步骤④中通入960g SO2,实际产出Br2的质量为1920g,则实际产量Br2的产率为___________ 。(产率=实际产量/理论产量×100%)

资料:常用提溴原料
| 提溴原料 | 天然海水 | 苦卤浓缩液(浓缩海水) |
| 溴含量(g·L-1) | 0.045 | 7.270 |
(1)选用苦卤浓缩液而不是天然海水作为提溴原料的原因是
(2)海水中溴元素的存在形式是Br—,从原子结构角度解释反应①能发生的原因:
(3)步骤③反应的化学方程式是
(4)在海水提溴生产工艺中,通常通过蒸馏法实现溴和水的分离(蒸馏是利用物质的沸点不同而实现分离的办法)。在蒸馏的过程中,温度应控制在80~90℃,温度过高或过低都不利于生产,请解释其原因
(5)若步骤④中通入960g SO2,实际产出Br2的质量为1920g,则实际产量Br2的产率为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】海洋资源的利用具有非常广阔的前景。回答下列问题:
Ⅰ.海水提溴
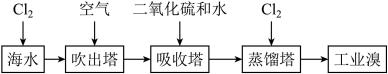
(1)吸收塔用二氧化硫和水吸收Br2的离子反应方程式:_____ 。
(2)蒸馏塔的蒸馏温度应控制在80-90℃最有利于生产,原因可能为:温度过高,_____ ;温度过低,_____ 。
Ⅱ.海水提镁
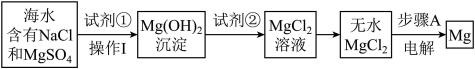
(3)工业上常用于沉淀Mg2+的廉价试剂①的俗名是_____ 。
(4)步骤A的化学方程式为_____ 。
Ⅲ.海带提碘
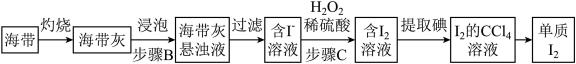
(5)步骤C中反应的离子方程式为_____ 。
Ⅰ.海水提溴

(1)吸收塔用二氧化硫和水吸收Br2的离子反应方程式:
(2)蒸馏塔的蒸馏温度应控制在80-90℃最有利于生产,原因可能为:温度过高,
Ⅱ.海水提镁

(3)工业上常用于沉淀Mg2+的廉价试剂①的俗名是
(4)步骤A的化学方程式为
Ⅲ.海带提碘

(5)步骤C中反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】 是常见的大气污染物,燃煤是产生
是常见的大气污染物,燃煤是产生 的主要原因。工业上有多种方法可以减少
的主要原因。工业上有多种方法可以减少 的排放。
的排放。
(1)往煤中添加一些生石灰,可使燃煤过程中产生的 转化成硫酸钙。该反应的化学方程式为
转化成硫酸钙。该反应的化学方程式为______ 。
(2)可用多种溶液做燃煤烟气中 的吸收液。
的吸收液。
①分别用等物质的量浓度的 溶液和NaOH溶液做吸收液,当生成等物质的量
溶液和NaOH溶液做吸收液,当生成等物质的量 时,两种吸收液体积比
时,两种吸收液体积比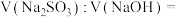
______ 。
②NaOH溶液吸收了足量的 后会失效,可将这种失效的溶液与一定量的石灰水溶液充分反应后过滤,使NaOH溶液再生,再生过程的离子方程式为
后会失效,可将这种失效的溶液与一定量的石灰水溶液充分反应后过滤,使NaOH溶液再生,再生过程的离子方程式为______ 。
(3)甲同学认为 溶液可以做
溶液可以做 的吸收液。为此甲同学设计如图实验(夹持装置和加热装置略,气密性已检验):
的吸收液。为此甲同学设计如图实验(夹持装置和加热装置略,气密性已检验):
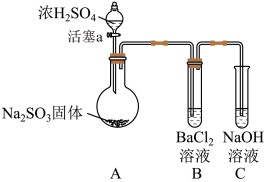
乙同学认为B中的白色沉淀是 ,产生
,产生 的原因是:
的原因是:
①A中产生的白雾是浓硫酸的酸雾,进入B中与 溶液反应生成
溶液反应生成 沉淀。
沉淀。
②______ 。
为证明 与
与 溶液不能得到
溶液不能得到 沉淀,乙同学对甲同学的实验装置做了如图改动并实验(夹持装置和加热装置略,气密性已检验):
沉淀,乙同学对甲同学的实验装置做了如图改动并实验(夹持装置和加热装置略,气密性已检验):
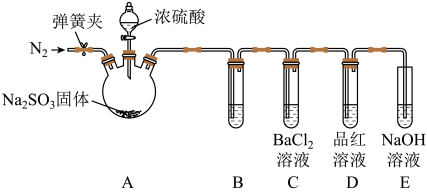
反应开始后,A中 固体表面有气泡产生同时有白雾生成;B、C试管中除了有气泡外,未见其他现象;D中红色褪去。
固体表面有气泡产生同时有白雾生成;B、C试管中除了有气泡外,未见其他现象;D中红色褪去。
③试管B中试剂是溶液______ ;滴加浓硫酸之前的操作是______ 。
④写出E装置的作用______ 。
⑤通过甲乙两位同学的实验,得出的结论是______ 。
 是常见的大气污染物,燃煤是产生
是常见的大气污染物,燃煤是产生 的主要原因。工业上有多种方法可以减少
的主要原因。工业上有多种方法可以减少 的排放。
的排放。(1)往煤中添加一些生石灰,可使燃煤过程中产生的
 转化成硫酸钙。该反应的化学方程式为
转化成硫酸钙。该反应的化学方程式为(2)可用多种溶液做燃煤烟气中
 的吸收液。
的吸收液。①分别用等物质的量浓度的
 溶液和NaOH溶液做吸收液,当生成等物质的量
溶液和NaOH溶液做吸收液,当生成等物质的量 时,两种吸收液体积比
时,两种吸收液体积比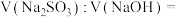
②NaOH溶液吸收了足量的
 后会失效,可将这种失效的溶液与一定量的石灰水溶液充分反应后过滤,使NaOH溶液再生,再生过程的离子方程式为
后会失效,可将这种失效的溶液与一定量的石灰水溶液充分反应后过滤,使NaOH溶液再生,再生过程的离子方程式为(3)甲同学认为
 溶液可以做
溶液可以做 的吸收液。为此甲同学设计如图实验(夹持装置和加热装置略,气密性已检验):
的吸收液。为此甲同学设计如图实验(夹持装置和加热装置略,气密性已检验):
已知: (固体)
(固体) (浓)
(浓)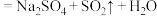 反应开始后,A中
反应开始后,A中 固体表面有气泡产生同时有白雾生成;B中有白色沉淀.甲认为B中白色沉淀是
固体表面有气泡产生同时有白雾生成;B中有白色沉淀.甲认为B中白色沉淀是 与
与 溶液反应生成的
溶液反应生成的 ,所以
,所以 溶液可做
溶液可做 吸收液。
吸收液。
乙同学认为B中的白色沉淀是
 ,产生
,产生 的原因是:
的原因是:①A中产生的白雾是浓硫酸的酸雾,进入B中与
 溶液反应生成
溶液反应生成 沉淀。
沉淀。②
为证明
 与
与 溶液不能得到
溶液不能得到 沉淀,乙同学对甲同学的实验装置做了如图改动并实验(夹持装置和加热装置略,气密性已检验):
沉淀,乙同学对甲同学的实验装置做了如图改动并实验(夹持装置和加热装置略,气密性已检验):
反应开始后,A中
 固体表面有气泡产生同时有白雾生成;B、C试管中除了有气泡外,未见其他现象;D中红色褪去。
固体表面有气泡产生同时有白雾生成;B、C试管中除了有气泡外,未见其他现象;D中红色褪去。③试管B中试剂是溶液
④写出E装置的作用
⑤通过甲乙两位同学的实验,得出的结论是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】 在工业生产中有着重要应用。利用以下装置制备
在工业生产中有着重要应用。利用以下装置制备 并测定产品纯度。
并测定产品纯度。
已知:Ⅰ. 是白色固体,不溶于水和乙醇,在潮湿空气中可被迅速氧化。
是白色固体,不溶于水和乙醇,在潮湿空气中可被迅速氧化。
Ⅱ.浓的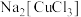 溶液为无色,加水稀释即析出
溶液为无色,加水稀释即析出 白色固体。
白色固体。

回答下列问题:
(1)①图中制取 的反应中,氧化剂和还原剂的物质的量之比为
的反应中,氧化剂和还原剂的物质的量之比为_____ 。
②装有浓盐酸的仪器名称为:_____ 。
③为吸收 尾气,C中可选用试剂
尾气,C中可选用试剂_____ (填标号)。
A. 溶液 B.饱和食盐水 C.浓
溶液 B.饱和食盐水 C.浓 D.
D. 溶液
溶液
(2)制备 :打开分液漏斗旋塞与搅拌器,装置B中依次发生反应的离子方程式为:
:打开分液漏斗旋塞与搅拌器,装置B中依次发生反应的离子方程式为:
①
②_____
③
观察到_____ 时停止反应。将B中溶液倾入盛有蒸馏水的烧杯中,立即得到白色 沉淀,抽滤得
沉淀,抽滤得 粗品。
粗品。
(3)洗涤 :洗涤时最好用95%的乙醇洗涤滤饼,其目的是
:洗涤时最好用95%的乙醇洗涤滤饼,其目的是_____ 。
(4) 纯度测定:称取所制备的氯化亚铜成品3.00g,将其置于过量的
纯度测定:称取所制备的氯化亚铜成品3.00g,将其置于过量的 溶液中,待样品完全溶解后,加入适量稀硫酸,配成250mL溶液。移取25.00mL溶液于锥形瓶中,用
溶液中,待样品完全溶解后,加入适量稀硫酸,配成250mL溶液。移取25.00mL溶液于锥形瓶中,用 的
的 溶液滴定至终点,再重复滴定2次,三次平均消耗
溶液滴定至终点,再重复滴定2次,三次平均消耗 溶液25.00mL(滴定过程中
溶液25.00mL(滴定过程中 转化为
转化为 ,
, 不反应)。
不反应)。
①产品中加入 溶液时,发生反应的离子方程式为
溶液时,发生反应的离子方程式为_____ ;
②产品中 的质量分数为
的质量分数为_____ 。
 在工业生产中有着重要应用。利用以下装置制备
在工业生产中有着重要应用。利用以下装置制备 并测定产品纯度。
并测定产品纯度。已知:Ⅰ.
 是白色固体,不溶于水和乙醇,在潮湿空气中可被迅速氧化。
是白色固体,不溶于水和乙醇,在潮湿空气中可被迅速氧化。Ⅱ.浓的
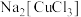 溶液为无色,加水稀释即析出
溶液为无色,加水稀释即析出 白色固体。
白色固体。
回答下列问题:
(1)①图中制取
 的反应中,氧化剂和还原剂的物质的量之比为
的反应中,氧化剂和还原剂的物质的量之比为②装有浓盐酸的仪器名称为:
③为吸收
 尾气,C中可选用试剂
尾气,C中可选用试剂A.
 溶液 B.饱和食盐水 C.浓
溶液 B.饱和食盐水 C.浓 D.
D. 溶液
溶液(2)制备
 :打开分液漏斗旋塞与搅拌器,装置B中依次发生反应的离子方程式为:
:打开分液漏斗旋塞与搅拌器,装置B中依次发生反应的离子方程式为:①

②
③

观察到
 沉淀,抽滤得
沉淀,抽滤得 粗品。
粗品。(3)洗涤
 :洗涤时最好用95%的乙醇洗涤滤饼,其目的是
:洗涤时最好用95%的乙醇洗涤滤饼,其目的是(4)
 纯度测定:称取所制备的氯化亚铜成品3.00g,将其置于过量的
纯度测定:称取所制备的氯化亚铜成品3.00g,将其置于过量的 溶液中,待样品完全溶解后,加入适量稀硫酸,配成250mL溶液。移取25.00mL溶液于锥形瓶中,用
溶液中,待样品完全溶解后,加入适量稀硫酸,配成250mL溶液。移取25.00mL溶液于锥形瓶中,用 的
的 溶液滴定至终点,再重复滴定2次,三次平均消耗
溶液滴定至终点,再重复滴定2次,三次平均消耗 溶液25.00mL(滴定过程中
溶液25.00mL(滴定过程中 转化为
转化为 ,
, 不反应)。
不反应)。①产品中加入
 溶液时,发生反应的离子方程式为
溶液时,发生反应的离子方程式为②产品中
 的质量分数为
的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】某实验小组以废催化剂(含SiO2、ZnS、CuS及少量的Fe3O4)为原料,回收锌和铜,设计实验流程如图:
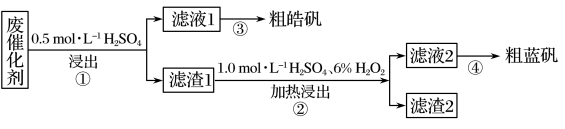
(1)在步骤①中,为提高浸出效率,可以采取的操作是_______ 、_______ (写出两种即可)。
(2) 粗皓矾的化学式为_______ ·7H2O,处理步骤①的污染气体可以用氢氧化钠溶液,利用到的原理为:_______ (用离子方程式表示)。
(3)在“滤液1”中,为检验是否含有Fe2+,可以采用的试剂是_______ ,若存在Fe2+,其现象为_______ 。
(4)已知蓝矾主要成分为:CuSO4·5H2O,步骤②发生主要反应的离子方程式为:_______ 。从“滤液2”中得到蓝矾的操作为:_______ 、_______ 、过滤、洗涤、干燥。

(1)在步骤①中,为提高浸出效率,可以采取的操作是
(2) 粗皓矾的化学式为
(3)在“滤液1”中,为检验是否含有Fe2+,可以采用的试剂是
(4)已知蓝矾主要成分为:CuSO4·5H2O,步骤②发生主要反应的离子方程式为:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】某工厂的废金属屑中主要成分为Cu、Fe和Al,此外还含有少量 和
和 ,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体
,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体 和胆矾晶体。请回答下列问题:
和胆矾晶体。请回答下列问题:
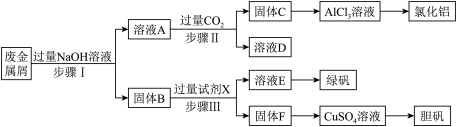
(1)写出步骤I反应的离子方程式__________________________________________________ ;
(2)步骤II中,溶液A中含铝化合物与过量 反应生成固体C的离⼦⽅程式为
反应生成固体C的离⼦⽅程式为____________ ;
(3)在步骤II时,⽤如图装置制取 并通入溶液A中。⼀段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,可采取的改进措施是
并通入溶液A中。⼀段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,可采取的改进措施是________ 。

(4)步骤III中试剂X是__________ 。
(5)取步骤III所得溶液E,滴加足量NaOH溶液,观察到的现象为__________ ,产生明显现象的化学方程式为__________ 。
 和
和 ,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体
,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体 和胆矾晶体。请回答下列问题:
和胆矾晶体。请回答下列问题:
(1)写出步骤I反应的离子方程式
(2)步骤II中,溶液A中含铝化合物与过量
 反应生成固体C的离⼦⽅程式为
反应生成固体C的离⼦⽅程式为(3)在步骤II时,⽤如图装置制取
 并通入溶液A中。⼀段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,可采取的改进措施是
并通入溶液A中。⼀段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,可采取的改进措施是
(4)步骤III中试剂X是
(5)取步骤III所得溶液E,滴加足量NaOH溶液,观察到的现象为
您最近一年使用:0次



