ABm型分子的价电子对数的计算方法
对于ABm型分子(A是中心原子,B是配位原子),分子的价电子对数可以通过下式确定:
价电子对数目(n)=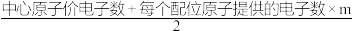
(1)中心原子的价电子数=___________ ;
(2)配位原子提供的价电子数:
卤素原子、氢原子按提供1个价电子数计算,O、S作为配位原子时按不提供价电子计算。如PCl5中n=___________ 。
(3)对于复杂离子,在计算价电子对数时,还应加上或减去离子所带的电荷数。如 中n=
中n=___________ , 中n=
中n=___________ 。
(4)若剩余1个电子,即出现奇数电子,也把这个单电子当作1对电子处理。如NO2中n=________ 。
对于ABm型分子(A是中心原子,B是配位原子),分子的价电子对数可以通过下式确定:
价电子对数目(n)=
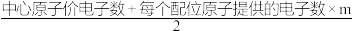
(1)中心原子的价电子数=
(2)配位原子提供的价电子数:
卤素原子、氢原子按提供1个价电子数计算,O、S作为配位原子时按不提供价电子计算。如PCl5中n=
(3)对于复杂离子,在计算价电子对数时,还应加上或减去离子所带的电荷数。如
 中n=
中n= 中n=
中n=(4)若剩余1个电子,即出现奇数电子,也把这个单电子当作1对电子处理。如NO2中n=
更新时间:2023-07-17 14:18:02
|
【知识点】 价层电子对互斥理论的应用解读
相似题推荐
填空题
|
较易
(0.85)
【推荐1】元素X的原子最外层电子排布式为nsnnpn+l。原子中能量最高的是______ 电子;元素X的氢化物的分子结构呈____ 形;该氢化物可以与H+离子以___ 键相合。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】根据要求完成下列问题。
(1)下列数据,前者小于后者的是_______ (填序号)。
①键长:N—N和 ②键能:
②键能: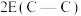 和
和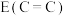
③键角: 和
和 ④键的极性:C—H和N—H
④键的极性:C—H和N—H
⑤沸点:邻羟基苯甲酸和对羟基苯甲酸 ⑥沸点: 和CO
和CO
(2)完成下表中的空白:
(1)下列数据,前者小于后者的是
①键长:N—N和
 ②键能:
②键能: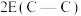 和
和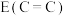
③键角:
 和
和 ④键的极性:C—H和N—H
④键的极性:C—H和N—H⑤沸点:邻羟基苯甲酸和对羟基苯甲酸 ⑥沸点:
 和CO
和CO(2)完成下表中的空白:
| 粒子 | VSEPR模型名称 | 分子(或离子)的空间结构 | 中心原子杂化轨道类型 |
| HCN | |||
 | |||
 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】在HF、H2O、NH3、CS2、CH4、N2、BF3分子中:
(1)以非极性键结合的非极性分子是________ ;
(2)以极性键结合的具有直线形结构的非极性分子是________ ;
(3)以极性键结合的具有正四面体形结构的非极性分子是________ ;
(4)以极性键结合的具有三角锥形结构的极性分子是________ ;
(5)以极性键结合的具有sp3杂化轨道结构的分子是________ ;
(6)以极性键结合的具有sp2杂化轨道结构的分子是________ 。
(1)以非极性键结合的非极性分子是
(2)以极性键结合的具有直线形结构的非极性分子是
(3)以极性键结合的具有正四面体形结构的非极性分子是
(4)以极性键结合的具有三角锥形结构的极性分子是
(5)以极性键结合的具有sp3杂化轨道结构的分子是
(6)以极性键结合的具有sp2杂化轨道结构的分子是
您最近一年使用:0次



