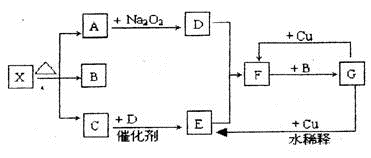
A是一种常见的铵盐,受热分解可得到B,B是碱性气体,C、D是常见的两种氧化物,E溶液显酸性。A、B、C、D、E是含有一种相同元素的五种化合物,在一定条件下可发生如图所示的转化。
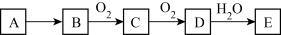
(1)B的化学式___________ ;D的颜色___________ ;
(2)实验室中常用A和另一种固体制备B,写出相应的化学方程式___________
(3)写出B到C的化学方程式___________
(4)已知E是一种常见的酸,E的稀溶液与铜反应的离子方程式___________ ,当消耗掉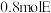 ,转移的电子数目是
,转移的电子数目是___________ (用 表示)
表示)
(5)汽车尾气中含有CO和NO,消除这两种物质对大气的污染的方法是安装催化转化器,使它们发生反应消除污染,试写出该反应的化学方程式:___________ 。

(1)B的化学式
(2)实验室中常用A和另一种固体制备B,写出相应的化学方程式
(3)写出B到C的化学方程式
(4)已知E是一种常见的酸,E的稀溶液与铜反应的离子方程式
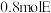 ,转移的电子数目是
,转移的电子数目是 表示)
表示)(5)汽车尾气中含有CO和NO,消除这两种物质对大气的污染的方法是安装催化转化器,使它们发生反应消除污染,试写出该反应的化学方程式:
更新时间:2023-07-17 22:04:15
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、X均为中学化学常见的纯净物,它们之间有如下转化关系(副产物已略去)。
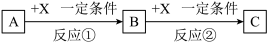
回答下列问题:
(1)若X是强氧化性气体单质,则A可能是_____ (填标号)。
a.C b.Al c.Na d.Mg
(2)若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,X在A中燃烧产生棕黄色的烟。
①B为_____ (填化学式)。
②C溶液在贮存时应加入少量X,理由是_____ (用离子方程式和必要的文字表示)。
③证明C溶液中存在该金属离子的操作方法是_____ 。
④向C的溶液中加入氢氧化钠溶液,观测到的实验现象是_____ ,此过程中属于氧化还原反应的化学方程式为_____ 。
(3)若A、B、C均为含有同种金属元素的化合物,X是强碱溶液或强酸溶液。
①B的化学式为_____ 。
②当X是强碱溶液时,反应①的离子方程式为_____ 。
③当X是强酸溶液时,反应①的离子方程式为_____ 。

回答下列问题:
(1)若X是强氧化性气体单质,则A可能是
a.C b.Al c.Na d.Mg
(2)若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,X在A中燃烧产生棕黄色的烟。
①B为
②C溶液在贮存时应加入少量X,理由是
③证明C溶液中存在该金属离子的操作方法是
④向C的溶液中加入氢氧化钠溶液,观测到的实验现象是
(3)若A、B、C均为含有同种金属元素的化合物,X是强碱溶液或强酸溶液。
①B的化学式为
②当X是强碱溶液时,反应①的离子方程式为
③当X是强酸溶液时,反应①的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E、F六种物质均是由短周期元素组成的中学常见的化学物质。它们之间的转化关系如下图(一定条件下)。A、C、E都为氢化物,三者中C的相对分子质量最小;A、C具有相同的电子数;D、E、F都为氧化物,且D、F皆为有毒气体。则:

(1)A:______ C:_______ D:_______ E:______ F:______ (填化学式)
(2)A、C、E三者沸点从高到低的顺序为____________________ (填化学式);
(3)A、C、E中稳定性最差的是____________________ (填化学式);

(1)A:
(2)A、C、E三者沸点从高到低的顺序为
(3)A、C、E中稳定性最差的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】如图是一些常见的单质,化合物之间的转化关系图,有些反应中的部分物质被唔去,常温常压下:A为无色有毒气体,B为红棕色粉末,C、E为金属单质.反应 均为工业上的重要反应:
均为工业上的重要反应:
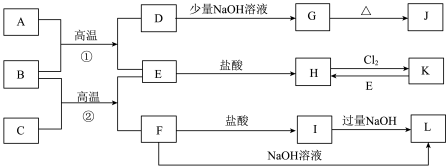
请回答下列问题:
(1) 的化学式为
的化学式为 ______ .
(2)写出C和NaOH溶液反应生成L的离子方程式:______ ;
(3)写出B与C高温反应生成E和F的化学方程式:______ ;
(4)写出D与J的稀溶液反应生成G的离子方程式:______ ;
 均为工业上的重要反应:
均为工业上的重要反应: 
请回答下列问题:
(1)
 的化学式为
的化学式为 (2)写出C和NaOH溶液反应生成L的离子方程式:
(3)写出B与C高温反应生成E和F的化学方程式:
(4)写出D与J的稀溶液反应生成G的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】化学自主实验小组通过实验探究NH3、NO2的性质。
探究I:利用如图所示装置探究NO2能否被NH3还原(K1、K2为止水夹,夹持固定装置略去)。
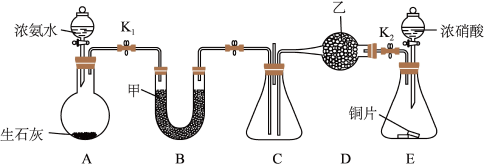
(1)A装置中制取NH3的化学方程式是____ 。
(2)甲、乙分别是____ (填字母)。
a.浓硫酸、碱石灰 b.碱石灰、碱石灰
c.碱石灰、无水氯化钙 d.五氧化二磷、五氧化二磷
(3)若NO2能够被NH3还原,预期C装置中能观察到的现象是____ 。
(4)此实验装置存在一个明显的缺陷是____ 。
探究II:探究NO2、O2混合气体的喷泉实验。
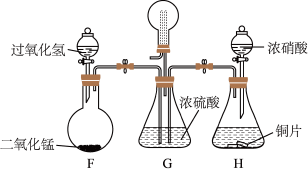
(5)请在G装置中的虚线上描出导管实线图___ 。
(6)G装置中浓硫酸有三种作用:混合NO2、O2气体;干燥NO2、O2;____ 。
(7)常温常压下,G装置上的圆底烧瓶集满气体进行喷泉实验,若最终液体充满整个烧瓶,则所得溶液物质的量浓度为___ mol·L-1(已知常温常压下气体摩尔体积为VL/mol)。
探究I:利用如图所示装置探究NO2能否被NH3还原(K1、K2为止水夹,夹持固定装置略去)。

(1)A装置中制取NH3的化学方程式是
(2)甲、乙分别是
a.浓硫酸、碱石灰 b.碱石灰、碱石灰
c.碱石灰、无水氯化钙 d.五氧化二磷、五氧化二磷
(3)若NO2能够被NH3还原,预期C装置中能观察到的现象是
(4)此实验装置存在一个明显的缺陷是
探究II:探究NO2、O2混合气体的喷泉实验。

(5)请在G装置中的虚线上描出导管实线图
(6)G装置中浓硫酸有三种作用:混合NO2、O2气体;干燥NO2、O2;
(7)常温常压下,G装置上的圆底烧瓶集满气体进行喷泉实验,若最终液体充满整个烧瓶,则所得溶液物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】下图为实验室制取氨气,二硫氨气体及相关性质实验的组合装置。
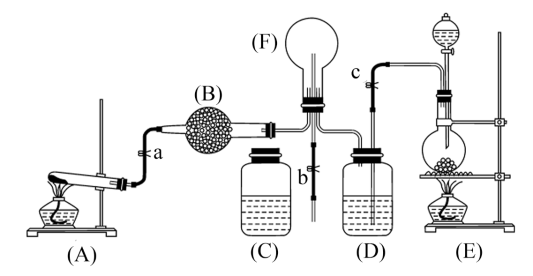
(1)A 、A 、A中取系统的化学反应为如果是E_____ 。
(2)仪器B的名称为_______ ,在此实验中B应加入_______ (写名)。
(3)当F中充满A中气体后,A停止制气,a ,打开弹簧夹c ,使先E中气体通入F中;
①如何测知F中已经充满了中产的气体:_______ ;
② D的作用是干燥的气体,D中盛是_______ (写名称);
③ E后,触发F中气体反应器的操作反应器燃烧瓶与塑料连接,并完成展开实验,F中触发的化学反应为进入,_______ 。
(4)A 、E中产生的气体都是有污染性的,其中包括E中产生尾气的成分为_______ 。

(1)A 、A 、A中取系统的化学反应为如果是E
(2)仪器B的名称为
(3)当F中充满A中气体后,A停止制气,a ,打开弹簧夹c ,使先E中气体通入F中;
①如何测知F中已经充满了中产的气体:
② D的作用是干燥的气体,D中盛是
③ E后,触发F中气体反应器的操作反应器燃烧瓶与塑料连接,并完成展开实验,F中触发的化学反应为进入,
(4)A 、E中产生的气体都是有污染性的,其中包括E中产生尾气的成分为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】叠氮化钠(NaN3)是易溶于水的白色晶体,微溶于乙醇。不溶于乙醚,常用作汽车安全气囊中的药剂,实验室制取叠氮化钠的原理、实验装置(图甲)及实验步骤如下:
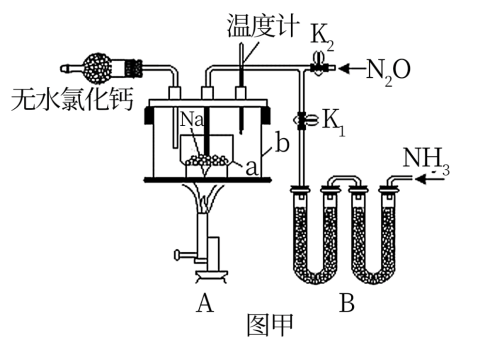
①关闭止水夹K2,打开止水夹K1,制取并通入氨气。
②加热装置A中的金属钠,使其熔化并充分反应后,停止通入氨气并关闭止水夹K1。
③向装置A中的b容器内充入加热介质,并加热到210~220 ℃,然后打开止水夹K2,通入Na2O。
请回答下列问题:

(1)盛放无水氯化钙的仪器名称是___________ ,图乙中可用来制取氨气的装置有___________ (填标号)。
(2)步骤①中先通氨气的目的是___________ ,步骤②氨气与熔化的钠反应生成NaNH2的化学方程式为___________ ,步骤③中最适宜的加热方式为___________ (填标号)。
a水浴加热 b.油浴加热 c.酒精灯直接加热
(3)生成NaN3的化学方程式为___________ 。
(4)反应结束后,进行以下操作,得到NaN3固体(NaNH2能与水反应生成NaOH和氨气)。
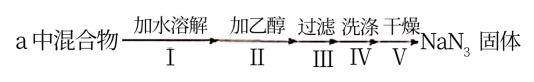
操作II的目的是___________ ,操作IV最好选用的试剂是___________ 。

①关闭止水夹K2,打开止水夹K1,制取并通入氨气。
②加热装置A中的金属钠,使其熔化并充分反应后,停止通入氨气并关闭止水夹K1。
③向装置A中的b容器内充入加热介质,并加热到210~220 ℃,然后打开止水夹K2,通入Na2O。
请回答下列问题:

(1)盛放无水氯化钙的仪器名称是
(2)步骤①中先通氨气的目的是
a水浴加热 b.油浴加热 c.酒精灯直接加热
(3)生成NaN3的化学方程式为
(4)反应结束后,进行以下操作,得到NaN3固体(NaNH2能与水反应生成NaOH和氨气)。

操作II的目的是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】氮氧化物、二氧化硫能引发酸雨、雾霾等。回答下列问题:
(1) 产生硝酸型酸雨的化学方程式为
产生硝酸型酸雨的化学方程式为_____ 。
(2)汽车尾气催化转化器可将尾气中的 均转化为无害气体,该反应的还原产物为
均转化为无害气体,该反应的还原产物为_____ 。
(3)目前工业上烟气脱硫脱硝的工艺流程如下: 。
。
①“催化氧化”的目的是_____ 。
②图中“产品”中含硫成分为_____ (填化学式)。
(4)氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧化制硝酸的流程示意图。_____ 。
②写出氧化炉中的化学反应方程式:_____ 。
(1)
 产生硝酸型酸雨的化学方程式为
产生硝酸型酸雨的化学方程式为(2)汽车尾气催化转化器可将尾气中的
 均转化为无害气体,该反应的还原产物为
均转化为无害气体,该反应的还原产物为(3)目前工业上烟气脱硫脱硝的工艺流程如下:
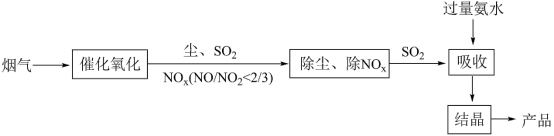
 。
。①“催化氧化”的目的是
②图中“产品”中含硫成分为
(4)氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧化制硝酸的流程示意图。
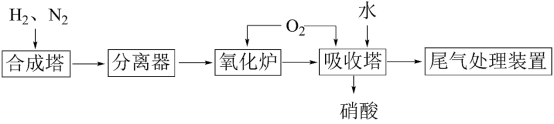
②写出氧化炉中的化学反应方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.汽车尾气是城市空气的污染源之一。治理的方法之一是在汽车的排气管上装一个“催化转换器”。它可以使CO与NO反应,生成可参与大气循环的无毒气体。
(1)下列与汽车尾气的排放密切相关的是___________ (填序号)。
A.光化学烟雾 B.水体富营养化与赤潮
C.白色污染 D.雾霾
(2)写出一氧化碳与一氧化氮反应的化学方程式:________________
Ⅱ.减少交通事故除遵守交通法规正确驾驶外,安全措施也极为重要。汽车的安全气囊内有叠氮化钠(NaN) I 与硝酸钱(NH4NO3)等物质。当汽车在高速行驶中受到猛烈撞击时,这些物质会迅速发生分解反应,产生大量气体,充满气囊,从而保护驾驶员和乘客的安全。
(3)下列判断正确的是____________ 填序号)。
A.道路起雾与H2O分子中的化学键断裂有关
B.NH4NO3中只含有极性共价键
C.NaN3受到猛烈撞击时有化学键的断裂
D.NaN3、NH4NO3均属于离子化合物
(4)汽车的安全气囊内叠氮化钠爆炸过程中的能量变化如图所示:
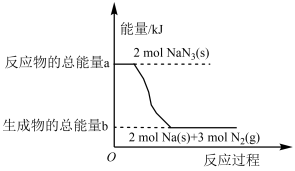
①叠氮化钠的爆炸反应属于__________ (填“吸热”或“放热”)反应。
②若上述爆炸过程中的能量变化为2(a-b)kJ,则消耗叠氮化钠的质量为__________ g。
③若安全气囊的体积为V L,NaN3的爆炸在ts内完成,反应过程中消耗292.5 g NaN3,则用N2表示的反应速率为____________ mol • L-1• s-1。
(1)下列与汽车尾气的排放密切相关的是
A.光化学烟雾 B.水体富营养化与赤潮
C.白色污染 D.雾霾
(2)写出一氧化碳与一氧化氮反应的化学方程式:
Ⅱ.减少交通事故除遵守交通法规正确驾驶外,安全措施也极为重要。汽车的安全气囊内有叠氮化钠(NaN) I 与硝酸钱(NH4NO3)等物质。当汽车在高速行驶中受到猛烈撞击时,这些物质会迅速发生分解反应,产生大量气体,充满气囊,从而保护驾驶员和乘客的安全。
(3)下列判断正确的是
A.道路起雾与H2O分子中的化学键断裂有关
B.NH4NO3中只含有极性共价键
C.NaN3受到猛烈撞击时有化学键的断裂
D.NaN3、NH4NO3均属于离子化合物
(4)汽车的安全气囊内叠氮化钠爆炸过程中的能量变化如图所示:

①叠氮化钠的爆炸反应属于
②若上述爆炸过程中的能量变化为2(a-b)kJ,则消耗叠氮化钠的质量为
③若安全气囊的体积为V L,NaN3的爆炸在ts内完成,反应过程中消耗292.5 g NaN3,则用N2表示的反应速率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】工业生产硝酸的尾气中含有氮氧化物NOx(假设仅为NO和NO2的混合物),影响生态环境。
I.氮氧化物NOx对环境主要影响有两点___ 、___ 。
II.工业上可用氨催化吸收法处理NOx,反应原理为:NH3+NOx N2+H2O某化学兴趣小组模拟该处理过程的实验装置如图:
N2+H2O某化学兴趣小组模拟该处理过程的实验装置如图:
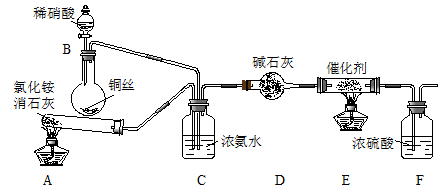
(1)装置A中发生反应的化学方程式为___ 。
(2)装置C的作用有两个:一个作用是通过气泡产生的速率来控制反应物的比例,另一个作用是___ 。
(3)反应6NO2+8NH3 7N2+12H2O可用于处理NO2。当转移3.6mol电子时,消耗NO2的物质的量为
7N2+12H2O可用于处理NO2。当转移3.6mol电子时,消耗NO2的物质的量为___ mol。
III.工业上也常用NaOH溶液吸收法处理NOx:
NO+NO2+2NaOH=2NaNO2+H2O(I)
2NO2+2NaOH=NaNO2+NaNO3+H2O(II)
(1)当NOx被NaOH溶液完全吸收时,NO、NO2的物质的量之比为___ 。
(2)2240mL(标准状况)NO和NO2的混合气体溶于200mLNaOH溶液中,恰好完全反应,并无气体放出,则NaOH溶液物质的量浓度是___ 。
I.氮氧化物NOx对环境主要影响有两点
II.工业上可用氨催化吸收法处理NOx,反应原理为:NH3+NOx
 N2+H2O某化学兴趣小组模拟该处理过程的实验装置如图:
N2+H2O某化学兴趣小组模拟该处理过程的实验装置如图:
(1)装置A中发生反应的化学方程式为
(2)装置C的作用有两个:一个作用是通过气泡产生的速率来控制反应物的比例,另一个作用是
(3)反应6NO2+8NH3
 7N2+12H2O可用于处理NO2。当转移3.6mol电子时,消耗NO2的物质的量为
7N2+12H2O可用于处理NO2。当转移3.6mol电子时,消耗NO2的物质的量为III.工业上也常用NaOH溶液吸收法处理NOx:
NO+NO2+2NaOH=2NaNO2+H2O(I)
2NO2+2NaOH=NaNO2+NaNO3+H2O(II)
(1)当NOx被NaOH溶液完全吸收时,NO、NO2的物质的量之比为
(2)2240mL(标准状况)NO和NO2的混合气体溶于200mLNaOH溶液中,恰好完全反应,并无气体放出,则NaOH溶液物质的量浓度是
您最近一年使用:0次
【推荐1】某研究性学习小组利用硝酸和废铜屑(含Cu和CuO)作为原料制备硝酸铜,设计的流程如下:
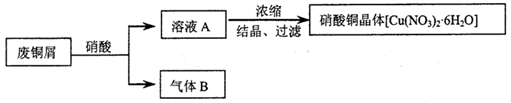
(1)某次实验使用了废铜屑共24g,用一定浓度的硝酸100mL完全溶解这些废铜屑时,共收集到标准状况下B气体6.72L(其中NO2 和NO的体积比为2∶1)。请通过计算回答下列问题:
①废铜屑中铜和氧化铜的物质的量之比_____________ 。
②若测得溶液A中H+的浓度为1mol·L-1,则原硝酸的物质的量浓度为________________ 。(假设反应前后溶液的体积不变)
(2)上述制备方案中产生的气体B,既造成原料的浪费,也污染了环境。请你设计方案解决上述问题___________________________________________________________________________ 。

(1)某次实验使用了废铜屑共24g,用一定浓度的硝酸100mL完全溶解这些废铜屑时,共收集到标准状况下B气体6.72L(其中NO2 和NO的体积比为2∶1)。请通过计算回答下列问题:
①废铜屑中铜和氧化铜的物质的量之比
②若测得溶液A中H+的浓度为1mol·L-1,则原硝酸的物质的量浓度为
(2)上述制备方案中产生的气体B,既造成原料的浪费,也污染了环境。请你设计方案解决上述问题
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】已知A、J为常见金属单质,常温下B为液体化合物,E是空气的主要成分之一,L是蓝色沉淀,H为红棕色气体;它们之间的转换关系如下图所示:
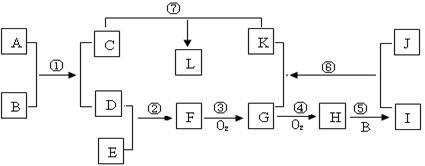
(1)H的化学式是________ 。
(2)③的化学方程式是__________________________________ 。
(3)⑥的离子方程式是_______________________________ 。
(4)F名称是________ ,检验此气体的方法是_____________ 。

(1)H的化学式是
(2)③的化学方程式是
(3)⑥的离子方程式是
(4)F名称是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】下图的各方框表示有关的一种反应物或生成物(某些物质已经略去),其中常温下A、C、D、E为无色气体,C能使湿润的红色石蕊试纸变蓝,B常温下为无色液体,Fe遇浓的G溶液钝化。
(1)写出下列各物质的化学式:
B:____________ ;F:____________ ;G:___________ 。
(2)写出下列变化的反应方程式:
A→D:________________________________________ ;
G→E:________________________________________ 。
(3)实验室里,常用加热_____________________ 的混合物的方法制取气体C,常采用____________ 法来收集。

(1)写出下列各物质的化学式:
B:
(2)写出下列变化的反应方程式:
A→D:
G→E:
(3)实验室里,常用加热
您最近一年使用:0次



