回答下列问题。
I.有一包白色固体粉末,其中可能含有NaCl、Ba(NO3)2、CuSO4、Na2CO3中的一种或几种,现做以下实验:
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤,溶液呈无色:
②向①的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生;
③取少量②的溶液,滴入稀硫酸,有白色沉淀产生;
④另取①中过滤后的溶液加入足量 AgNO3溶液,产生白色沉淀。
根据上述实验事实,回答下列问题:
(1)原白色粉末中一定含有的是___________ ,可能含有的是___________ 。(写化学式)
(2)步骤②中的离子方程式___________ 。
Ⅱ.人体胃液中含有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,用适量的小苏打(NaHCO3)能治疗胃酸过多。
(3)小苏打在水中的电离方程式:___________ 。
(4)不可以服用 BaCO3来治疗胃酸过多,理由是___________ 。
(5)如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是 Al(OH)3],反应的离子方程式为___________ 。
I.有一包白色固体粉末,其中可能含有NaCl、Ba(NO3)2、CuSO4、Na2CO3中的一种或几种,现做以下实验:
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤,溶液呈无色:
②向①的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生;
③取少量②的溶液,滴入稀硫酸,有白色沉淀产生;
④另取①中过滤后的溶液加入足量 AgNO3溶液,产生白色沉淀。
根据上述实验事实,回答下列问题:
(1)原白色粉末中一定含有的是
(2)步骤②中的离子方程式
Ⅱ.人体胃液中含有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,用适量的小苏打(NaHCO3)能治疗胃酸过多。
(3)小苏打在水中的电离方程式:
(4)不可以服用 BaCO3来治疗胃酸过多,理由是
(5)如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是 Al(OH)3],反应的离子方程式为
更新时间:2023-08-19 12:11:10
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】Ⅰ.现有下列物质:①铜 ②CO2 ③稀硝酸 ④CH4 ⑤硫酸溶液 ⑥NaOH固体 ⑦氨水⑧NH3 ⑨NaHSO4固体 ⑩NaCO3•10H2O晶体 ⑪BaSO4 ⑫酒精溶液
(1)上述物质可导电的有___ (填编号,下同);
(2)属于电解质的有___ ,属于非电解质的有___ 。
(3)将⑨溶于水配成溶液,其电离方程式为___ 。
Ⅱ.工业上通常用工业酒精和生石灰混合蒸馏法制取无水乙醇。如图是实验室中模拟工业原理制取无水乙醇的装置。

回答下列问题:
(1)图中除了忘记添加沸石还存在的错误有___ 、___ 、___ 。
(2)该方法除去工业酒精中的水的原理是(用化学方程式表示)___ 。
(3)装置中仪器B、C的名称分别是B__ 、C___ 。
(4)在蒸馏操作中,仪器B中加入沸石(或碎瓷片)的作用是__ 。实验开始后若发现忘记添加沸石,则应___ 。
(1)上述物质可导电的有
(2)属于电解质的有
(3)将⑨溶于水配成溶液,其电离方程式为
Ⅱ.工业上通常用工业酒精和生石灰混合蒸馏法制取无水乙醇。如图是实验室中模拟工业原理制取无水乙醇的装置。

回答下列问题:
(1)图中除了忘记添加沸石还存在的错误有
(2)该方法除去工业酒精中的水的原理是(用化学方程式表示)
(3)装置中仪器B、C的名称分别是B
(4)在蒸馏操作中,仪器B中加入沸石(或碎瓷片)的作用是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】A~D为核电荷数小于18的元素,其性质或结构信息如下表:
请根据表中的信息回答下列问题:
(1)四种元素名称为:A______ ;B______ ;C______ ;D________ ;
(2)B原子的结构示意图:________ ;
(3)由A、B、D三种元素构成的物质中含有的化学键类型___ ,写出该物质的电子式:___ ,写出该物质在水中的电离方程式_____ 。D与硫元素形成的化合物水溶液跟单质C的水溶液混合发生置换反应,其离子方程式为_______ 。
(4)AC的浓溶液与化合物DCB3的溶液反应生成C的单质,其中的还原反应为_____ →_____ (用化学式表示),每有1molDCB3参加反应,电子转移______ mol。
(5)有某AC的浓溶液,密度为1.19g/cm3,质量百分比浓度为36.5%,其物质的量浓度为____ 。
| 元素 | A | B | C | D |
| 性质或 结构信息 | 原子核内只有 1个质子 | 海水中含量最多,其原子有2个电子层 | 其阴离子是构成食盐的粒子 | 其原子的M电子层上只有1个电子 |
(1)四种元素名称为:A
(2)B原子的结构示意图:
(3)由A、B、D三种元素构成的物质中含有的化学键类型
(4)AC的浓溶液与化合物DCB3的溶液反应生成C的单质,其中的还原反应为
(5)有某AC的浓溶液,密度为1.19g/cm3,质量百分比浓度为36.5%,其物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】有一包白色粉末,可能是CuSO4、CaCO3、BaCl2、Na2SO4、NaOH中的一种或几种,为证明其组成,进行如下实验:
(1)取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液,则白色沉淀可能是_____ ,原混合物中一定不含有_______ 。
(2)向实验(1)滤出的白色沉淀中加入足量的盐酸,沉淀全部溶解,并产生无色气体,则原混合物中一定含有_______ 。
(3)将实验(1)中得到的滤液分成两份,将实验(2)中产生的无色气体先通入其中的一份,无沉淀产生。气体导出后再通入另一份滤液中,立即产生白色沉淀,再过滤。出现上述现象的原因是实验(2)中产生的气体里含有______ 。
(4)向实验(3)中过滤后所得的滤液里加入AgNO3溶液和稀硝酸,又产生白色沉淀,根据此现象推断,原混合物中一定还含有____ ,根据实验全过程推断,原混合物中还含有____ 。
(1)取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液,则白色沉淀可能是
(2)向实验(1)滤出的白色沉淀中加入足量的盐酸,沉淀全部溶解,并产生无色气体,则原混合物中一定含有
(3)将实验(1)中得到的滤液分成两份,将实验(2)中产生的无色气体先通入其中的一份,无沉淀产生。气体导出后再通入另一份滤液中,立即产生白色沉淀,再过滤。出现上述现象的原因是实验(2)中产生的气体里含有
(4)向实验(3)中过滤后所得的滤液里加入AgNO3溶液和稀硝酸,又产生白色沉淀,根据此现象推断,原混合物中一定还含有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E 5瓶透明溶液,分别是HCl、BaCl2、NaHSO4、Na2CO3、AgNO3溶液中的一种。已知:
①A与B反应有气体生成 ②B与C反应有沉淀生成
③C与D反应有沉淀生成 ④D与E反应有沉淀生成
⑤A与E反应有气体生成 ⑥在②和③的反应中生成的沉淀是同一种物质
请填空:
(1)在②和③的反应中,生成的沉淀物质的化学式(分子式)是______ 。
(2)A是______ ,B是_________ ,C是__________ ,D是________ ,E是_________ 。
①A与B反应有气体生成 ②B与C反应有沉淀生成
③C与D反应有沉淀生成 ④D与E反应有沉淀生成
⑤A与E反应有气体生成 ⑥在②和③的反应中生成的沉淀是同一种物质
请填空:
(1)在②和③的反应中,生成的沉淀物质的化学式(分子式)是
(2)A是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】某无色透明溶液中除了H+和OH-,可能大量存在Ag+、Mg2+、Cu2+、Fe3+、Na+、 、
、 中的几种,请填写下列空白:
中的几种,请填写下列空白:
(1)不用做任何实验就可以肯定原溶液中一定不存在的离子是_________ ,一定存在的离子是__________ 。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是______________ 。
(3)取(2)中滤液,加入过量的氢氧化钠溶液,出现白色沉淀,说明原溶液中肯定有______ ,写出加入氢氧化钠溶液发生反应的离子方程式:__________ 。
 、
、 中的几种,请填写下列空白:
中的几种,请填写下列空白:(1)不用做任何实验就可以肯定原溶液中一定不存在的离子是
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是
(3)取(2)中滤液,加入过量的氢氧化钠溶液,出现白色沉淀,说明原溶液中肯定有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】膨松剂是一种食品添加剂。膨松剂反应产生气体的量作为检验膨松剂品质的一项重要指标。已知某膨松剂含碳酸氢钠、碳酸氢铵中的一种或两种,化学兴趣小组对该膨松剂进行如下探究:
查阅资料:碱石灰是固体氢氧化钠与氧化钙的混合
实验一:检验膨松剂成分

在玻璃管中加入该膨松剂,按右图连接好装置(铁架台略去,下同)。点燃酒精灯:
(1)关闭铁夹1,打开铁夹2,观察到___________ ,说明膨松剂中没有碳酸氢铵;
(2)打开铁夹1,关闭铁夹2,观察到___________ ,说明膨松剂中有碳酸氢钠;
结论:膨松剂含碳酸氢钠
实验二:测定膨松剂受热产生气体的量,测定膨松剂中碳酸氢钠的含量。
将质量为 的膨松剂样品装入装置B中,用下图装置测定该膨松剂样品产生的二氧化碳气体的质量(整套装置气密性良好,各装置中气体吸收剂足量)。
的膨松剂样品装入装置B中,用下图装置测定该膨松剂样品产生的二氧化碳气体的质量(整套装置气密性良好,各装置中气体吸收剂足量)。
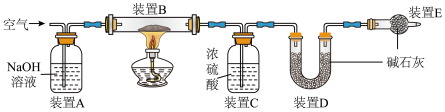
(3)在加热前,先对装置A、B和C(已连接)通一段时间的空气,再连接上装置D、E.装置A的作用是___________ ;装置C的作用___________ 。
(4)测定实验前后装置___________ (填装置名称)的质量,其质量差即为产CO2的质量;若没有装置E,造成测定二氧化碳气体的质量结果___________ (填“偏大”、“不变”或“偏小”)。
(5)充分反应后,停止加热,测得装置B中固体的质量为 。停止加热后,仍继续通入空气一段时间,目的是
。停止加热后,仍继续通入空气一段时间,目的是___________ 。
(6)若上述实验测得CO2的质量为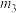 ,则该膨松剂中碳酸氢钠的质量分数为
,则该膨松剂中碳酸氢钠的质量分数为___________ 。
查阅资料:碱石灰是固体氢氧化钠与氧化钙的混合
实验一:检验膨松剂成分

在玻璃管中加入该膨松剂,按右图连接好装置(铁架台略去,下同)。点燃酒精灯:
(1)关闭铁夹1,打开铁夹2,观察到
(2)打开铁夹1,关闭铁夹2,观察到
结论:膨松剂含碳酸氢钠
实验二:测定膨松剂受热产生气体的量,测定膨松剂中碳酸氢钠的含量。
将质量为
 的膨松剂样品装入装置B中,用下图装置测定该膨松剂样品产生的二氧化碳气体的质量(整套装置气密性良好,各装置中气体吸收剂足量)。
的膨松剂样品装入装置B中,用下图装置测定该膨松剂样品产生的二氧化碳气体的质量(整套装置气密性良好,各装置中气体吸收剂足量)。
(3)在加热前,先对装置A、B和C(已连接)通一段时间的空气,再连接上装置D、E.装置A的作用是
(4)测定实验前后装置
(5)充分反应后,停止加热,测得装置B中固体的质量为
 。停止加热后,仍继续通入空气一段时间,目的是
。停止加热后,仍继续通入空气一段时间,目的是(6)若上述实验测得CO2的质量为
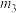 ,则该膨松剂中碳酸氢钠的质量分数为
,则该膨松剂中碳酸氢钠的质量分数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】有A、B两种常见化合物,其焰色反应均呈黄色,B的俗名叫小苏打,是发酵粉的主要成分,C是一种单质气体,相互转化关系如图所示(其他物质均已略去)。
回答下列问题:

(1)A的化学式________________ ,B的化学式_______________________
(2)B加稀硫酸产生D的离子方程式_________
(3)A与D反应的化学方程式_________ ,由此反应写出A的一种重要用途___________________
(4) A、B在密闭装置中加热,充分反应后,若只得到一种固体化合物,E的化学式为_________
回答下列问题:

(1)A的化学式
(2)B加稀硫酸产生D的离子方程式
(3)A与D反应的化学方程式
(4) A、B在密闭装置中加热,充分反应后,若只得到一种固体化合物,E的化学式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】利用熔融焙烧工艺可从铝热法生产金属铬所得铬渣(含Al、Al2O3、Cr2O3、SiO2)中浸出铝和铬,实现铬和铝的再生利用,其工艺流程如下: 。
。
(1)铬渣粉碎的目的是______ 。
(2)操作I、II、III中所用到的玻璃仪器有玻璃棒、_____ 、烧杯,滤渣A的主要成分是____ (填化学式)。
(3)滤液a中通入O2发生反应的离子方程式为___________ 。
(4)滤渣B的主要成分为氢氧化铝,滤渣C受热分解所得的物质可以循环利用。
①滤渣B在工业、医疗等方面都有广泛的应用,其在医疗上主要用于______ 。
②滤渣C受热分解后可循环利用的物质有_____ (填化学式),其受热分解的化学方程式为___ 。

 。
。(1)铬渣粉碎的目的是
(2)操作I、II、III中所用到的玻璃仪器有玻璃棒、
(3)滤液a中通入O2发生反应的离子方程式为
(4)滤渣B的主要成分为氢氧化铝,滤渣C受热分解所得的物质可以循环利用。
①滤渣B在工业、医疗等方面都有广泛的应用,其在医疗上主要用于
②滤渣C受热分解后可循环利用的物质有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知六种短周期元素A、B、C、D、E、F的原子序数依次增大,A的原子核内没有中子,A、D同主族,C、F同主族,A和B可形成5核10电子的阳离子,C与D形成的离子化合物D2C中所有离子的电子数相同,E的最高价氧化物的水化物可与D、F的最高价氧化物的水化物反应。试回答下列问题:
(1)E在元素周期表中的位置是___________ 。
(2)写出A和B形成4核10电子分子的电子式和结构式___________ 、___________ 。
(3)C、D、F的简单离子半径由大到小的顺序为(用离子符号表示)___________ 。
(4)根据“对角线规则”,铍(Be)的性质与上述六种元素中的___________ (填名称)相似,能溶于氢氧化钠溶液,生成Na2BeO2与H2。请写出氢氧化铍与氢氧化钠溶液反应的化学方程式___________ 。
(5)A、C、D可形成多种二元化合物。下列说法不正确的是___________(填字母)。
(6)能说明氯的非金属性比F强的事实是___________(填字母)。
①F的最高价氧化物水化物比次氯酸稳定
②高氯酸的酸性比F的最高价氧化物的水化物的酸性强
③F的简单阴离子比Cl—易被氧化
④HCl比F的氢化物稳定
⑤铜与盐酸不反应,但能与F的最高价氧化物的水化物的浓溶液反应
⑥铁与氯气在加热条件下反应生成氯化铁,铁与F单质在加热条件下反应生成某化亚铁
(1)E在元素周期表中的位置是
(2)写出A和B形成4核10电子分子的电子式和结构式
(3)C、D、F的简单离子半径由大到小的顺序为(用离子符号表示)
(4)根据“对角线规则”,铍(Be)的性质与上述六种元素中的
(5)A、C、D可形成多种二元化合物。下列说法不正确的是___________(填字母)。
| A.A2C2和D2C2中都含共价键 |
| B.A、D可形成离子化合物 |
C.D2C、D2C2中阴阳离子个数比均为 |
| D.D2C和D2C2均能溶于A2C,并发生化合反应 |
①F的最高价氧化物水化物比次氯酸稳定
②高氯酸的酸性比F的最高价氧化物的水化物的酸性强
③F的简单阴离子比Cl—易被氧化
④HCl比F的氢化物稳定
⑤铜与盐酸不反应,但能与F的最高价氧化物的水化物的浓溶液反应
⑥铁与氯气在加热条件下反应生成氯化铁,铁与F单质在加热条件下反应生成某化亚铁
| A.全部 | B.②③④⑥ | C.①②④⑤⑥ | D.②③④⑤⑥ |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】已知A、E为金属单质,B是淡黄色粉末且常用于防毒面具中,注:部分反应条件和产物省略 ,回答下题。
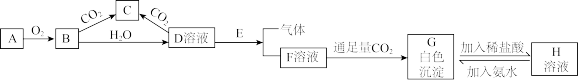
(1)实验室中 常常保存在盛放
常常保存在盛放_______ 的广口瓶, 焰色反应为
焰色反应为_______ 色。
(2)写出 转变成
转变成 的化学方程式
的化学方程式_______ 。该反应中氧化剂是_______ ,还原剂是_______ ,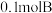 参与该反应,转移电子的个数为
参与该反应,转移电子的个数为_______ 。
(3)写出D溶液与E反应生成F和气体的化学方程式:_______ 。
(4)F→G的离子方程式_______ 。
(5)H→G的离子方程式_______ 。

(1)实验室中
 常常保存在盛放
常常保存在盛放 焰色反应为
焰色反应为(2)写出
 转变成
转变成 的化学方程式
的化学方程式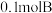 参与该反应,转移电子的个数为
参与该反应,转移电子的个数为(3)写出D溶液与E反应生成F和气体的化学方程式:
(4)F→G的离子方程式
(5)H→G的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】氮化铝(AlN)是一种新型无机非金属材料。某AlN样品仅含有Al2O3杂质,为测定AlN的含量,设计如下三种实验方案(已知:AlN+NaOH+H2O===NaAlO2+NH3↑)。
【方案1】取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。

(1)上图C装置中球形干燥管的作用是_________ 。
(2)完成以下实验步骤:组装好实验装置,首先检查气密性,再加入实验药品,接下来的实验操作是______________________ ,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,通入氮气一段时间,测定C装置反应前后的质量变化。通入氮气的目的是______________________ 。
(3)由于装置存在缺陷,导致测定结果偏高,请提出改进意见:_________________________ 。
【方案2】用下图装置测定m g样品中AlN的纯度(部分夹持装置已略去)。

(4)为测定生成气体的体积,量气装置中的X液体可以是__________ 。
A.CCl4 B.H2O C.NH4Cl溶液 D.苯
【方案3】按以下步骤测定样品中AlN的纯度:

(5)步骤②生成沉淀的离子方程式为__________________________________________ 。
【方案1】取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。

(1)上图C装置中球形干燥管的作用是
(2)完成以下实验步骤:组装好实验装置,首先检查气密性,再加入实验药品,接下来的实验操作是
(3)由于装置存在缺陷,导致测定结果偏高,请提出改进意见:
【方案2】用下图装置测定m g样品中AlN的纯度(部分夹持装置已略去)。

(4)为测定生成气体的体积,量气装置中的X液体可以是
A.CCl4 B.H2O C.NH4Cl溶液 D.苯
【方案3】按以下步骤测定样品中AlN的纯度:

(5)步骤②生成沉淀的离子方程式为
您最近一年使用:0次

 有关的问题。
有关的问题。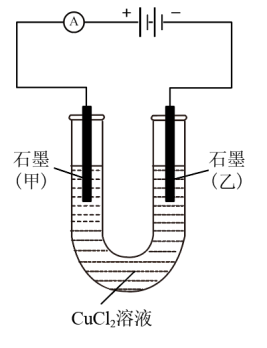
 溶液的
溶液的
 ”或“
”或“ ”或“
”或“ ”)。
”)。

