已知: 易溶于水,
易溶于水, 微溶于水。以含锂的电解铝废渣(主要含
微溶于水。以含锂的电解铝废渣(主要含 、
、 、
、 、
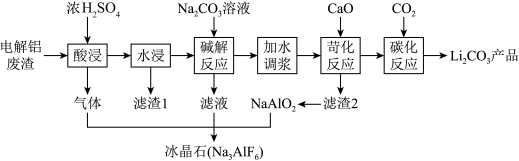
、 )和浓硫酸为原料,制备电池级碳酸锂,同时得到副产品冰晶石的工艺流程如图,下列有关说法不正确的是
)和浓硫酸为原料,制备电池级碳酸锂,同时得到副产品冰晶石的工艺流程如图,下列有关说法不正确的是
 易溶于水,
易溶于水, 微溶于水。以含锂的电解铝废渣(主要含
微溶于水。以含锂的电解铝废渣(主要含 、
、 、
、 、
、 )和浓硫酸为原料,制备电池级碳酸锂,同时得到副产品冰晶石的工艺流程如图,下列有关说法不正确的是
)和浓硫酸为原料,制备电池级碳酸锂,同时得到副产品冰晶石的工艺流程如图,下列有关说法不正确的是
A.第一步酸浸时产生气体的化学式为 |
B.滤渣1的成分为 |
C.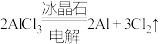 |
D.碳化反应后的溶液得到 的具体实验操作是蒸发浓缩,冷却结晶,过滤,洗涤,干燥 的具体实验操作是蒸发浓缩,冷却结晶,过滤,洗涤,干燥 |
更新时间:2023-08-23 16:51:35
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列解释事实的方程式正确的是
| A.氢氧化亚铁暴露于空气中变色:Fe(OH)2+O2+H2O=Fe(OH)3 |
B.用Na2SO3溶液吸收少量Cl2:3S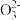 +Cl2+H2O=2HS +Cl2+H2O=2HS +2Cl-+S +2Cl-+S |
C.同浓度、同体积的NH4HSO4溶液与NaOH溶液混合:N +OH-=NH3·H2O +OH-=NH3·H2O |
D.Zn溶于过量的浓硝酸中:3Zn+8H++2N =3Zn2++2NO↑+4H2O =3Zn2++2NO↑+4H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】氨氮废水是造成河流湖泊富营养化的主要原因,处理氨氮废水(主要以 和NH3·H2O的形式存在)的主要流程如图所示:
和NH3·H2O的形式存在)的主要流程如图所示:

下列说法不正确的是
 和NH3·H2O的形式存在)的主要流程如图所示:
和NH3·H2O的形式存在)的主要流程如图所示:
下列说法不正确的是
| A.过程I降低氮元素浓度的方法:加入NaOH溶液,调节pH为碱性,升高温度,再通入空气,赶出氨气 |
B.过程II是在碱性条件下通入氧气实现: → → → → 转化, 转化, 被氧气氧微生物化为 被氧气氧微生物化为 ,总反应的离子方程式: ,总反应的离子方程式: +2O2 +2O2   +H2O+2H+ +H2O+2H+ |
C.过程III中甲醇的作用是作还原剂,将 还原为N2 还原为N2 |
D.过程III的转化过程为 → → →N2,每生成1molN2转移10mol电子 →N2,每生成1molN2转移10mol电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列有关浓硫酸与浓硝酸的叙述,不正确的是
| A.露置在空气中,前者质量增加,后者质量减小 |
| B.常温下,两者均能使铁、铝钝化 |
| C.一定条件下,两者均能与铜反应 |
| D.两者都具有强氧化性,均能氧化SO2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某化学兴趣小组为探究酸性高锰酸钾与铜的反应,设计实验如下,在培养皿中加入足量的酸性高锰酸钾溶液,放入铜珠,实验结果如下,下列说法正确的是
已知:Cu+在酸性溶液中不能稳定存在:2Cu+ = Cu + Cu2+
2 + 3Mn2+ + 2H2O = 5MnO2 ↓+4H+
+ 3Mn2+ + 2H2O = 5MnO2 ↓+4H+
实验 | 现象 |
 | 一段时间后,培养皿中由铜珠向外侧依次呈现: I区澄清且紫色褪色明显 Ⅱ区底部覆盖棕黑色固体 Ⅲ区澄清且紫色变浅 |
2
 + 3Mn2+ + 2H2O = 5MnO2 ↓+4H+
+ 3Mn2+ + 2H2O = 5MnO2 ↓+4H+| A.I区铜反应后的主要产物是Cu2+,不可能是Cu+ |
| B.Ⅱ区棕黑色固体是MnO2,由铜和酸性高锰酸钾溶液反应产生 |
C.Ⅲ区紫色变浅说明在Ⅲ区 也发生了氧化还原反应 也发生了氧化还原反应 |
| D.如果酸性高锰酸钾溶液量少,所有反应完全后,产物中没有Mn2+ |
您最近一年使用:0次
【推荐1】除去下列物质中的杂质(括号内为杂质),所选用试剂及操作方法不正确的是
| 选项 | 待提纯的物质 | 选用的试剂 | 操作方法 |
| A | Fe(OH)3[Fe(OH)2] | 氧气 | 在空气中灼烧 |
| B | NaCl(Na2CO3) | 稀盐酸 | 加入过量的稀盐酸,蒸发结晶 |
| C | 铁粉(铝粉) | NaOH溶液 | 加入过量NaOH溶液并过滤、洗涤、干燥 |
| D | FeCl2溶液(FeCl3) | 铁粉 | 加入过量铁粉后过滤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】以电石渣[主要成分为 Ca(OH)2和 CaCO3]为原料制备 KClO3的流程如下:

下列说法正确的是

下列说法正确的是
| A.打浆步骤,将电石渣配制成溶液 |
| B.氯化步骤,发生的主要反应 2Ca(OH)2+2Cl2=Ca(ClO)2+CaCl2+2H2O |
| C.转化步骤,发生复分解反应,将所得溶液蒸发结晶过滤得 KClO3晶体 |
| D.KClO3晶体中可能混有 KCl、KClO 等杂质 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】工业上应用两矿法浸出软锰矿(主要成分 )和方铅矿(主要成分
)和方铅矿(主要成分 、
、 )制备
)制备 和
和 的转化流程如图:
的转化流程如图:

已知: 微溶于水,溶液中存在可逆反应:
微溶于水,溶液中存在可逆反应: 。下列说法错误的是
。下列说法错误的是
 )和方铅矿(主要成分
)和方铅矿(主要成分 、
、 )制备
)制备 和
和 的转化流程如图:
的转化流程如图:
已知:
 微溶于水,溶液中存在可逆反应:
微溶于水,溶液中存在可逆反应: 。下列说法错误的是
。下列说法错误的是A.Ⅰ中 的作用是提供大量 的作用是提供大量 |
B.Ⅱ中生成的沉淀 是 是 |
| C.Ⅳ中试剂X可能作氧化剂 |
D.Ⅴ中发生反应: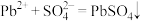 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】关于物质转化规律“单质 (酸性或碱性)氧化物
(酸性或碱性)氧化物 酸或碱→盐”说法正确的是
酸或碱→盐”说法正确的是
 (酸性或碱性)氧化物
(酸性或碱性)氧化物 酸或碱→盐”说法正确的是
酸或碱→盐”说法正确的是| A.若单质为碳,氧化物可以为CO |
B.“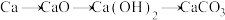 ”符合该转化规律 ”符合该转化规律 |
| C.若钠元素可实现转化,则碱为Na2CO3 |
| D.单质H2能实现上述物质间的转化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】某电解精炼铜的阳极泥(含Cu2Te)经预处理后主要含有TeO2和少量Ag、Au,以此预处理阳极泥为原料制备单质碲的一种工艺流程如图:
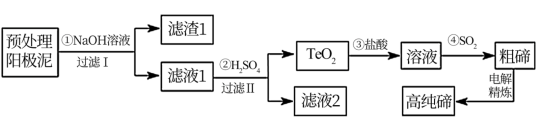
已知:TeO2是两性氧化物,微溶于水,易溶于较浓的强酸和强碱分别生成Te4+和TeO 。下列说法不正确的是
。下列说法不正确的是

已知:TeO2是两性氧化物,微溶于水,易溶于较浓的强酸和强碱分别生成Te4+和TeO
 。下列说法不正确的是
。下列说法不正确的是| A.Cu2Te中Te的化合价为−2 |
| B.阳极泥预处理时发生反应:Cu2Te+O2→CuO+TeO2,该反应中氧化剂与还原剂的物质的量之比为1:2 |
C.步骤④发生反应的离子方程式是Te4++2SO2+4H2O=Te↓+2SO +8H+ +8H+ |
| D.要从滤渣1中分离出Au,可以向滤渣1中稀硝酸 |
您最近一年使用:0次

 N2O4(g) △H>0
N2O4(g) △H>0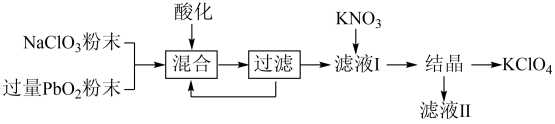
 +2H+=Pb2++
+2H+=Pb2++ +H2O
+H2O

