生活中处处有化学。请回答下列问题:
(1)苏打水是很多人喜爱的饮品,请写出小苏打在水中的电离方程式_______ 。
(2)“84消毒液”与洁厕灵(主要成分是浓盐酸)不能混用,混合会产生黄绿色的有毒气体,请用离子方程式解释原因_______ 。
(3)Na2O2常用作呼吸面罩供氧剂,请写出Na2O2的电子式_______ 。
(4)硅是太阳能电池板的主要原材料,请写出硅元素在周期表的位置_______ 。
(5)4gCO在氧气中燃烧生成CO2,放出9.6kJ热量,写出CO燃烧的热化学方程式_______ 。
(6)已知:①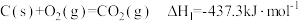
②H2(g)+1/2O2(g)=H2O(g) ∆H2=-285.8kJ·mol-1
③CO(g)+1/2O2(g)=CO2(g) ∆H3=-283.0kJ·mol-1
写出煤气化(碳和水蒸气反应生成一氧化碳和氢气)的热化学方程式_______ 。
(1)苏打水是很多人喜爱的饮品,请写出小苏打在水中的电离方程式
(2)“84消毒液”与洁厕灵(主要成分是浓盐酸)不能混用,混合会产生黄绿色的有毒气体,请用离子方程式解释原因
(3)Na2O2常用作呼吸面罩供氧剂,请写出Na2O2的电子式
(4)硅是太阳能电池板的主要原材料,请写出硅元素在周期表的位置
(5)4gCO在氧气中燃烧生成CO2,放出9.6kJ热量,写出CO燃烧的热化学方程式
(6)已知:①
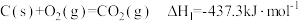
②H2(g)+1/2O2(g)=H2O(g) ∆H2=-285.8kJ·mol-1
③CO(g)+1/2O2(g)=CO2(g) ∆H3=-283.0kJ·mol-1
写出煤气化(碳和水蒸气反应生成一氧化碳和氢气)的热化学方程式
更新时间:2023-08-29 15:08:22
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】按要求回答下列问题:
(1)①铜 ②烧碱 ③大理石 ④氯化钠晶体 ⑤盐酸 ⑥氨气 ⑦蔗糖 ⑧二氧化碳 ⑨液态氯化氢 ⑩澄清石灰水。上述物质中能导电的是_______ ,属于电解质的是_______ ,属于非电解质的是_______ (填编号)
(2)按要求写出下列方程式:
①NaHCO3电离的电离方程式:_______ 。
②碳酸钙与盐酸反应的离子有程式:_______ 。
(1)①铜 ②烧碱 ③大理石 ④氯化钠晶体 ⑤盐酸 ⑥氨气 ⑦蔗糖 ⑧二氧化碳 ⑨液态氯化氢 ⑩澄清石灰水。上述物质中能导电的是
(2)按要求写出下列方程式:
①NaHCO3电离的电离方程式:
②碳酸钙与盐酸反应的离子有程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下面是同学们熟悉的物质:
①O2 ②干冰 ③NaBr ④H2SO4 ⑤Na2CO3⑥NH4Cl ⑦NaHSO4 ⑧Ne ⑨Na2O2 ⑩NaOH
(1)这些物质中,只含有共价键的是_______ ;只含有离子键的是_______ ;既含有共价键又含有离子键的是_______ ;不存在化学键的是_______ ;电解质有_______ ;非电解质有_______ (填编号)
(2)NaHSO4在熔融状态下电离,破坏的化学键是_______ ,写出其电离方程式_______ 。
(3)写出②与⑨发生反应的化学方程式:_______ 。
(4)写出在稀溶液中⑥和⑩反应的离子方程式:_______ 。
①O2 ②干冰 ③NaBr ④H2SO4 ⑤Na2CO3⑥NH4Cl ⑦NaHSO4 ⑧Ne ⑨Na2O2 ⑩NaOH
(1)这些物质中,只含有共价键的是
(2)NaHSO4在熔融状态下电离,破坏的化学键是
(3)写出②与⑨发生反应的化学方程式:
(4)写出在稀溶液中⑥和⑩反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】用电弧法合成碳纳米管,常伴有大量杂质_______碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其反应方程式为: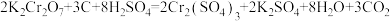
(1)用双线桥法表示出电子转移的方向和数目_______ 。
(2)此反应的氧化产物为_______ 。
(3)根据该反应判断还原性的强弱:C_______  (填“强于”或“弱于”)。
(填“强于”或“弱于”)。
(4)若产生1个 分子,该反应转移电子的个数为
分子,该反应转移电子的个数为_______ 。
(5)写出 在水溶液中的电离方程式:
在水溶液中的电离方程式:_______ 。
(6)配平下列化学反应方程式,并用单线桥法表示反应中电子转移的方向和数目_______ 。(已知该反应中 只发生如下变化过程:
只发生如下变化过程: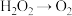 。)
。)
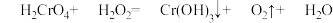
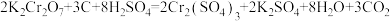
(1)用双线桥法表示出电子转移的方向和数目
(2)此反应的氧化产物为
(3)根据该反应判断还原性的强弱:C
 (填“强于”或“弱于”)。
(填“强于”或“弱于”)。(4)若产生1个
 分子,该反应转移电子的个数为
分子,该反应转移电子的个数为(5)写出
 在水溶液中的电离方程式:
在水溶液中的电离方程式:(6)配平下列化学反应方程式,并用单线桥法表示反应中电子转移的方向和数目
 只发生如下变化过程:
只发生如下变化过程: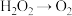 。)
。)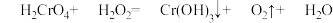
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ:分类法是一种重要的学习方法,有四种物质类别不同转化关系满足下图,“→”代表前者经历一次反应可以直接生成后者:
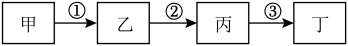
(1)甲若为金属单质_______ ,则乙_______ ,丙_______ ,丁_______ (填化学式)。
(2)甲若为非金属单质_______ ,则乙_______ ,丙_______ ,丁_______ (填化学式)。
Ⅱ:分类方法应用比较广泛,属于同一类的物质具有相似性。如:
(3) 、
、 、
、 、
、 都属于酸性氧化物,由
都属于酸性氧化物,由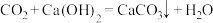 ,可得出
,可得出 与氢氧化钠反应的化学方程为
与氢氧化钠反应的化学方程为_______ 。
(4) 、
、 、
、 都属于弱酸的酸式盐,
都属于弱酸的酸式盐, 及
及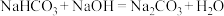 ,完成
,完成 与
与 反应的化学方程式
反应的化学方程式_______ 、写出澄清石灰水与过量 溶液反应的离子方程式
溶液反应的离子方程式_______ 。

(1)甲若为金属单质
(2)甲若为非金属单质
Ⅱ:分类方法应用比较广泛,属于同一类的物质具有相似性。如:
(3)
 、
、 、
、 、
、 都属于酸性氧化物,由
都属于酸性氧化物,由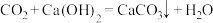 ,可得出
,可得出 与氢氧化钠反应的化学方程为
与氢氧化钠反应的化学方程为(4)
 、
、 、
、 都属于弱酸的酸式盐,
都属于弱酸的酸式盐, 及
及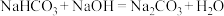 ,完成
,完成 与
与 反应的化学方程式
反应的化学方程式 溶液反应的离子方程式
溶液反应的离子方程式
您最近一年使用:0次
【推荐2】Ⅰ.2022年9月20日是第34个“全国爱牙日”。今年的主题是“口腔健康、全身健康”。为了防止龋齿,正确的刷牙方式和选用适宜的牙膏很重要。

(1)牙膏中的摩擦剂碳酸钙可以用石灰石来制备。某同学设计了一种实验室制备碳酸钙的实验方案,其流程图如下:

请写出上述方案中反应③的离子方程式:_______ 。
(2)请你仍用石灰石作为原料,选择适当的试剂,设计实验室制备碳酸钙的另一种实验方案。依照第(1)题中所示,将你的实验方案用流程图表示出来。________
(可供选择的试剂:稀硫酸、稀盐酸、Na2CO3溶液、Na2SO4溶液、CO2)

你设计的方案的优点为_______ 。(答出两条)
Ⅱ.高铁酸钠(Na2FeO4)是一种新型的净水剂,可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O
(3)该反应中氧化剂是_______ (填化学式,下同),在反应中_______ (填“得到”或“失去”)电子;还原剂是_______ ,_______ 元素被氧化,还原产物为_______ 。
(4)在化学方程式上方用单线桥标出电子转移的方向和数目:______
2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O
(5)当反应中有1个 离子生成时,转移的电子数是
离子生成时,转移的电子数是_______ 个。

(1)牙膏中的摩擦剂碳酸钙可以用石灰石来制备。某同学设计了一种实验室制备碳酸钙的实验方案,其流程图如下:

请写出上述方案中反应③的离子方程式:
(2)请你仍用石灰石作为原料,选择适当的试剂,设计实验室制备碳酸钙的另一种实验方案。依照第(1)题中所示,将你的实验方案用流程图表示出来。
(可供选择的试剂:稀硫酸、稀盐酸、Na2CO3溶液、Na2SO4溶液、CO2)

你设计的方案的优点为
Ⅱ.高铁酸钠(Na2FeO4)是一种新型的净水剂,可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O
(3)该反应中氧化剂是
(4)在化学方程式上方用单线桥标出电子转移的方向和数目:
2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O
(5)当反应中有1个
 离子生成时,转移的电子数是
离子生成时,转移的电子数是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.完成以下填空:
(1)现有:①固体 ②稀硫酸③氨气④熔融
②稀硫酸③氨气④熔融 ⑤蔗糖⑥铜;其中能导电的是
⑤蔗糖⑥铜;其中能导电的是___________ (填序号,下同);属于电解质的是___________ 。
(2)配制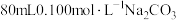 溶液,需要
溶液,需要 晶体的质量为
晶体的质量为___________ 。
II.酸式盐是盐的一种,可看作是多元酸中的氢离子未被完全中和所得到的盐,常见的有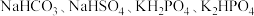 等。已知
等。已知 (次磷酸)与足量的
(次磷酸)与足量的 反应只生成一种盐
反应只生成一种盐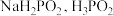 水溶液中存在
水溶液中存在 分子。
分子。
(3) 属于
属于___________ 酸; 为
为___________ 盐(填序号)。
①一元酸,②二元酸,③三元酸,④强酸,⑤弱酸,⑥正盐,⑦酸式盐
(4)写出 溶液与足量
溶液与足量 溶液反应的离子方程式
溶液反应的离子方程式___________ 。
(1)现有:①固体
 ②稀硫酸③氨气④熔融
②稀硫酸③氨气④熔融 ⑤蔗糖⑥铜;其中能导电的是
⑤蔗糖⑥铜;其中能导电的是(2)配制
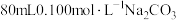 溶液,需要
溶液,需要 晶体的质量为
晶体的质量为II.酸式盐是盐的一种,可看作是多元酸中的氢离子未被完全中和所得到的盐,常见的有
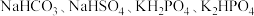 等。已知
等。已知 (次磷酸)与足量的
(次磷酸)与足量的 反应只生成一种盐
反应只生成一种盐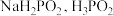 水溶液中存在
水溶液中存在 分子。
分子。(3)
 属于
属于 为
为①一元酸,②二元酸,③三元酸,④强酸,⑤弱酸,⑥正盐,⑦酸式盐
(4)写出
 溶液与足量
溶液与足量 溶液反应的离子方程式
溶液反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】在化学科学研究中,物质发生化学反应的反应热可通过实验测定,也可通过化学计算的方式间接获得。
(1)实验方法测定反应热
①中和反应反应热的测定:用50mL0.50mol/L的盐酸与50mL0.55mol/L的NaOH溶液进行中和反应。实验中所需要使用的仪器除量热计、量筒外,还需要的玻璃仪器有_______ 。为了减少实验误差,实验过程中应将NaOH溶液_______ (填“一次性”或“分多次”)倒入盛有盐酸的量热计内筒中;溶液混合后,准确读取混合溶液的_______ ,记为终止温度。若量取盐酸溶液时俯视读数,会造成中和热数值_______ (填“偏大”或“偏小”)
②实验测得在一定温度下,0.2molCH4(g)与足量H2O(g)完全反应生成CO2(g)和H2(g)吸收33kJ的热量,该反应的热化学方程式为_______ 。
(2)通过化学计算间接获得反应热
①已知断裂1molH—H键、I—I键、H—I键需要吸收的能量分别为436kJ、153kJ、299kJ。则反应H2(g)+I2(g)=2HI(g)的△H=_______ kJ·mol-1。
②已知:CO(g)+2H2(g)=CH3OH(g) △H1=-90.8kJ·mol-1;
2H2(g)+O2(g)=2H2O(l) △H2=-571.6kJ·mol-1;
H2(g)+ O2(g)=H2O(g) △H3=-241.8kJ·mol-1。
O2(g)=H2O(g) △H3=-241.8kJ·mol-1。
CH3OH(g)+O2(g)=CO(g)+2H2O(g) △H=_______ kJ·mol-1。
(1)实验方法测定反应热
①中和反应反应热的测定:用50mL0.50mol/L的盐酸与50mL0.55mol/L的NaOH溶液进行中和反应。实验中所需要使用的仪器除量热计、量筒外,还需要的玻璃仪器有
②实验测得在一定温度下,0.2molCH4(g)与足量H2O(g)完全反应生成CO2(g)和H2(g)吸收33kJ的热量,该反应的热化学方程式为
(2)通过化学计算间接获得反应热
①已知断裂1molH—H键、I—I键、H—I键需要吸收的能量分别为436kJ、153kJ、299kJ。则反应H2(g)+I2(g)=2HI(g)的△H=
②已知:CO(g)+2H2(g)=CH3OH(g) △H1=-90.8kJ·mol-1;
2H2(g)+O2(g)=2H2O(l) △H2=-571.6kJ·mol-1;
H2(g)+
 O2(g)=H2O(g) △H3=-241.8kJ·mol-1。
O2(g)=H2O(g) △H3=-241.8kJ·mol-1。CH3OH(g)+O2(g)=CO(g)+2H2O(g) △H=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】雾霾天气多次肆虐我国中东部地区。其中,汽车尾气和燃煤尾气是造成空气污染的原因之一。
(1)汽车尾气净化的主要原理为2NO(g)+2CO(g) 2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如下图所示。
2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如下图所示。
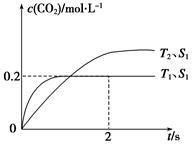
据此判断:
①该反应的ΔH__________ 0(填“>”或“<”),ΔS__________ 0(填“>”或“<”)
②在T1温度下,0~2 s内的平均反应速率v(N2)=____________________ 。
③当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若增大催化剂的表面积,则CO转化率__________ (填“增大”,“减少”或“不变”)
④若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是________________ (填字母)。
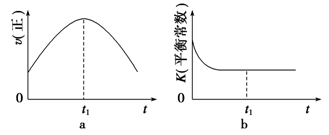
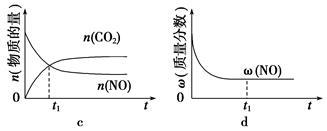
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题。
①煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
例如:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)ΔH=-867.0 kJ·mol-1
2NO2(g) N2O4(g)ΔH=-56.9 kJ·mol-1
N2O4(g)ΔH=-56.9 kJ·mol-1
写出CH4催化还原N2O4(g)生成N2和H2O(g)的热化学方程式_________________ 。
②将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。下图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。电极a、b表面发生的电极反应式分别为
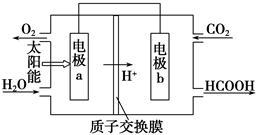
a:_________________________________________ ;
b:_________________________________________ 。
(1)汽车尾气净化的主要原理为2NO(g)+2CO(g)
 2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如下图所示。
2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如下图所示。
据此判断:
①该反应的ΔH
②在T1温度下,0~2 s内的平均反应速率v(N2)=
③当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若增大催化剂的表面积,则CO转化率
④若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是


(2)直接排放煤燃烧产生的烟气会引起严重的环境问题。
①煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
例如:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)ΔH=-867.0 kJ·mol-1
2NO2(g)
 N2O4(g)ΔH=-56.9 kJ·mol-1
N2O4(g)ΔH=-56.9 kJ·mol-1写出CH4催化还原N2O4(g)生成N2和H2O(g)的热化学方程式
②将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。下图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。电极a、b表面发生的电极反应式分别为

a:
b:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】甲醇( )是一种重要的化工原料,广泛应用于化工生产,也可以直接用作燃料。已知:
)是一种重要的化工原料,广泛应用于化工生产,也可以直接用作燃料。已知:

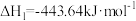

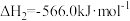
(1)试写出 在氧气中完全燃烧生成
在氧气中完全燃烧生成 和
和 的热化学方程式:
的热化学方程式:_______ 。
(2)科研人员研发出一种由强碱溶液作电解质溶液的新型甲醇手机电池,充满电后手机可连续使用一个月,则放电时,甲醇在_______ (填“正”或“负”)极发生反应。
(3)某同学设计了一种用电解法制取 的实验装置(如图所示),通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法错误的是
的实验装置(如图所示),通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法错误的是_______ (填序号)。
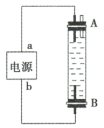
A.a为电源正极,b为电源负极 B.可以用NaCl溶液作为电解质溶液
C.A、B两端都必须用铁作电极 D.A极发生的反应为
 )是一种重要的化工原料,广泛应用于化工生产,也可以直接用作燃料。已知:
)是一种重要的化工原料,广泛应用于化工生产,也可以直接用作燃料。已知:
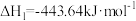

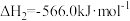
(1)试写出
 在氧气中完全燃烧生成
在氧气中完全燃烧生成 和
和 的热化学方程式:
的热化学方程式:(2)科研人员研发出一种由强碱溶液作电解质溶液的新型甲醇手机电池,充满电后手机可连续使用一个月,则放电时,甲醇在
(3)某同学设计了一种用电解法制取
 的实验装置(如图所示),通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法错误的是
的实验装置(如图所示),通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法错误的是
A.a为电源正极,b为电源负极 B.可以用NaCl溶液作为电解质溶液
C.A、B两端都必须用铁作电极 D.A极发生的反应为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】联合国大会将 2019年定为“化学元素周期表国际年”,高度体现了元素周期表的重要性。下表显示了元素周期表中短周期的一部分,①~⑦代表七种短周期元素。
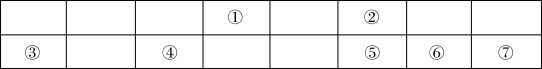
(1)七种元素中化学性质最不活泼的是_______ (填元素符号),形成化合物数目最多的元素是_______ (填元素符号)。
(2)元素②的最低价阴离子的离子结构示意图是_______ 。
(3)②、⑤两种元素的最简单氢化物中稳定性较强的是_______ (填化学式)。
(4)⑤、⑥两种元素的最高价氧化物对应的水化物中,酸性较弱的是_______ (填化学式)。
(5)元素③的最高价氧化物对应水化物与元素④的单质反应的离子方程式为_______ 。
(6)用电子式表示元素③和元素⑥形成化合物的过程_______ 。

(1)七种元素中化学性质最不活泼的是
(2)元素②的最低价阴离子的离子结构示意图是
(3)②、⑤两种元素的最简单氢化物中稳定性较强的是
(4)⑤、⑥两种元素的最高价氧化物对应的水化物中,酸性较弱的是
(5)元素③的最高价氧化物对应水化物与元素④的单质反应的离子方程式为
(6)用电子式表示元素③和元素⑥形成化合物的过程
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据要求填空(所涉及元素均为前20号)
(1)A元素的原子M层有5个电子,则其原子结构示意图为__________________ ;最高价氯化物的化学式_______________________ 。
(2)C元素原子最外层电子是最内层电子的3倍,其形成的离子与Ar元素有相同的电子结构,请写出C离子的结构示意图和电子式:________________ 、_________ 。
(3)标出下列反应的电子转移方向和数目,并填写有关内容:
KClO3+6HCl→3Cl2↑+3H2O+KCl、___________
氧化剂______________ ;氧化产物______________ ;还原剂______________ ;还原产物______________ ;被氧化的元素______________ ;HCl的作用______________ .
(1)A元素的原子M层有5个电子,则其原子结构示意图为
(2)C元素原子最外层电子是最内层电子的3倍,其形成的离子与Ar元素有相同的电子结构,请写出C离子的结构示意图和电子式:
(3)标出下列反应的电子转移方向和数目,并填写有关内容:
KClO3+6HCl→3Cl2↑+3H2O+KCl、
氧化剂
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下表为元素周期表的一部分,请参照元素①—⑩在表中的位置,用相应的化学用语 回答下列问题;
(1)表中⑩号元素有一种含20个中子的核素,请写出其原子符号_______ 。
(2)④、⑦、⑩的离子半径由大到小的顺序为_______ (用元素符号作答)。
(3)由表中④、⑥元素可以组成一种淡黄色的固体物质,画出该物质的电子式____ ,该物质含有的化学键类型有_____ 。
(4)元素⑩的一种含氧酸是常用的漂白性物质,这种含氧酸的结构式为____ ,元素⑤和⑩的氢化物中,酸性更强的是_____ 。
(5)上述10种元素中的两种能形成一种四核10电子分子,请用电子式表示其形成过程____ 。
| ① | |||||||
| ② | ③ | ④ | ⑤ | ||||
| ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)表中⑩号元素有一种含20个中子的核素,请写出其原子符号
(2)④、⑦、⑩的离子半径由大到小的顺序为
(3)由表中④、⑥元素可以组成一种淡黄色的固体物质,画出该物质的电子式
(4)元素⑩的一种含氧酸是常用的漂白性物质,这种含氧酸的结构式为
(5)上述10种元素中的两种能形成一种四核10电子分子,请用电子式表示其形成过程
您最近一年使用:0次



