中国承诺2030年前, 的排放不再增长,达到峰值之后逐步降低。其中由
的排放不再增长,达到峰值之后逐步降低。其中由 和
和 制备合成气(CO、
制备合成气(CO、 ),再由合成气制备
),再由合成气制备 的反应转化关系如图所示。设
的反应转化关系如图所示。设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 的排放不再增长,达到峰值之后逐步降低。其中由
的排放不再增长,达到峰值之后逐步降低。其中由 和
和 制备合成气(CO、
制备合成气(CO、 ),再由合成气制备
),再由合成气制备 的反应转化关系如图所示。设
的反应转化关系如图所示。设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
A.标准状况下,11.2 L 所含的极性键为 所含的极性键为 |
B.等物质的量的 和 和 , , 的质子数比 的质子数比 多 多 |
C.制备合成气的反应中,若生成1 mol CO,理论上反应Ⅰ和Ⅱ共转移电子数为 |
D.反应Ⅲ的化学方程式为 ,原子利用率为100%,符合绿色化学理念 ,原子利用率为100%,符合绿色化学理念 |
更新时间:2023-08-31 16:36:36
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】NA表示阿伏加德罗常数的值,下列说法中正确的是
| A.0.1molNaHSO4固体所含的离子总数为0.3NA |
B.0.1mol/L硫酸溶液中含NA个 |
| C.标准状况下将22.4LNH3溶于1L水配成1mol/L的氨水溶液 |
| D.100g的46%C2H5OH水溶液中含4mol氧原子 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】用NA表示阿伏加 德罗常数,下列叙述正确的是( )
| A.22.4L CO2含有NA个分子 |
| B.常温常压下,0.1mol Na2CO3含有的Na+数目为0.1NA |
| C.常温常压下,18gH2O含有的氢原子数为2NA |
| D.物质的量浓度为0.5mol·L-1的MgCl2溶液中,含有Cl-个数为NA |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.常温常压下,28g乙烯和丙烯的混合气体中含有原子的数目为 |
B.标准状况下,11.2L二氯甲烷所含分子数为 |
C.常温常压下,1.7g羟基(-OH)所含电子的数目为 |
D.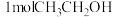 分子中含有的共价键数目为 分子中含有的共价键数目为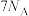 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】科学家发现金星大气中存在 ,据此推断金星大气层或存在生命。利用下列反应可制备
,据此推断金星大气层或存在生命。利用下列反应可制备 :
: 。下列说法正确的是
。下列说法正确的是
 ,据此推断金星大气层或存在生命。利用下列反应可制备
,据此推断金星大气层或存在生命。利用下列反应可制备 :
: 。下列说法正确的是
。下列说法正确的是A. 中化学键为非极性键 中化学键为非极性键 |
B.中子数为10的氧原子可表示为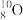 |
C.每1mol 参加反应理论上可生成22.4L 参加反应理论上可生成22.4L |
D.每消耗12.4g的 ,则过程中转移电子数为0.3NA ,则过程中转移电子数为0.3NA |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】将1.92g铜粉投入足量稀硝酸中,发生反应:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,反应结束后加水将溶液稀释至200mL。下列说法中正确的是
| A.生成还原产物Cu(NO3)2物质的量为0.03mol |
| B.被还原的HNO3物质的量为0.08mol |
| C.反应生成448mLNO气体 |
| D.反应中转移电子数目约为3.612×1022 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.常温常压下,15g甲基含有的电子数目为 |
B.标准状况下, 含有的分子数目为 含有的分子数目为 |
C.常温下,12g金刚石中含有的共价键数目为 |
D.标准状况下, 与水反应,转移电子的数目为 与水反应,转移电子的数目为 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】NA表示阿伏加德罗常数,下列说法正确的是
| A.氟气与水反应生成1molO2共转移2NA个电子 |
| B.标准状况下NA个O2分子的质量与22.4LSO2气体的质量大致相等 |
| C.含NA个负电荷的RO32-离子的质量为40g,则R的摩尔质量为32g·mol–1 |
| D.25℃时,pH=13的烧碱溶液中约含NA个氢氧根(OH-)离子 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】“中国名片”、“中国制造”发展在众多领域受到世界瞩目,它们与化学有着密切联系。下列说法不正确的是
A.新型核潜艇“长征18”可以在海底潜伏数月之久,运用 作供氧剂 作供氧剂 |
| B.港珠澳大桥桥梁采用先进的抗腐蚀方法,钢铁桥梁被腐蚀是氧化还原反应 |
| C.成都大运会开幕式上灿烂绽放的烟花利用了焰色试验的原理,是化学变化 |
| D.冬奥会采用氢燃料电池车,开发光伏发电系统等措施有利于实现“碳中和” |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】化学与生活、生产、环境密切相关,下列有关说法错误的是
| A.K2FeO4和明矾都可做水处理剂,工作(净水)原理完全相同 |
| B.氢能是一种新型能源,具有热值高、资源丰富、无毒、无污染的优点 |
| C.植树造林、节能减排是实现碳中和的途径之一 |
| D.反应SO2(g)+2H2S(g)=3S(s)+2H2O(l)在常温下能自发进行,则该反应的∆H<0 |
您最近一年使用:0次



