近年我国某些城市酸雨污染较为严重,主要是因为大量燃烧含硫量高的煤。
【实验目的】通过实验证明煤中含有碳元素和硫元素。
(1)查阅资料知,二氧化硫能使酸性高锰酸钾溶液褪色,该反应体现出SO2的___________ 性;
(2)根据上述资料,甲同学和丙同学分别设计实验方案进行探究。
【实验操作】甲同学进行了如图所示A、B两步实验。
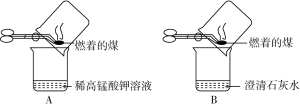
【实验现象】A中稀高锰酸钾溶液褪色,B中澄清石灰水变浑浊。
【得出结论】煤燃烧生成二氧化硫和二氧化碳,证明煤中含有碳元素和硫元素。
①乙同学认为甲同学的方案不合理,其理由是___________ 。
【实验操作】丙同学进行了如图所示实验。
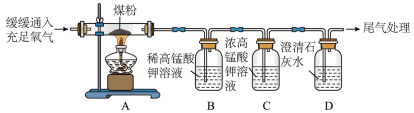
②C装置的作用是___________ ;
③证明煤中含有碳元素和硫元素的现象是___________ 。
④C装置中的浓高锰酸钾溶液也可以替换为___________ (填标号)。
A.足量I2的淀粉溶液 B.足量饱和NaHCO3溶液
C.足量NaHSO3溶液 D.足量溴水
【实验目的】通过实验证明煤中含有碳元素和硫元素。
(1)查阅资料知,二氧化硫能使酸性高锰酸钾溶液褪色,该反应体现出SO2的
(2)根据上述资料,甲同学和丙同学分别设计实验方案进行探究。
【实验操作】甲同学进行了如图所示A、B两步实验。

【实验现象】A中稀高锰酸钾溶液褪色,B中澄清石灰水变浑浊。
【得出结论】煤燃烧生成二氧化硫和二氧化碳,证明煤中含有碳元素和硫元素。
①乙同学认为甲同学的方案不合理,其理由是
【实验操作】丙同学进行了如图所示实验。

②C装置的作用是
③证明煤中含有碳元素和硫元素的现象是
④C装置中的浓高锰酸钾溶液也可以替换为
A.足量I2的淀粉溶液 B.足量饱和NaHCO3溶液
C.足量NaHSO3溶液 D.足量溴水
更新时间:2023-09-05 11:14:03
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】某课外小组设计了下图所示的实验装置(图中固定装置已略去),进行SO2性质的研究。

(1)从物质分类的角度,SO2属于________ (填“酸性”或“碱性”)氧化物。写出硫酸型酸雨形成的反应方程式: _______ ,_____ 。
(2)图中D装置可用来验证SO2具有该性质,其中所加入的试剂是_____ 。
(3)当向该装置通入SO2时,A中紫色石蕊溶液变红,用化学用语解释其原因是______ 。
(4)从元素化合价的角度分析,SO2的性质。
①当向该装置通入SO2一段时间后,可观察C中溶液褪色,MnO4-转化为Mn2+,说明SO2具
有______ 性,反应的离子方程式为 _________ 。
②如验证SO2还具有另一方面的性质,可选择的药品是__________ 。

(1)从物质分类的角度,SO2属于
(2)图中D装置可用来验证SO2具有该性质,其中所加入的试剂是
(3)当向该装置通入SO2时,A中紫色石蕊溶液变红,用化学用语解释其原因是
(4)从元素化合价的角度分析,SO2的性质。
①当向该装置通入SO2一段时间后,可观察C中溶液褪色,MnO4-转化为Mn2+,说明SO2具
有
②如验证SO2还具有另一方面的性质,可选择的药品是
A.过氧化氢 B.浓硫酸 C.氯水 D.硫化钠溶液
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】海水中有丰富的资源,海底有丰富的矿藏、石油、天然气等,海水中还含有大量的电解质,它们电离产生Cl-、Br-、I-、 、Na+、Mg2+、Ca2+等,都是重要资源。开发和利用海水资源是当前科学研究的一项重要任务,如图是某化工厂对海水资源综合利用的示意图:
、Na+、Mg2+、Ca2+等,都是重要资源。开发和利用海水资源是当前科学研究的一项重要任务,如图是某化工厂对海水资源综合利用的示意图:

请根据以上信息回答下列问题:
(1)写出步骤②、⑧分离提纯的方法:②__________ ,⑧__________ 。
(2)步骤⑦分离提纯过程中需要选用的玻璃仪器除烧杯外,还需要的仪器是___________ 。
(3)步骤③的是电解食盐水,工业上称为氯碱工业,D具有杀菌消毒的作用,在喷洒前需要在空气中晾置一会,这样做的原因是___________ 。
(4)初步提纯后的粗盐中含有Mg2+、Ca2+、 等杂质,精制时所用的试剂为①盐酸②氯化钡溶液③氢氧化钠溶液④碳酸钠溶液,下列试剂添加顺序合理的是___________。
等杂质,精制时所用的试剂为①盐酸②氯化钡溶液③氢氧化钠溶液④碳酸钠溶液,下列试剂添加顺序合理的是___________。
(5)流程⑥将溴单质从水溶液中分离出来是利用溴单质具有___________ 性。对粗溴一般做如下处理:

其中步骤Ⅱ、Ⅲ起到的作用是___________ 。写出步骤Ⅱ中用SO2吸收Br2的离子方程式:___________ 。
 、Na+、Mg2+、Ca2+等,都是重要资源。开发和利用海水资源是当前科学研究的一项重要任务,如图是某化工厂对海水资源综合利用的示意图:
、Na+、Mg2+、Ca2+等,都是重要资源。开发和利用海水资源是当前科学研究的一项重要任务,如图是某化工厂对海水资源综合利用的示意图:
请根据以上信息回答下列问题:
(1)写出步骤②、⑧分离提纯的方法:②
(2)步骤⑦分离提纯过程中需要选用的玻璃仪器除烧杯外,还需要的仪器是
(3)步骤③的是电解食盐水,工业上称为氯碱工业,D具有杀菌消毒的作用,在喷洒前需要在空气中晾置一会,这样做的原因是
(4)初步提纯后的粗盐中含有Mg2+、Ca2+、
 等杂质,精制时所用的试剂为①盐酸②氯化钡溶液③氢氧化钠溶液④碳酸钠溶液,下列试剂添加顺序合理的是___________。
等杂质,精制时所用的试剂为①盐酸②氯化钡溶液③氢氧化钠溶液④碳酸钠溶液,下列试剂添加顺序合理的是___________。| A.②③④① | B.③④①② | C.④③②① | D.③②④① |

其中步骤Ⅱ、Ⅲ起到的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】硫酸工业中会产生含 的烟气,有机化工中会产生含
的烟气,有机化工中会产生含 的尾气,这些尾气排放到空气中会污染环境。
的尾气,这些尾气排放到空气中会污染环境。
(1)用氨水可吸收含 的烟气,写出该反应的化学方程式:
的烟气,写出该反应的化学方程式:_______ 。
(2)用如图所示的装置可以将含 的烟气和
的烟气和 混合吸收。
混合吸收。

①若NaOH溶液不足,出口处可能有 或
或 中的一种排出。实验小组为检验出口处是否有
中的一种排出。实验小组为检验出口处是否有 排出,将出口处的气体通入装有品红溶液的试管中,观察到品红溶液褪色。该现象能否说明出口处有
排出,将出口处的气体通入装有品红溶液的试管中,观察到品红溶液褪色。该现象能否说明出口处有 排出,若能,则说明理由,若不能,请在不使用其他试剂的条件下,用含褪色后溶液的试管进行补充实验,确认出口处是否有
排出,若能,则说明理由,若不能,请在不使用其他试剂的条件下,用含褪色后溶液的试管进行补充实验,确认出口处是否有 排出:
排出:_______ 。
②某同学预测反应后的溶液中可能大量存在 、
、 、
、 、
、 、
、 等离子。该预测是不正确的是,因为
等离子。该预测是不正确的是,因为_______ 和_______ 不能大量共存。
③实验结束后,经检测广口瓶溶液中含 、
、 等离子。为测定溶液中
等离子。为测定溶液中 的物质的量浓度,现进行如下实验:取100mL广口瓶中溶液,向其中滴加
的物质的量浓度,现进行如下实验:取100mL广口瓶中溶液,向其中滴加 的标准
的标准 溶液(发生反应
溶液(发生反应
 ),恰好完全反应时消耗标准
),恰好完全反应时消耗标准 溶液20mL。向反应后的溶液中继续滴加
溶液20mL。向反应后的溶液中继续滴加 溶液,恰好完全反应时,生成沉淀6.99g.计算原广口瓶溶液中
溶液,恰好完全反应时,生成沉淀6.99g.计算原广口瓶溶液中 的物质的量浓度,并写出计算过程
的物质的量浓度,并写出计算过程_______ 。
 的烟气,有机化工中会产生含
的烟气,有机化工中会产生含 的尾气,这些尾气排放到空气中会污染环境。
的尾气,这些尾气排放到空气中会污染环境。(1)用氨水可吸收含
 的烟气,写出该反应的化学方程式:
的烟气,写出该反应的化学方程式:(2)用如图所示的装置可以将含
 的烟气和
的烟气和 混合吸收。
混合吸收。
①若NaOH溶液不足,出口处可能有
 或
或 中的一种排出。实验小组为检验出口处是否有
中的一种排出。实验小组为检验出口处是否有 排出,将出口处的气体通入装有品红溶液的试管中,观察到品红溶液褪色。该现象能否说明出口处有
排出,将出口处的气体通入装有品红溶液的试管中,观察到品红溶液褪色。该现象能否说明出口处有 排出,若能,则说明理由,若不能,请在不使用其他试剂的条件下,用含褪色后溶液的试管进行补充实验,确认出口处是否有
排出,若能,则说明理由,若不能,请在不使用其他试剂的条件下,用含褪色后溶液的试管进行补充实验,确认出口处是否有 排出:
排出:②某同学预测反应后的溶液中可能大量存在
 、
、 、
、 、
、 、
、 等离子。该预测是不正确的是,因为
等离子。该预测是不正确的是,因为③实验结束后,经检测广口瓶溶液中含
 、
、 等离子。为测定溶液中
等离子。为测定溶液中 的物质的量浓度,现进行如下实验:取100mL广口瓶中溶液,向其中滴加
的物质的量浓度,现进行如下实验:取100mL广口瓶中溶液,向其中滴加 的标准
的标准 溶液(发生反应
溶液(发生反应
 ),恰好完全反应时消耗标准
),恰好完全反应时消耗标准 溶液20mL。向反应后的溶液中继续滴加
溶液20mL。向反应后的溶液中继续滴加 溶液,恰好完全反应时,生成沉淀6.99g.计算原广口瓶溶液中
溶液,恰好完全反应时,生成沉淀6.99g.计算原广口瓶溶液中 的物质的量浓度,并写出计算过程
的物质的量浓度,并写出计算过程
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务.
 实验目的
实验目的 制取乙酸乙酯
制取乙酸乙酯
 实验原理
实验原理 甲、乙、丙三位同学均采取乙醇、乙酸与浓
甲、乙、丙三位同学均采取乙醇、乙酸与浓 混合共热的方法制取乙酸乙酯,反应的方程式为
混合共热的方法制取乙酸乙酯,反应的方程式为 ______  其中浓
其中浓 的作用是
的作用是 ______ 和 ______
 装置设计
装置设计 甲、乙、丙三位同学分别设计如图三套实验装置:
甲、乙、丙三位同学分别设计如图三套实验装置:

请从甲、乙两位同学设计的装置中选择一种作为实验室制取乙酸乙酯的装置,我选择的装置是______  选填“甲”或“乙”
选填“甲”或“乙” ,丙同学将甲装置中的玻璃管改成球形干燥管,除起冷凝作用外,另一重要作用是
,丙同学将甲装置中的玻璃管改成球形干燥管,除起冷凝作用外,另一重要作用是 ______
 实验步骤
实验步骤
 按我选择的装置仪器,在试管中先加入3mL乙醇,并在摇动下缓缓加入2mL浓
按我选择的装置仪器,在试管中先加入3mL乙醇,并在摇动下缓缓加入2mL浓 充分摇匀,冷却后再加入2mL冰醋酸;
充分摇匀,冷却后再加入2mL冰醋酸; 将试管固定在铁架台上;
将试管固定在铁架台上; 在试管B中加入适量的饱和
在试管B中加入适量的饱和 溶液;
溶液; 用酒精灯对试管A加热;
用酒精灯对试管A加热; 当观察到试管B中有明显现象时停止实验.
当观察到试管B中有明显现象时停止实验.
 问题讨论
问题讨论
 步骤
步骤 装好实验装置,加入样品前还应检查
装好实验装置,加入样品前还应检查 ______ .
 从试管B中分离出乙酸乙酯的实验操作是
从试管B中分离出乙酸乙酯的实验操作是 ______ .
 实验目的
实验目的 制取乙酸乙酯
制取乙酸乙酯 实验原理
实验原理 甲、乙、丙三位同学均采取乙醇、乙酸与浓
甲、乙、丙三位同学均采取乙醇、乙酸与浓 混合共热的方法制取乙酸乙酯,反应的方程式为
混合共热的方法制取乙酸乙酯,反应的方程式为  其中浓
其中浓 的作用是
的作用是  装置设计
装置设计 甲、乙、丙三位同学分别设计如图三套实验装置:
甲、乙、丙三位同学分别设计如图三套实验装置:
请从甲、乙两位同学设计的装置中选择一种作为实验室制取乙酸乙酯的装置,我选择的装置是
 选填“甲”或“乙”
选填“甲”或“乙” ,丙同学将甲装置中的玻璃管改成球形干燥管,除起冷凝作用外,另一重要作用是
,丙同学将甲装置中的玻璃管改成球形干燥管,除起冷凝作用外,另一重要作用是  实验步骤
实验步骤
 按我选择的装置仪器,在试管中先加入3mL乙醇,并在摇动下缓缓加入2mL浓
按我选择的装置仪器,在试管中先加入3mL乙醇,并在摇动下缓缓加入2mL浓 充分摇匀,冷却后再加入2mL冰醋酸;
充分摇匀,冷却后再加入2mL冰醋酸; 将试管固定在铁架台上;
将试管固定在铁架台上; 在试管B中加入适量的饱和
在试管B中加入适量的饱和 溶液;
溶液; 用酒精灯对试管A加热;
用酒精灯对试管A加热; 当观察到试管B中有明显现象时停止实验.
当观察到试管B中有明显现象时停止实验. 问题讨论
问题讨论
 步骤
步骤 装好实验装置,加入样品前还应检查
装好实验装置,加入样品前还应检查  从试管B中分离出乙酸乙酯的实验操作是
从试管B中分离出乙酸乙酯的实验操作是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】化学是以实验为基础的学科。
演示实验1:金属钠与水的反应是中学化学中的一个重要反应,该反应的演示方法分别如图中①②所示:
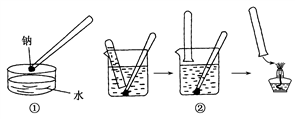
(1)现按图①所示的方法,在室温时,向盛有Ca(HCO3)2溶液的水槽中,加入一小块金属钠。下列现象描述正确的是________ (填选项字母)。
A.钠浮在液面上,并四处游动,最后消失
B.钠熔化成一个光亮的小球
C.反应开始后,溶液由无色变红色
D.恢复到室温时,烧杯底部有固体物质析出
(2)请补充并完成①实验中从试剂瓶中取出钠到向水槽中投入钠的有关操作:用镊子从试剂瓶中取出一小块钠→_____________ →用镊子夹取切好的金属钠投入到盛有Ca(HCO3)2溶液的烧杯中。
(3)按图②所示方法来收集产生的气体,需将钠包好,再放入水中。取相同质量的钠按下列几种情况收集产生的气体在相同条件下体积最大的是________ (填选项字母)。
A.用铝箔包住钠
B.用锡箔包住钠
C.直接将钠投入水中
演示实验2:某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并放出耀眼的光芒”“纸漏斗的下部被烧穿,有熔融物落入沙中”。查阅《化学手册》知:Al、Al2O3、Fe、Fe2O3的熔点、沸点数据如下:
(4)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是________ ,反应的离子方程式为___________________________ 。
(5)实验室溶解该熔融物,下列试剂中最好的是________ (填选项字母)。
A.浓硫酸 B.稀硫酸
C.稀硝酸 D.氢氧化钠溶液
演示实验1:金属钠与水的反应是中学化学中的一个重要反应,该反应的演示方法分别如图中①②所示:

(1)现按图①所示的方法,在室温时,向盛有Ca(HCO3)2溶液的水槽中,加入一小块金属钠。下列现象描述正确的是
A.钠浮在液面上,并四处游动,最后消失
B.钠熔化成一个光亮的小球
C.反应开始后,溶液由无色变红色
D.恢复到室温时,烧杯底部有固体物质析出
(2)请补充并完成①实验中从试剂瓶中取出钠到向水槽中投入钠的有关操作:用镊子从试剂瓶中取出一小块钠→
(3)按图②所示方法来收集产生的气体,需将钠包好,再放入水中。取相同质量的钠按下列几种情况收集产生的气体在相同条件下体积最大的是
A.用铝箔包住钠
B.用锡箔包住钠
C.直接将钠投入水中
演示实验2:某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并放出耀眼的光芒”“纸漏斗的下部被烧穿,有熔融物落入沙中”。查阅《化学手册》知:Al、Al2O3、Fe、Fe2O3的熔点、沸点数据如下:
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2 054 | 1 535 | 1 462 |
| 沸点/℃ | 2 467 | 2 980 | 2 750 |
(5)实验室溶解该熔融物,下列试剂中最好的是
A.浓硫酸 B.稀硫酸
C.稀硝酸 D.氢氧化钠溶液
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某校化学课外研究小组为验证浓硫酸与金属Zn反应产生的气体中含SO2和H2,进行了下列实验活动:

(1)在装入药品前,甲同学需检查装置_____ 。
(2)填写下表中的实验现象:_____ 。
(3)装置C的作用是_____ ,写出装置C中发生反应的离子方程式_____ 。
(4)装置D的作用是_____ 。
(5)SO2是大气污染物之一,也是某工业生产中的主要尾气之一。某校兴趣小组欲采用下列方案测定此工业尾气中的SO2的含量。

通过的尾气体积为VL(已换算成标准状况)时,该尾气中SO2含量(体积分数)为_____ (用含有V、m的代数式表示)。

(1)在装入药品前,甲同学需检查装置
(2)填写下表中的实验现象:
| 装置 | B | F | G |
| 实验现象 |
(4)装置D的作用是
(5)SO2是大气污染物之一,也是某工业生产中的主要尾气之一。某校兴趣小组欲采用下列方案测定此工业尾气中的SO2的含量。

通过的尾气体积为VL(已换算成标准状况)时,该尾气中SO2含量(体积分数)为
您最近一年使用:0次



