某大学开发出纸一样薄的可生物降解锌电池,一化学兴趣小组受到启发,设计出如图所示装置用于探究原电池构成条件。回答下列问题:
(1)甲同学设计了下列实验探究原电池的构成条件。
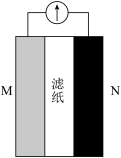
①实验1中电流计指针发生偏转的原因为_______ (填标号)。
A.铝与铜的活泼性不同 B.稀硫酸为电解质
C.整个装置形成了闭合回路 D.铜不与稀硫酸反应
②实验1中电流计发生偏转的原因之一是溶液中有自由移动的_______ (填“分子”、“离子”或“电子”);实验4中,原电池的负极为_______ (填“铝箔”或“铜箔”)。
(2)乙同学设计了下列实验探究原电池的构成条件。
①实验5、6中,所用稀H2SO4的物质的量的浓度相同,N极均观察到有气泡产生,产生气泡较快的是实验_______ (填“5”或“6”),原因是_______ 。
②实验7中的未知溶液可能为_______ (填标号)。
a.浓盐酸 b.浓硝酸 c.NaOH溶液 d.稀硫酸
(3)丙同学按下列材料设计了一原电池,该电池工作时, 移向
移向_______ (填“M”或“N”)极,该电池的正极表面发生的电极反应为_______ 。
(1)甲同学设计了下列实验探究原电池的构成条件。

| 试验编号 | M极材料 | N极材料 | 滤纸浸泡物质 | 电流计指针是否偏转 |
| 1 | 铝箔 | 铜箔 | 稀H2SO4 | 是 |
| 2 | 铝箔 | 铜箔 | 乙醇 | 否 |
| 3 | 铝箔 | 铜箔 | 蔗糖溶液 | 否 |
| 4 | 铝箔 | 铜箔 | 番茄汁(pH≈4) | 是 |
A.铝与铜的活泼性不同 B.稀硫酸为电解质
C.整个装置形成了闭合回路 D.铜不与稀硫酸反应
②实验1中电流计发生偏转的原因之一是溶液中有自由移动的
(2)乙同学设计了下列实验探究原电池的构成条件。
| 试验编号 | M极材料 | N极材料 | 滤纸浸泡物质 | 电流计指针是否偏转及偏转方向 |
| 5 | 铝箔 | 铜箔 | 稀H2SO4 | 偏向铝箔 |
| 6 | 铝箔 | 铝箔 | 稀H2SO4 | 不偏转 |
| 7 | 铜箔 | 铝箔 | 未知溶液 | 偏向铜箔 |
②实验7中的未知溶液可能为
a.浓盐酸 b.浓硝酸 c.NaOH溶液 d.稀硫酸
(3)丙同学按下列材料设计了一原电池,该电池工作时,
 移向
移向| M极材料 | N极材料 | 滤纸浸泡物质 |
| 铁箔 | 铜箔 | FeCl3稀溶液 |
更新时间:2023-09-06 22:57:58
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】研究大气中含硫化合物(主要是SO2和H2S)的转化具有重要意义。
(1)工业上采用高温热分解H2S的方法制取H2,在膜反应器中分离H2,发生的反应为2H2S(g) 2H2(g)+S2(g) △H。
2H2(g)+S2(g) △H。
已知:①H2S(g) H2(g)+S(g) △H1;
H2(g)+S(g) △H1;
②2S(g) S2(g) △H2。
S2(g) △H2。
则△H=______ (用含△H1、△H2的式子表示)。
(2)土壤中的微生物可将大气中的H2S经两步反应氧化成SO ,两步反应的能量变化示意图如图:
,两步反应的能量变化示意图如图: (aq)的热化学方程式为
(aq)的热化学方程式为_______ 。
(3)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。______ 。
②在温度一定和不补加溶液的条件下,缓慢通入混合气体,并充分搅拌。欲使生成的硫单质中不含CuS,可采取的措施有_______ 。
(4)二氧化硫—空气质子交换膜燃料电池可以利用大气中所含SO2快速启动,其装置示意图如图所示:______ (填“从A到B”或“从B到A”)。
②负极的电极反应为________ 。
(1)工业上采用高温热分解H2S的方法制取H2,在膜反应器中分离H2,发生的反应为2H2S(g)
 2H2(g)+S2(g) △H。
2H2(g)+S2(g) △H。已知:①H2S(g)
 H2(g)+S(g) △H1;
H2(g)+S(g) △H1;②2S(g)
 S2(g) △H2。
S2(g) △H2。则△H=
(2)土壤中的微生物可将大气中的H2S经两步反应氧化成SO
 ,两步反应的能量变化示意图如图:
,两步反应的能量变化示意图如图: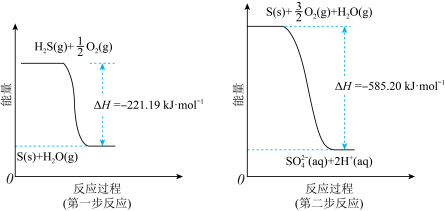
 (aq)的热化学方程式为
(aq)的热化学方程式为(3)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。
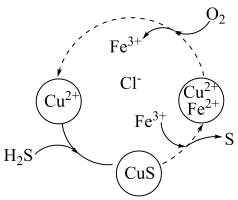
②在温度一定和不补加溶液的条件下,缓慢通入混合气体,并充分搅拌。欲使生成的硫单质中不含CuS,可采取的措施有
(4)二氧化硫—空气质子交换膜燃料电池可以利用大气中所含SO2快速启动,其装置示意图如图所示:
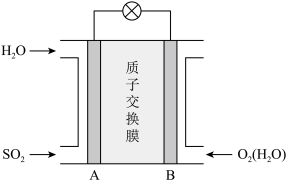
②负极的电极反应为
您最近一年使用:0次
【推荐2】某课外小组利用甲烷燃料电池为电源在铁螺母表面上镀铜,装置如图所示:
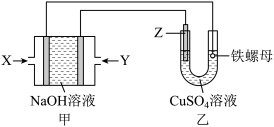
回答下列问题:
(1)X是气体___________ (填化学式),判断理由是___________ ,X所在电极的电极反应式是___________ 。
(2)Z是___________ (填化学式)。铁螺母表面镀铜完成后,理论上 溶液的浓度
溶液的浓度___________ (填“增大”“减小”或“不变”)。
(3)铁螺母表面镀铜完成后,称重,质量增加3.2g,则理论上消耗甲烷___________ L(标准状况)。实际上消耗甲烷的体积比理论值大,其原因可能是___________ 。

回答下列问题:
(1)X是气体
(2)Z是
 溶液的浓度
溶液的浓度(3)铁螺母表面镀铜完成后,称重,质量增加3.2g,则理论上消耗甲烷
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】 ( 1 )观察如图所示的两个装置,图1装置中铜电极上产生大量的无色气泡,图2装置中铜电极上无气体产生,而铬电极上产生大量的有色气体。根据上述现象试推测金属铬具有的两种重要化学性质为

①____________________________________ 。
②____________________________________ 。
( 2 )如图是甲烷燃料电池原理示意图,回答下列问题:

① 电池的负极是________ (填“a”或“b”)电极,该极的电极反应式为_____________________ 。
② 电池工作一段时间后电解质溶液的pH________ 。(填“增大”“减小”或“不变”)
(3)如图甲乙所示为某实验小组设计的原电池:

①该小组依据的氧化还原反应为(写离子方程式)________ 。
②已知反应前电极质量相等,一段时间后,两电极质量相差12 g,则导线中通过________ mol电子。
③用吸管吸出铁片附近溶液少许置于试管中,向其中滴加少量新制饱和氯水,发生的离子反应为__________ ,然后滴加几滴硫氰化钾溶液,溶液变红。

①
②
( 2 )如图是甲烷燃料电池原理示意图,回答下列问题:

① 电池的负极是
② 电池工作一段时间后电解质溶液的pH
(3)如图甲乙所示为某实验小组设计的原电池:

①该小组依据的氧化还原反应为(写离子方程式)
②已知反应前电极质量相等,一段时间后,两电极质量相差12 g,则导线中通过
③用吸管吸出铁片附近溶液少许置于试管中,向其中滴加少量新制饱和氯水,发生的离子反应为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】电池的应用给我们的生活带来了便利,请根据原电池工作原理回答下列问题:
(1)①图中原电池工作时,正极上的电极反应式为________ 。
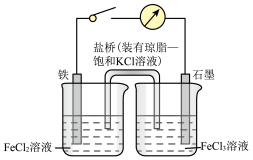
②该原电池工作时,下列说法正确的是_______ (填标号)。
A.电子移动的方向:铁电极 石墨电极
石墨电极
B.盐桥中的K+会向右侧烧杯移动
C.FeCl2溶液的颜色会逐渐变浅
D.将KCl盐桥换成AgNO3盐桥,该装置不能长时间正常工作
(2)铅酸蓄电池是常见的二次电池,其工作原理如图所示。
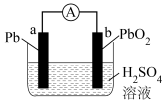
①写出放电时正极的电极反应式:_______ 。
②铅酸蓄电池放电时一段时间,当转移0.2mol电子时,负极质量将增大______ g。
(3)肼—空气燃料电池是一种无污染,能量高,有广泛的应用前景的燃料电池。某化学小组设计一种肼—空气燃料电池,除将化学能转化为电能外,还能将饱和食盐水淡化,同时还可获得盐酸和NaOH两种副产品。其工作原理如图所示:
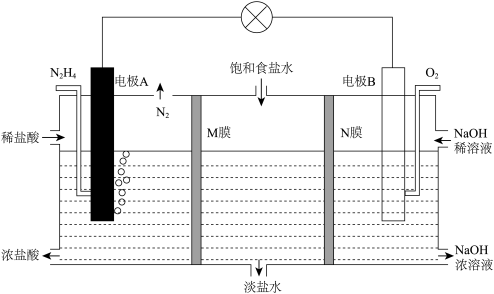
①该燃料电池A电极名称是______ (填“正极”或“负极”),A电极的电极反应式为_______ 。
②N膜为_______ (填“阳离子交换膜”或“阴离子交换膜”)。
③当电路中有0.2mol电子转移时,正极室质量增加_____ g。
(1)①图中原电池工作时,正极上的电极反应式为

②该原电池工作时,下列说法正确的是
A.电子移动的方向:铁电极
 石墨电极
石墨电极B.盐桥中的K+会向右侧烧杯移动
C.FeCl2溶液的颜色会逐渐变浅
D.将KCl盐桥换成AgNO3盐桥,该装置不能长时间正常工作
(2)铅酸蓄电池是常见的二次电池,其工作原理如图所示。

①写出放电时正极的电极反应式:
②铅酸蓄电池放电时一段时间,当转移0.2mol电子时,负极质量将增大
(3)肼—空气燃料电池是一种无污染,能量高,有广泛的应用前景的燃料电池。某化学小组设计一种肼—空气燃料电池,除将化学能转化为电能外,还能将饱和食盐水淡化,同时还可获得盐酸和NaOH两种副产品。其工作原理如图所示:

①该燃料电池A电极名称是
②N膜为
③当电路中有0.2mol电子转移时,正极室质量增加
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】能量、速率与限度是认识和研究化学反应的重要视角。
Ⅰ.为了探究原电池的工作原理,设计如下装置。

(1)甲装置中负极电极反应式为_____ 。
(2)当乙装置中的负极质量减少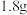 时,正极产生气体
时,正极产生气体_____ L(标准状况下); 向
向_____ (填“ ”或“
”或“ ”)电极移动。
”)电极移动。
(3)当丙装置中导线通过 电子时,两电极质量相差
电子时,两电极质量相差_____ g(放电前两电极质量相等)。
Ⅱ. 都是重要的能源物质,也是重要的化工原料。利用
都是重要的能源物质,也是重要的化工原料。利用 还原
还原 能有效促进“碳中和”,反应的化学方程式为
能有效促进“碳中和”,反应的化学方程式为 。
。
(4)反应过程中的能量变化如图所示:
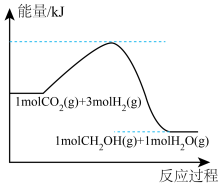
则该反应是_____ (填“放热”或“吸热”)反应。
(5)300℃时,向容积为 的恒容密闭容器中,充入
的恒容密闭容器中,充入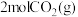 和
和 ,反应过程中测得各物质的物质的量浓度随时间变化如图所示。回答下列问题:
,反应过程中测得各物质的物质的量浓度随时间变化如图所示。回答下列问题:
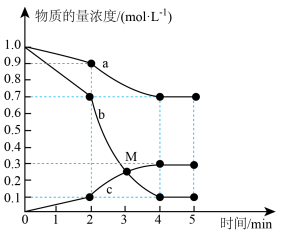
① 的浓度随时间变化曲线为
的浓度随时间变化曲线为_____ (填“a”、“b”或“c”);在M点,
_____ 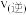 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
② 时,反应速率改变的原因可能是
时,反应速率改变的原因可能是_____ 。
A.升高温度B.降低温度C.充入一定量的 D.加入催化剂
D.加入催化剂
③下列叙述不能说明该反应达到平衡状态的是_____ 。
A.
B.混合气体的密度不再变化
C.混合气体的平均摩尔质量不再变化
D.单位时间内生成 ,同时消耗
,同时消耗
Ⅰ.为了探究原电池的工作原理,设计如下装置。

(1)甲装置中负极电极反应式为
(2)当乙装置中的负极质量减少
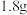 时,正极产生气体
时,正极产生气体 向
向 ”或“
”或“ ”)电极移动。
”)电极移动。(3)当丙装置中导线通过
 电子时,两电极质量相差
电子时,两电极质量相差Ⅱ.
 都是重要的能源物质,也是重要的化工原料。利用
都是重要的能源物质,也是重要的化工原料。利用 还原
还原 能有效促进“碳中和”,反应的化学方程式为
能有效促进“碳中和”,反应的化学方程式为 。
。(4)反应过程中的能量变化如图所示:

则该反应是
(5)300℃时,向容积为
 的恒容密闭容器中,充入
的恒容密闭容器中,充入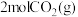 和
和 ,反应过程中测得各物质的物质的量浓度随时间变化如图所示。回答下列问题:
,反应过程中测得各物质的物质的量浓度随时间变化如图所示。回答下列问题:
①
 的浓度随时间变化曲线为
的浓度随时间变化曲线为
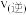 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。②
 时,反应速率改变的原因可能是
时,反应速率改变的原因可能是A.升高温度B.降低温度C.充入一定量的
 D.加入催化剂
D.加入催化剂③下列叙述不能说明该反应达到平衡状态的是
A.

B.混合气体的密度不再变化
C.混合气体的平均摩尔质量不再变化
D.单位时间内生成
 ,同时消耗
,同时消耗
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】如图是两种溶液进行电解的装置。电极A是由金属M制成的,M的硝酸盐的化学式为M(NO3)2,B、C、D都是铂电极,P、Q是电池的两极。

(1)电路接通后,B极上析出金属M,其电极反应为_______ ;同时C极产生____ ,电极反应为_______ ;D极产生____ ,电极反应为_______ 。
(2)电池中P是____ 极,Q是____ 极。
(3)A极上电极反应为__________ 。
(4)当电路中通过2.408×1022个电子时,B极上析出1.27 g M,则M的相对原子质量为____ 。
(5)如果将电池的正、负极交换接入原电路,当通过1.204×1022个电子时,B极上的现象是________ ,电极反应为______ ;A极上析出金属___ g,电极反应为______ (假设M为Cu)。

(1)电路接通后,B极上析出金属M,其电极反应为
(2)电池中P是
(3)A极上电极反应为
(4)当电路中通过2.408×1022个电子时,B极上析出1.27 g M,则M的相对原子质量为
(5)如果将电池的正、负极交换接入原电路,当通过1.204×1022个电子时,B极上的现象是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】霾由多种污染物形成,包含颗粒物(PM2.5)、氮氧化物(NOx)、CO、SO2等。化学在解决雾霾污染中有着重要的作用
(1)已知:①2CO(g)+O2(g)=2CO2(g) ΔH1=-566.0 kJ·mol-1
②2NO(g)+O2(g)=2NO2(g) ΔH2=-116.5 kJ·mol-1
③N2(g)+O2(g)=2NO(g) ΔH3=+180.5 kJ·mol-1
废气中NO2与CO 转化成无污染气体的热化学方程式为_______ 。
(2)研究发现利用NH3可除去硝酸工业尾气中的NO。NH3与NO的物质的量之比分别为1∶2、1∶1.5、3∶1时,NO脱除率随温度变化的曲线如图所示。
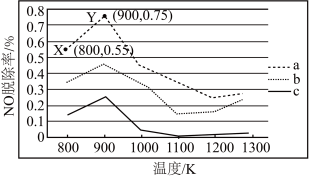
①曲线a中,NO的起始浓度为6×10-4 mg·m-3,从X点到Y点经过10 s,则该时间段内NO的脱除速率为_______ mg· m-3·s-1。
②曲线c对应的NH3与NO的物质的量之比是_______ ,其理由是_______ 。
(3)利用反应6NO2+8NH3=7N2+12H2O构成的电池既能有效消除氮氧化物的排放,减轻雾霾污染,又能充分利用化学能,装置如图所示。
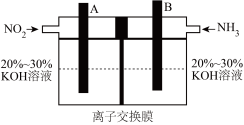
①B极的电极反应式为_______ 。
②若反应转移1.2 mol电子,A极生成N2的体积为_______ L(标准状况)。
(4)炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成活化氧,活化氧可以快速氧化SO2.活化过程的能量变化模拟计算结果如图所示:

无水情况下,一个氧分子反应的活化能为_______ ,容易活化氧分子的条件是_______ (填“有水”或“无水”)。
(1)已知:①2CO(g)+O2(g)=2CO2(g) ΔH1=-566.0 kJ·mol-1
②2NO(g)+O2(g)=2NO2(g) ΔH2=-116.5 kJ·mol-1
③N2(g)+O2(g)=2NO(g) ΔH3=+180.5 kJ·mol-1
废气中NO2与CO 转化成无污染气体的热化学方程式为
(2)研究发现利用NH3可除去硝酸工业尾气中的NO。NH3与NO的物质的量之比分别为1∶2、1∶1.5、3∶1时,NO脱除率随温度变化的曲线如图所示。

①曲线a中,NO的起始浓度为6×10-4 mg·m-3,从X点到Y点经过10 s,则该时间段内NO的脱除速率为
②曲线c对应的NH3与NO的物质的量之比是
(3)利用反应6NO2+8NH3=7N2+12H2O构成的电池既能有效消除氮氧化物的排放,减轻雾霾污染,又能充分利用化学能,装置如图所示。

①B极的电极反应式为
②若反应转移1.2 mol电子,A极生成N2的体积为
(4)炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成活化氧,活化氧可以快速氧化SO2.活化过程的能量变化模拟计算结果如图所示:

无水情况下,一个氧分子反应的活化能为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】BiOCl常用于电子设备等领域和一般化妆品的白色颜料。某工厂采用辉铋矿(主要成分为 ,含有
,含有 、
、 杂质)与软锰矿(主要成分为
杂质)与软锰矿(主要成分为 )联合焙烧法制备BiOCl的工艺流程如图所示。
)联合焙烧法制备BiOCl的工艺流程如图所示。

已知:①焙烧时过量的 分解为
分解为 。
。
②金属活动性: 。
。
③ 易水解。常温下,
易水解。常温下,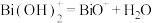 。
。
回答下列问题:
(1)为加快“水浸”的速率,可采取的措施有___________ (写一条)。
(2)“酸浸”产生气体a的离子方程式是___________ ,浓盐酸除了浸取一些金属离子、提供 外,还有一个重要的作用是
外,还有一个重要的作用是___________ 。
(3)某科研小组将“转化”设计为原电池,其反应原理如图所示:

①Y和Z是含有 的溶液,则Y是
的溶液,则Y是___________ 、Z是___________ 。
②X应选择___________ (填“Fe”“Cu”或“石墨”),电极反应式是___________ 。
 ,含有
,含有 、
、 杂质)与软锰矿(主要成分为
杂质)与软锰矿(主要成分为 )联合焙烧法制备BiOCl的工艺流程如图所示。
)联合焙烧法制备BiOCl的工艺流程如图所示。
已知:①焙烧时过量的
 分解为
分解为 。
。②金属活动性:
 。
。③
 易水解。常温下,
易水解。常温下,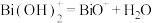 。
。回答下列问题:
(1)为加快“水浸”的速率,可采取的措施有
(2)“酸浸”产生气体a的离子方程式是
 外,还有一个重要的作用是
外,还有一个重要的作用是(3)某科研小组将“转化”设计为原电池,其反应原理如图所示:

①Y和Z是含有
 的溶液,则Y是
的溶液,则Y是②X应选择
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】电化学是化学研究重要分支,在生产生活中发挥着非常重要的作用。请回答下列问题:
(1)某空间站局部能量转化系统如图所示,其中氢氧燃料电池采用KOH溶液为电解液,燃料电池放电时的负极反应式为_______ 。
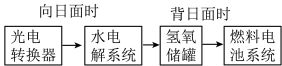
(2)在载人航天器的生态系统中,不仅要求分离出CO2,还要求提供充足的O2.某种电化学装置可实现转化2CO2=2CO+O2,CO可用作燃料。已知该反应的阳极反应式为4OH--4e-=O2↑+2H2O,则阴极反应式为:_______ 。
(3)铅酸蓄电池是最常见的二次电池,电压稳定,安全可靠,价格低廉,应用广泛。电池总反应为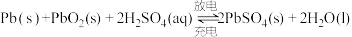 。
。
①放电时,正极的电极反应式:_______ ,电解质溶液中硫酸的浓度_______ (填“增大”“减小”或“不变”),当外电路通过0.5 mol 时,理论上负极板的质量增加
时,理论上负极板的质量增加_______ g。
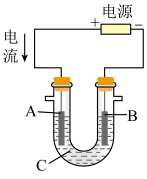
②用该蓄电池作电源,进行粗铜(含Ag、Pt、Au等杂质)的电解精炼。如下图所示,电解液c选用_______ 溶液,A电极的材料是_______ ,B电极反应式是_______ 。
(4)以CH3OH燃料电池为电源电解法制取ClO2,二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。

①CH3OH燃料电池放电过程中,负极反应式为_______ 。
②图中电解池用石墨作电极,在一定条件下电解饱和食盐水制取ClO2,阳极产生ClO2的反应式为_______ 。
③电解一段时间,从阴极处收集到的气体比阳极处收集到气体多1.12 L时(标准状况,忽略生成的气体溶解),停止电解,通过阳离子交换膜的阳离子为_______ mol(精确到小数点后两位)。
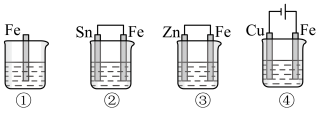
(5)下图所示的各容器中均盛有海水,铁在其中被腐蚀时由快到慢的顺序是_______。
(1)某空间站局部能量转化系统如图所示,其中氢氧燃料电池采用KOH溶液为电解液,燃料电池放电时的负极反应式为

(2)在载人航天器的生态系统中,不仅要求分离出CO2,还要求提供充足的O2.某种电化学装置可实现转化2CO2=2CO+O2,CO可用作燃料。已知该反应的阳极反应式为4OH--4e-=O2↑+2H2O,则阴极反应式为:
(3)铅酸蓄电池是最常见的二次电池,电压稳定,安全可靠,价格低廉,应用广泛。电池总反应为
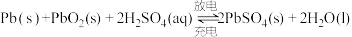 。
。①放电时,正极的电极反应式:
 时,理论上负极板的质量增加
时,理论上负极板的质量增加②用该蓄电池作电源,进行粗铜(含Ag、Pt、Au等杂质)的电解精炼。如下图所示,电解液c选用

(4)以CH3OH燃料电池为电源电解法制取ClO2,二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。

①CH3OH燃料电池放电过程中,负极反应式为
②图中电解池用石墨作电极,在一定条件下电解饱和食盐水制取ClO2,阳极产生ClO2的反应式为
③电解一段时间,从阴极处收集到的气体比阳极处收集到气体多1.12 L时(标准状况,忽略生成的气体溶解),停止电解,通过阳离子交换膜的阳离子为
(5)下图所示的各容器中均盛有海水,铁在其中被腐蚀时由快到慢的顺序是_______。

| A.④>②>③>① | B.②>①>③>④ |
| C.④>②>①>③ | D.③>②>④>① |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】科学探究要实事求是、严谨细致。某化学兴趣小组设计实验进行有关氯化物的探究实验,回答下列问题:
Ⅰ.FeCl3在工业生产中应用广泛,某化学研究性学习小组模拟工业流程制备无水FeCl3。经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。他们设计了以Fe粉和Cl2为原料制备无水FeCl3的实验方案,装置示意图如下:___________ 。
(2)装置A中设计g管的作用是___________ 。
(3)装置A中发生反应的离子方程式为___________ 。
Ⅱ.利用惰性电极电解0.1mol/LFeCl2溶液,探究外界条件对电极反应(离子放电顺序)的影响。
实验数据如表所示:
(4)由实验1、2现象可以得出结论:增大pH,___________ 优先于___________ 放电;
Ⅲ.为了探究外界条件对氯化铵水解平衡的影响,兴趣小组设计了如下实验方案:
(5)该实验限选药品和仪器:恒温水浴、pH传感器、烧杯、0.1mol/L硝酸银溶液、蒸馏水和各种浓度的NH4Cl溶液。
①实验中,“待测物理量X”是___________ ;
②为了探究浓度对氯化铵水解平衡的影响,实验6可与实验___________ 作对照实验;
③实验目的ii是___________ ;
④氯化铵在生产生活中有很多实用的用途,请写出一种应用:___________ 。
Ⅰ.FeCl3在工业生产中应用广泛,某化学研究性学习小组模拟工业流程制备无水FeCl3。经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。他们设计了以Fe粉和Cl2为原料制备无水FeCl3的实验方案,装置示意图如下:
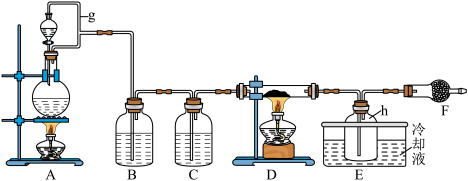
(2)装置A中设计g管的作用是
(3)装置A中发生反应的离子方程式为
Ⅱ.利用惰性电极电解0.1mol/LFeCl2溶液,探究外界条件对电极反应(离子放电顺序)的影响。
实验数据如表所示:
| 实验编号 | 电压/V | pH | 阳极现象 | 阴极现象 |
| 1 | 1.5 | 1.00 | 无气泡,滴加KSCN显红色 | 较多气泡,极少量金属析出 |
| 2 | 1.5 | 5.52 | 无气泡,滴加KSCN显红色 | 无气泡,银白色金属析出 |
| 3 | 3.0 | 5.52 | 少量气泡,滴加KSCN显红色 | 无气泡,银白色金属析出 |
| 4 | 4.5 | 5.52 | 大量气泡,滴加KSCN显红色 | 较多气泡,极少量金属析出 |
(4)由实验1、2现象可以得出结论:增大pH,
Ⅲ.为了探究外界条件对氯化铵水解平衡的影响,兴趣小组设计了如下实验方案:
| 实验编号 | c(NH4Cl)/mol·L-1 | 温度/℃ | 待测物理量X | 实验目的 |
| 5 | 0.5 | 30 | a | ___________ |
| 6 | 1.5 | i | b | 探究浓度对氯化铵水解平衡的影响 |
| 7 | 1.5 | 35 | c | ii |
| 8 | 2.0 | 40 | d | 探究温度、浓度同时对氯化铵化解平衡的影响 |
(5)该实验限选药品和仪器:恒温水浴、pH传感器、烧杯、0.1mol/L硝酸银溶液、蒸馏水和各种浓度的NH4Cl溶液。
①实验中,“待测物理量X”是
②为了探究浓度对氯化铵水解平衡的影响,实验6可与实验
③实验目的ii是
④氯化铵在生产生活中有很多实用的用途,请写出一种应用:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】有甲、乙两位同学均想利用原电池反应检测金属的活动性强弱,两人均使用镁片与铝片作电极,但甲同学将电极放入6 mol·L-1的H2SO4溶液中,乙同学将电极放入6 mol·L-1的NaOH溶液中,如下图所示:

(1)写出甲池中负极的电极反应式:___ 。
(2)写出乙池中负极的电极反应式和总反应的离子方程式:负极___ ;总反应的离子方程式_____ 。
(3)如果甲与乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出__ 活动性更强,而乙会判断出__ 活动性更强。(填写元素符号)
(4)由此实验,可得到如下哪些正确结论__ 。
A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动性顺序已过时,已没有实用价值
D.该实验说明化学研究对象复杂,反应受条件的影响较大,因此应具体问题具体分析
(5)丙同学依据甲、乙同学的思路,设计如下实验:
将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入稀NaOH溶液中,分别形成了原电池。
①在这两个原电池中,负极分别为__ 。
A.铝片、铜片 B.铜片、铝片C.铝片、铝片 D.铜片、铜片
②写出插入浓硝酸中形成原电池的电极反应式___ 。

(1)写出甲池中负极的电极反应式:
(2)写出乙池中负极的电极反应式和总反应的离子方程式:负极
(3)如果甲与乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出
(4)由此实验,可得到如下哪些正确结论
A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动性顺序已过时,已没有实用价值
D.该实验说明化学研究对象复杂,反应受条件的影响较大,因此应具体问题具体分析
(5)丙同学依据甲、乙同学的思路,设计如下实验:
将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入稀NaOH溶液中,分别形成了原电池。
①在这两个原电池中,负极分别为
A.铝片、铜片 B.铜片、铝片C.铝片、铝片 D.铜片、铜片
②写出插入浓硝酸中形成原电池的电极反应式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】有A、B、C、D、E、F六种短周期元素,原子序数依次增大,B、C、D的阳离子、A的阴离子均具有与氖原子相同的电子层结构;A、B可形成离子化合物B2A;D的最高价氧化物既能与强酸反应,又能与强碱反应;E的原子结构示意图为: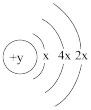 ;F的最外层电子数是电子层数的2倍。试回答下列各问题:
;F的最外层电子数是电子层数的2倍。试回答下列各问题:
(1)B元素为_________ (填元素符号)
(2)F元素位于元素周期表中第_______ 周期第______ 族
(3)化合物B2A的电子式____________________
(4)D的最高价氧化物与B的最高价氧化物对应的水化物溶液反应的离子方程式:________
(5)将C、D用导线相连浸入B的最高价氧化物对应的水化物的溶液中,形成原电池,正极的电极反应为_______________________
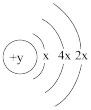 ;F的最外层电子数是电子层数的2倍。试回答下列各问题:
;F的最外层电子数是电子层数的2倍。试回答下列各问题:(1)B元素为
(2)F元素位于元素周期表中第
(3)化合物B2A的电子式
(4)D的最高价氧化物与B的最高价氧化物对应的水化物溶液反应的离子方程式:
(5)将C、D用导线相连浸入B的最高价氧化物对应的水化物的溶液中,形成原电池,正极的电极反应为
您最近一年使用:0次



