有A、B、C、D、E、F六种短周期元素,原子序数依次增大,B、C、D的阳离子、A的阴离子均具有与氖原子相同的电子层结构;A、B可形成离子化合物B2A;D的最高价氧化物既能与强酸反应,又能与强碱反应;E的原子结构示意图为: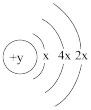 ;F的最外层电子数是电子层数的2倍。试回答下列各问题:
;F的最外层电子数是电子层数的2倍。试回答下列各问题:
(1)B元素为_________ (填元素符号)
(2)F元素位于元素周期表中第_______ 周期第______ 族
(3)化合物B2A的电子式____________________
(4)D的最高价氧化物与B的最高价氧化物对应的水化物溶液反应的离子方程式:________
(5)将C、D用导线相连浸入B的最高价氧化物对应的水化物的溶液中,形成原电池,正极的电极反应为_______________________
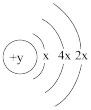 ;F的最外层电子数是电子层数的2倍。试回答下列各问题:
;F的最外层电子数是电子层数的2倍。试回答下列各问题:(1)B元素为
(2)F元素位于元素周期表中第
(3)化合物B2A的电子式
(4)D的最高价氧化物与B的最高价氧化物对应的水化物溶液反应的离子方程式:
(5)将C、D用导线相连浸入B的最高价氧化物对应的水化物的溶液中,形成原电池,正极的电极反应为
9-10高一下·江苏盐城·期末 查看更多[4]
(已下线)2010年江苏省盐城中学高一下学期期末考试化学试题(已下线)2010年江苏省南洋中学高一下学期期末考试化学试题(已下线)2010年江苏省文峰中学高一下学期期末考试化学试题新疆塔城地区塔城市2022-2023学年高二上学期11月期中考试化学试题
更新时间:2016-12-09 00:45:56
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)工业上用钛矿石(主要成分为FeTiO3,主要含FeO、Al2O3、SiO2等杂质)经过以下流程制得TiO2:

其中,步骤II发生的主要反应为:2H2SO4+ FeTiO3=TiOSO4+FeSO4+2H2O
①步骤I发生反应的离子方程式是:_____________ 、___________ 。为提高钛矿石的碱浸出速率,步骤I可采取的办法除提高碱的浓度外,还可以采取的办法有_________________ 、__________________________ (写出两种方法)。
②步骤II中加入Fe的目的是___________________ ;分离出FeSO4晶体的操作是___________ 。
③步骤III形成的TiO2·nH2O为胶体,其反应的化学方程式为____________________ 。
(2)可利用TiO2通过下述两种方法制备金属钛:
方法一:将TiO2作阴极,石墨作阳极,熔融CaO为电解液,碳块作电解槽池,电解TiO2制得钛,阳极上一定生成的气体是____________ ,可能生成的气体是__________________ 。
方法二:通过以下反应制备金属钛
①TiO2(s)+2Cl2(g) TiCl4(g)+O2(g)△H=+ 151kJ/mol
TiCl4(g)+O2(g)△H=+ 151kJ/mol
②TiCl4+2Mg 2MgCl2+Ti
2MgCl2+Ti
实际生产中,需在反应①过程中加入碳,可以顺利制得TiCl4。碳的作用除燃烧放热外,还具有的作用是_______________________________________ 。
(1)工业上用钛矿石(主要成分为FeTiO3,主要含FeO、Al2O3、SiO2等杂质)经过以下流程制得TiO2:

其中,步骤II发生的主要反应为:2H2SO4+ FeTiO3=TiOSO4+FeSO4+2H2O
①步骤I发生反应的离子方程式是:
②步骤II中加入Fe的目的是
③步骤III形成的TiO2·nH2O为胶体,其反应的化学方程式为
(2)可利用TiO2通过下述两种方法制备金属钛:
方法一:将TiO2作阴极,石墨作阳极,熔融CaO为电解液,碳块作电解槽池,电解TiO2制得钛,阳极上一定生成的气体是
方法二:通过以下反应制备金属钛
①TiO2(s)+2Cl2(g)
 TiCl4(g)+O2(g)△H=+ 151kJ/mol
TiCl4(g)+O2(g)△H=+ 151kJ/mol②TiCl4+2Mg
 2MgCl2+Ti
2MgCl2+Ti实际生产中,需在反应①过程中加入碳,可以顺利制得TiCl4。碳的作用除燃烧放热外,还具有的作用是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】物质A是由四种短周期元素组成的带结晶水的化合物,为测定其组成进行如下实验:

已知:固体D、沉淀F既能溶于酸又能溶于碱,所加试剂均过量。
请回答下列问题:
(1)组成A的元素除H、O外还有___________ (写元素符号),A的化学式为___________ 。
(2)A灼烧的化学方程式为___________ 。
(3)写出溶液E生成F的离子方程式:___________ 。
(4)溶液E中存在的阳离子是___________ (填离子符号),检验金属阳离子的具体操作是___________ 。

已知:固体D、沉淀F既能溶于酸又能溶于碱,所加试剂均过量。
请回答下列问题:
(1)组成A的元素除H、O外还有
(2)A灼烧的化学方程式为
(3)写出溶液E生成F的离子方程式:
(4)溶液E中存在的阳离子是
您最近一年使用:0次
【推荐3】七铝十二钙(12CaO·7Al2O3)是新型的超导材料和发光材料,用白云石(主要含CaCO3和MgCO3)和废铝片制备七铝十二钙的工艺如图:
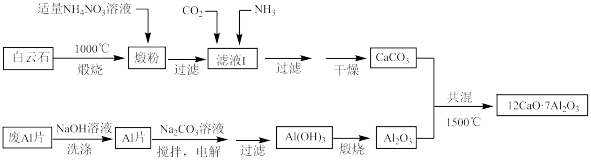
(1)煅粉主要含CaO和____ 。
(2)用NaOH溶液可除去废Al片表面的氧化膜,写出反应的离子方程式为____ 。
(3)写出1500℃共混的化学反应方程式____ 。
(4)用适量的NH4NO3溶液浸取煅粉后,恢复到25℃时镁化合物几乎不溶,若滤液I中c(Mg2+)小于5×10-6 mol·L-1,则溶液pH大于____ (Mg(OH)2的Ksp=5×10-12)。

(1)煅粉主要含CaO和
(2)用NaOH溶液可除去废Al片表面的氧化膜,写出反应的离子方程式为
(3)写出1500℃共混的化学反应方程式
(4)用适量的NH4NO3溶液浸取煅粉后,恢复到25℃时镁化合物几乎不溶,若滤液I中c(Mg2+)小于5×10-6 mol·L-1,则溶液pH大于
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某研究性学习小组欲探究原电池的形成条件,按下图所示装置进行实验
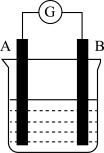
分析上述数据,回答下列问题:
(1)实验1中电流由________ 极流向_______ 极(填“A”或“B”)
(2)实验4中电子由B极流向A极,表明负极是_________ 电极(填“镁”或“铝”)
(3)实验3 表明______
A.铜在潮湿空气中不会被腐蚀 B.铜的腐蚀是自发进行的
(4)分析上表有关信息,下列说法不正确 的是____________
A.相对活泼的金属一定做负极
B.失去电子的电极是负极
C.烧杯中的液体,必须是电解质溶液
D.浸入同一电解质溶液中的两个电极,是活泼性不同的两种金属(或其中一种非金属)

| 序号 | A | B | 烧杯中的液体 | 指针是否偏转 |
| 1 | Zn | Cu | 稀硫酸 | 有 |
| 2 | Zn | Zn | 稀硫酸 | 无 |
| 3 | Cu | C | 氯化钠溶液 | 有 |
| 4 | Mg | Al | 氢氧化钠溶液 | 有 |
分析上述数据,回答下列问题:
(1)实验1中电流由
(2)实验4中电子由B极流向A极,表明负极是
(3)实验3 表明
A.铜在潮湿空气中不会被腐蚀 B.铜的腐蚀是自发进行的
(4)分析上表有关信息,下列说法
A.相对活泼的金属一定做负极
B.失去电子的电极是负极
C.烧杯中的液体,必须是电解质溶液
D.浸入同一电解质溶液中的两个电极,是活泼性不同的两种金属(或其中一种非金属)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某实验小组同学对电化学原理进行了一系列探究活动。
(1)如图为某实验小组依据氧化还原反应:(用离子方程式表示)__________________ ,设计的原电池装置,反应前,电极质量相等,一段时间后,两电极质量相差12 g,导线中通过________ mol电子。
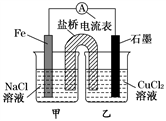
(2)用吸管吸出铁片附近溶液少许置于试管中,向其中滴加少量新制饱和氯水,写出发生反应的离子方程式___________ ,然后滴加几滴硫氰化钾溶液,溶液变红,继续滴加过量新制饱和氯水,颜色褪去,同学们对此做了多种假设,某同学的假设是:“溶液中的+3价铁被氧化为更高的价态。”如果+3价铁被氧化为FeO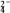 ,试写出该反应的离子方程式
,试写出该反应的离子方程式____________________ 。
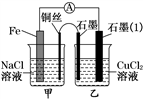
(3)如图其他条件不变,若将盐桥换成弯铜导线与石墨相连成n型,如图所示。一段时间后,在甲装置铜丝附近滴加酚酞试液,现象是溶液变红,电极反应为______________ ;乙装置中石墨(1)为________ 极(填“正”、“负”、“阴”或“阳”),乙装置中与铜丝相连石墨电极上发生的反应式为________________ 。
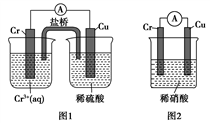
(4)观察如图所示的两个装置,图1装置中铜电极上产生大量的无色气泡,图2装置中铜电极上无气体产生,而铬电极上产生大量的有色气体。根据上述现象试推测金属铬具有的两种重要化学性质为__________________________ 、__________________________ 。
(1)如图为某实验小组依据氧化还原反应:(用离子方程式表示)

(2)用吸管吸出铁片附近溶液少许置于试管中,向其中滴加少量新制饱和氯水,写出发生反应的离子方程式
 ,试写出该反应的离子方程式
,试写出该反应的离子方程式(3)如图其他条件不变,若将盐桥换成弯铜导线与石墨相连成n型,如图所示。一段时间后,在甲装置铜丝附近滴加酚酞试液,现象是溶液变红,电极反应为

(4)观察如图所示的两个装置,图1装置中铜电极上产生大量的无色气泡,图2装置中铜电极上无气体产生,而铬电极上产生大量的有色气体。根据上述现象试推测金属铬具有的两种重要化学性质为

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6 mol·L-1的H2SO4溶液中,乙同学将电极放入6 mol·L-1的NaOH溶液中,如图所示。
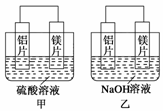
(1)写出甲中正极的电极反应式___________________ 。
(2)乙中总反应的离子方程式:________________________ 。
(3)如果甲与乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出__________ 活动性更强,而乙会判断出_____________ 活动性更强。(填写元素符号)
(4)由此实验得出的下列结论中,正确的有______________ 。

(1)写出甲中正极的电极反应式
(2)乙中总反应的离子方程式:
(3)如果甲与乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出
(4)由此实验得出的下列结论中,正确的有
| A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质 |
| B.镁的金属性不一定比铝的金属性强 |
| C.该实验说明金属活动性顺序表已过时,没有实用价值了 |
| D.该实验说明化学研究对象复杂、反应受条件影响较大,应具体问题具体分析 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】X、Y、Z、W、R、Q为前30号元素,且原子序数依次增大。X是元素周期表中原子半径最小的元素;Y元素基态原子有三个能级上有电子,且每个能级上的电子数相等;Z元素基态原子的单电子数在同周期元素基态原子中最多;W与Z同周期,第一电离能比Z的低;R与Y同主族;Q的最外层只有一个电子,其他电子层均有 个电子(n表示电子层序数)。请回答下列问题:
个电子(n表示电子层序数)。请回答下列问题:
(1)元素Q在元素周期表中的位置为_______ ,Q+的核外电子排布式为_______ 。
(2)化合物X2W2的电子式为_______ ,W的杂化方式为_______ ;ZW 的空间结构为
的空间结构为_______ 。
(3)Y、R的最高价氧化物中沸点较高的是_______ (填化学式),原因是_______ 。Y、R的最高价氧化物对应水化物酸性较强的是_______ (填化学式),通过离子方程式_______ 可以证明。
(4)原子坐标参数和晶胞参数是晶胞的两个基本参数。

①图a中原子坐标参数分别为:A(0,0,0),B( ,
, ,0),C(
,0),C( ,0,
,0, ),则D的原子坐标参数为
),则D的原子坐标参数为_______ 。
②图b为铜的晶胞,铜原子半径为Rnm,NA是阿伏加德罗常数的值,则铜晶体的密度为_______ g·cm-3(用含R、NA的式子表示)
 个电子(n表示电子层序数)。请回答下列问题:
个电子(n表示电子层序数)。请回答下列问题:(1)元素Q在元素周期表中的位置为
(2)化合物X2W2的电子式为
 的空间结构为
的空间结构为(3)Y、R的最高价氧化物中沸点较高的是
(4)原子坐标参数和晶胞参数是晶胞的两个基本参数。

①图a中原子坐标参数分别为:A(0,0,0),B(
 ,
, ,0),C(
,0),C( ,0,
,0, ),则D的原子坐标参数为
),则D的原子坐标参数为②图b为铜的晶胞,铜原子半径为Rnm,NA是阿伏加德罗常数的值,则铜晶体的密度为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】a、b、c、d、e、f、g为七种由短周期元素构成的粒子,它们都有10个电子,其结构特点如下:

其中b的离子半径大于e的离子半径;d是由极性键构成的四原子分子;试写出:
(1)写出下列粒子的电子式:
①c__________ ;②d__________ ;③e__________ ;④a__________ 。
(2)b与e相应元素的最高价氧化物对应水化物的碱性强弱比较为:__________ >__________ (用化学式表示)。
(3)用电子式表示b元素与氧形成的化合物b2O的形成过程:________________ 。

其中b的离子半径大于e的离子半径;d是由极性键构成的四原子分子;试写出:
(1)写出下列粒子的电子式:
①c
(2)b与e相应元素的最高价氧化物对应水化物的碱性强弱比较为:
(3)用电子式表示b元素与氧形成的化合物b2O的形成过程:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】短周期主族元素A、B、C、D、E的原子序数依次增大,其原子半径和原子最外层电子数之间的关系如图所示。回答下列问题:

(1)B在元素周期表中的位置为___ ;A、B组成的原子个数比为1:1的化合物的电子式为__ 。
(2)B、C的简单离子中半径较大的是___ (填离子符号),A、B、C三种元素组成的化合物中含有的化学键类型是___ 。
(3)C、E的最高价氧化物对应的水化物反应的离子方程式为__ 。
(4)下列叙述能说明E的非金属性强于D的是__ (填序号)。
a.E的简单氢化物的稳定性比D的强
b.D的氧化物对应的水化物的酸性比E的弱
c.D的单质常温下为固体,E的单质常温下为气体
d.将E的单质通入D的简单氢化物的水溶液中,有D的单质生成

(1)B在元素周期表中的位置为
(2)B、C的简单离子中半径较大的是
(3)C、E的最高价氧化物对应的水化物反应的离子方程式为
(4)下列叙述能说明E的非金属性强于D的是
a.E的简单氢化物的稳定性比D的强
b.D的氧化物对应的水化物的酸性比E的弱
c.D的单质常温下为固体,E的单质常温下为气体
d.将E的单质通入D的简单氢化物的水溶液中,有D的单质生成
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】已知A、B、C、D、E五种短周期主族元素的原子序数依次增大,A是元素周期表中原子半径最小的,C与A同主族;A与B、D、E所形成的常见化合物在常温下均呈气态,在周期表中D与E左右相邻,B的最高价氧化物的水化物与其氢化物反应生成盐,且B的核电荷数与E的最外层电子数相同。
请回答下列问题:
(1)B在元素周期表的位置为第_____ 周期,第_____ 族。
(2)C、D、E三种元素形成的简单离子的半径由大到小的顺序为______ (用离子符号表示)。
(3)A、B、E可组成一种化合物,其原子个数之比为4:1:1,该化合物的水溶液与C的最高价氧化物的水化物反应的离子方程式为____________________________________ ;
(4)B的一种氢化物分子中含有18个电子,其结构式为____________ ;C与D同主族短周期元素原子形成个数比为1:1的化合物,用电子式表示其化学键的形成过程为________________________ 。
(5)BE3在常温下是一种淡黄色的液体,遇水即发生水解可生成一种具有漂白性的物质和一种核外电子总数为10的气体,写出该反应的化学方程式___________________________ ;
(6)下列事实能证明D与E非金属性强弱的是_____________________ (选填字母序号)。
A.常温下,D的单质呈固态,E的单质呈气态
B.E的氢化物的稳定性强于D的氢化物
C.E与D形成的化合物中,D呈正价
D.E的氢化物的沸点高于D的氢化物
(7)已知D、E两种元素形成的化合物H,H结构与过氧化氢相似,属于______________ (填“离子”或“共价”)化合物。5.4 g的H中含有的共用电子对数目为________ 。
请回答下列问题:
(1)B在元素周期表的位置为第
(2)C、D、E三种元素形成的简单离子的半径由大到小的顺序为
(3)A、B、E可组成一种化合物,其原子个数之比为4:1:1,该化合物的水溶液与C的最高价氧化物的水化物反应的离子方程式为
(4)B的一种氢化物分子中含有18个电子,其结构式为
(5)BE3在常温下是一种淡黄色的液体,遇水即发生水解可生成一种具有漂白性的物质和一种核外电子总数为10的气体,写出该反应的化学方程式
(6)下列事实能证明D与E非金属性强弱的是
A.常温下,D的单质呈固态,E的单质呈气态
B.E的氢化物的稳定性强于D的氢化物
C.E与D形成的化合物中,D呈正价
D.E的氢化物的沸点高于D的氢化物
(7)已知D、E两种元素形成的化合物H,H结构与过氧化氢相似,属于
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】有X、Y、 Z、M、R、Q六种短周期主族元素,部分信息如下表所示:
请回答下列问题:
(1)R在元素周期表中的位置是________ 。
(2)根据表中数据推测,Y的原子半径的最小范围是________ 。
(3) Z、M、Q的简单离子的离子半径由大到小的顺序为_______ (用元素符号表示)。
(4)Y与R相比,非金属性较强的是______ (用元素符号表示),下列事实能证明这一结论的是_____ (选填字母序号)
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性:XR>YX4
c.Y与R形成的化合物中Y呈正价
(5)写出R的单质与Z的最高价氧化物对应水化物的水溶液反应的离子方程式:__________ 。
| X | Y | Z | M | R | Q | |
| 原子半径/nm | 0.186 | 0.074 | 0.099 | 0.160 | ||
| 主要化合价 | -4,+4 | -2 | -1,+7 | |||
| 其它信息 | 某种核素无中子 | 常用的半导体材料 | 短周期主族元素中原子半径最大 | 次外层电子数是最外层电子数的4倍 |
请回答下列问题:
(1)R在元素周期表中的位置是
(2)根据表中数据推测,Y的原子半径的最小范围是
(3) Z、M、Q的简单离子的离子半径由大到小的顺序为
(4)Y与R相比,非金属性较强的是
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性:XR>YX4
c.Y与R形成的化合物中Y呈正价
(5)写出R的单质与Z的最高价氧化物对应水化物的水溶液反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】有A、B、C、D、E五种元素,它们原子的核电荷数依次递增且均小于18;A原子核内仅有1个质子;B原子的电子总数与C原子的最外层电子数相等; C原子有两个电子层,最外层电子数是次外层电子数的3倍;D元素的最外层电子数是其电子层数的三分之一。E的单质是黄绿色气体且有毒。
(1)写出A分别与B、C所形成化合物的化学式:________ ,_________ 。
(2)分别写出C和D的原子结构示意图:_______________ ,_________ 。
(3)写出C、D、E所形成的化合物的电离方程式:_________________________ 。
(4)写出E的单质与A、C、D三元素所形成的化合物反应的化学方程式,若是氧化还原反应,请用双线桥标出电子转移的数目和方向:___________________ 。
(1)写出A分别与B、C所形成化合物的化学式:
(2)分别写出C和D的原子结构示意图:
(3)写出C、D、E所形成的化合物的电离方程式:
(4)写出E的单质与A、C、D三元素所形成的化合物反应的化学方程式,若是氧化还原反应,请用双线桥标出电子转移的数目和方向:
您最近一年使用:0次



