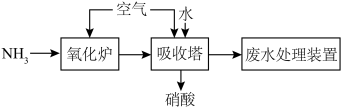
HNO3是极其重要的化工原料,在工业、农业、医药、军事等领域有着广泛的应用,现代工业上常用氨催化氧化制硝酸的流程示意图如下:________________________ 。
(2)工业上常用碱液来吸收NOx,有关的化学反应为:
①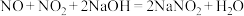 ;
;
② 。
。
现有一定条件下0.2molNO2和0.1molNO的混合气体恰好被200mLNaOH溶液完全吸收,则NaOH溶液的物质的量浓度为____________ mol/L。
(3)已知氨氮废水中氮元素多以 和NH3•H2O的形式存在,加入NaClO可将废水中的NH3•H2O转化为无污染气体,该反应的化学方程式为
和NH3•H2O的形式存在,加入NaClO可将废水中的NH3•H2O转化为无污染气体,该反应的化学方程式为_______________________________________________ 。
(4)《本草纲目拾遗》记载“强水性最烈,能蚀五金”,请写出稀强水与铜反应的离子方程式:__________________________ 。
(5)长期存放的浓硝酸呈黄色是因为其分解生成的_____________ 溶于硝酸中,实验室常将浓硝酸保存在
__________ 试剂瓶中,并放在__________ 处。
(2)工业上常用碱液来吸收NOx,有关的化学反应为:
①
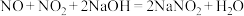 ;
;②
 。
。现有一定条件下0.2molNO2和0.1molNO的混合气体恰好被200mLNaOH溶液完全吸收,则NaOH溶液的物质的量浓度为
(3)已知氨氮废水中氮元素多以
 和NH3•H2O的形式存在,加入NaClO可将废水中的NH3•H2O转化为无污染气体,该反应的化学方程式为
和NH3•H2O的形式存在,加入NaClO可将废水中的NH3•H2O转化为无污染气体,该反应的化学方程式为(4)《本草纲目拾遗》记载“强水性最烈,能蚀五金”,请写出稀强水与铜反应的离子方程式:
(5)长期存放的浓硝酸呈黄色是因为其分解生成的
更新时间:2023/09/06 13:06:14
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】氧化还原型有机反应在生产、生活中有广泛应用。
(1)酒精仪中酸性重铬酸钾(稀硫酸酸化)可将乙醇氧化成乙酸,本身被还原成Cr3+。写出该反应的离子方程式:_______ ;在该反应中还原剂是_______ (填化学式)。氧化23g乙醇时转移电子的物质的量为_______ 。
(2)向酸性高锰酸钾溶液中通入乙烯,溶液褪色。配平下列反应方程式:_______ 。
_______KMnO4+_______H2SO4+_______CH2=CH2 _______K2SO4+_______MnSO4+_______CO2↑+_______
_______K2SO4+_______MnSO4+_______CO2↑+_______
(3)乙烯与双氧水在一定条件下反应生成HOCH2CH2OH,化学方程式为CH2=CH2+H2O2 HOCH2CH2OH,这个反应既是加成反应,又是氧化反应。判断为“氧化反应”的依据是
HOCH2CH2OH,这个反应既是加成反应,又是氧化反应。判断为“氧化反应”的依据是_______ 。
(4)在保温瓶胆上镀银,常用葡萄糖作还原剂。发生反应如下HOCH2(CHOH)4CHO+2Ag(NH3)2OH HOCH2(CHOH)4COONH4+2Ag↓+3NH3+H2O。镀银时,假设平均每个瓶胆上消耗0.108g银,则10000个这样的瓶胆最少需要消耗葡萄糖的质量为
HOCH2(CHOH)4COONH4+2Ag↓+3NH3+H2O。镀银时,假设平均每个瓶胆上消耗0.108g银,则10000个这样的瓶胆最少需要消耗葡萄糖的质量为_______ kg。
(1)酒精仪中酸性重铬酸钾(稀硫酸酸化)可将乙醇氧化成乙酸,本身被还原成Cr3+。写出该反应的离子方程式:
(2)向酸性高锰酸钾溶液中通入乙烯,溶液褪色。配平下列反应方程式:
_______KMnO4+_______H2SO4+_______CH2=CH2
 _______K2SO4+_______MnSO4+_______CO2↑+_______
_______K2SO4+_______MnSO4+_______CO2↑+_______(3)乙烯与双氧水在一定条件下反应生成HOCH2CH2OH,化学方程式为CH2=CH2+H2O2
 HOCH2CH2OH,这个反应既是加成反应,又是氧化反应。判断为“氧化反应”的依据是
HOCH2CH2OH,这个反应既是加成反应,又是氧化反应。判断为“氧化反应”的依据是(4)在保温瓶胆上镀银,常用葡萄糖作还原剂。发生反应如下HOCH2(CHOH)4CHO+2Ag(NH3)2OH
 HOCH2(CHOH)4COONH4+2Ag↓+3NH3+H2O。镀银时,假设平均每个瓶胆上消耗0.108g银,则10000个这样的瓶胆最少需要消耗葡萄糖的质量为
HOCH2(CHOH)4COONH4+2Ag↓+3NH3+H2O。镀银时,假设平均每个瓶胆上消耗0.108g银,则10000个这样的瓶胆最少需要消耗葡萄糖的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在工业上次磷酸(H3PO2)常用于化学镀银,发生的反应如下:____Ag++___ H3PO2+___H2O→____Ag↓+____ H3PO4+___H+
请回答下列问题:
(1)H3PO2中,P元素的化合价为_____ ;该反应中,H3PO2作_____ (填“氧化剂”或“还原剂”)。
(2)上述离子方程式中,各物质的化学计量数分别为___________ 。
(3)若反应中生成10.8g Ag,则转移的电子数为__________ 。
(4)H3PO2是一元中强酸,写出其与足量NaOH 溶液反应的离子方程式:________ 。
请回答下列问题:
(1)H3PO2中,P元素的化合价为
(2)上述离子方程式中,各物质的化学计量数分别为
(3)若反应中生成10.8g Ag,则转移的电子数为
(4)H3PO2是一元中强酸,写出其与足量NaOH 溶液反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】有下列物质:①硫酸 ② 溶液 ③
溶液 ③ ④小苏打 ⑤纯碱 ⑥
④小苏打 ⑤纯碱 ⑥ ⑦明矾。回答下列问题:
⑦明矾。回答下列问题:
(1)将上述物质按下图进行分类。
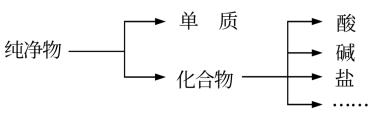
图中所示所属的分类方法为_______ 。
(2)纯碱是重要的化工原料之一,写出其在水中的电离方程式:_______ 。
(3)明矾 [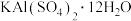 ]是常见的净水剂,属于
]是常见的净水剂,属于_______ (填“酸”“碱”或“盐”),实验室利用明矾制备 的离子方程式为
的离子方程式为_______ 。
(4)取 溶液做导电性实验,往烧杯中滴加
溶液做导电性实验,往烧杯中滴加 稀硫酸。装置如图1,测得溶液电导率如图2所示。
稀硫酸。装置如图1,测得溶液电导率如图2所示。

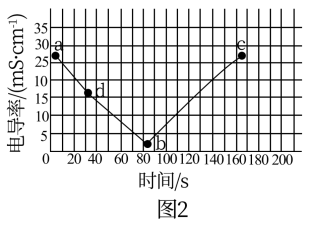
①由 过程中,可观察到的现象有
过程中,可观察到的现象有_______ ,发生反应的离子方程式为_______ 。
②b点时加入 溶液的体积为
溶液的体积为_______  。
。
 溶液 ③
溶液 ③ ④小苏打 ⑤纯碱 ⑥
④小苏打 ⑤纯碱 ⑥ ⑦明矾。回答下列问题:
⑦明矾。回答下列问题:(1)将上述物质按下图进行分类。

图中所示所属的分类方法为
(2)纯碱是重要的化工原料之一,写出其在水中的电离方程式:
(3)明矾 [
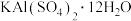 ]是常见的净水剂,属于
]是常见的净水剂,属于 的离子方程式为
的离子方程式为(4)取
 溶液做导电性实验,往烧杯中滴加
溶液做导电性实验,往烧杯中滴加 稀硫酸。装置如图1,测得溶液电导率如图2所示。
稀硫酸。装置如图1,测得溶液电导率如图2所示。

①由
 过程中,可观察到的现象有
过程中,可观察到的现象有②b点时加入
 溶液的体积为
溶液的体积为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
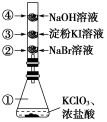
【推荐1】已知常温下KClO3与浓盐酸反应放出氯气,现按如图进行卤素的性质实验。玻璃管内装有分别滴加过不同溶液的白色棉球,反应一段时间后①②③④处的颜色分别为黄绿色、橙色、蓝色、白色。
(1)②处颜色变化的原因是什么_____ ?写出离子方程式。可得出的结论是什么_____ ?
(2)③处变蓝的原因是什么_____ ?写出可能的离子方程式,可能得出的结论是什么_____ ?
(3)通过该实验现象可得出的结论是什么_____ ?
(1)②处颜色变化的原因是什么
(2)③处变蓝的原因是什么
(3)通过该实验现象可得出的结论是什么
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知实验室制取氯气的反应原理为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,据此回答下列问题:
MnCl2+Cl2↑+2H2O,据此回答下列问题:
(1)氧化剂是___________ (填写化学式);还原剂是___________ (填写化学式);氧化产物是___________ (填化学式),HCl在反应中体现的性质___________ 。氧化剂和还原剂个数比是 ___________ 。
(2)该实验室制取氯气反应的离子方程式为___________ 。
(3)用单线桥法表示电子转移的方向和数目:KClO3+6HCl(浓) KCl+3Cl2↑+3H2O
KCl+3Cl2↑+3H2O ___________
(4)请配平反应
①___________ ____H++____ +____
+____ = ____Cr3++____
= ____Cr3++____ +____H2O
+____H2O
②___________ ____Fe2++____H++____ =____Fe3++____N2O↑+____H2O
=____Fe3++____N2O↑+____H2O
 MnCl2+Cl2↑+2H2O,据此回答下列问题:
MnCl2+Cl2↑+2H2O,据此回答下列问题:(1)氧化剂是
(2)该实验室制取氯气反应的离子方程式为
(3)用单线桥法表示电子转移的方向和数目:KClO3+6HCl(浓)
 KCl+3Cl2↑+3H2O
KCl+3Cl2↑+3H2O (4)请配平反应
①
 +____
+____ = ____Cr3++____
= ____Cr3++____ +____H2O
+____H2O②
 =____Fe3++____N2O↑+____H2O
=____Fe3++____N2O↑+____H2O
您最近一年使用:0次
【推荐3】KClO3和浓盐酸在一定温度下发生如(1)的反应:
(1)请配平方程式,并用双线桥表示得失电子情况:
_____ KClO3+______ HCl(浓)=______ KCl+______ ClO2↑+Cl2↑+______ H2O
_______________________________________________________________
(2)氧化剂是_________ ,还原产物是_________ (写化学式)。
(3)产生0.1molCl2时,转移电子的物质的量为__________ mol。
(1)请配平方程式,并用双线桥表示得失电子情况:
(2)氧化剂是
(3)产生0.1molCl2时,转移电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】工业制备原理

写出上述转化的化学方程式,并指出含氮物质发生的是氧化反应还是还原反应
(1)_________________________ ,N2发生____ 反应。
(2)_________________________ ,NH3发生____ 反应。
(3)_________________________ ,NO发生____ 反应。
(4)_________________________ ,NO2既发生____ 反应,又发生____ 反应。

写出上述转化的化学方程式,并指出含氮物质发生的是氧化反应还是还原反应
(1)
(2)
(3)
(4)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.NH3与NO2是常见的氮的化合物,研究它们的综合利用有重要意义。
(1)汽车尾气中含有污染性气体NO2,NO2产生的环境问题有_______ (填一种)。
(2)热电厂通常用NH3消除燃煤烟气中产生的NO2,写出该反应的化学方程式________________ 。
(3)氨气与氯化氢气体混合的现象是________________ ,该反应的实际应用为________________________ 。(填一种)
(4)若将少量氨气与过量氯气混合,则生成一种酸性气体和另一种化合物A,A中所有原子均满足8电子稳定结构,试写出A的化学式________ ,A在一定条件下能与水反应,并可用于饮用水的消毒,试写出A与水反应的化学方程式________________________ 。
(1)汽车尾气中含有污染性气体NO2,NO2产生的环境问题有
(2)热电厂通常用NH3消除燃煤烟气中产生的NO2,写出该反应的化学方程式
(3)氨气与氯化氢气体混合的现象是
(4)若将少量氨气与过量氯气混合,则生成一种酸性气体和另一种化合物A,A中所有原子均满足8电子稳定结构,试写出A的化学式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知氮元素是地球大气中含量最多的元素,请完成下列有关问题:
(1)写出N2的电子式:__ 。
(2)将空气中的氮气转化为氮的化合物的过程称为固氮,则下列属于固氮过程的是__ (填字母)。
A.NH3经过催化氧化生成NO
B.NH3和HNO3反应生成NH4NO3
C.N2和H2在一定条件下反应生成NH3
D.雷雨闪电时空气中的N2和O2化合生成NO
(3)如图是实验室制取氨气的装置和选用试剂,其中错误的是__ (填字母)。
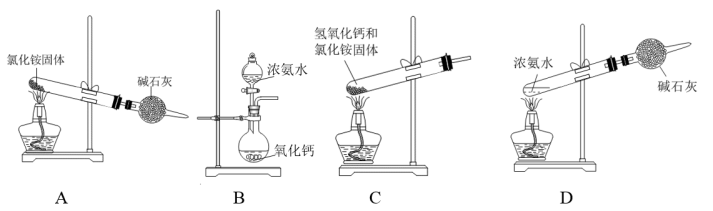
选取了正确的制备装置后,若想收集一试管氨气,可用___ 排空气法。
(4)NH4HCO3是常用的铵态氮肥,在施用时若受热会释放出氨气而降低肥效。检验其中 的方法是将固体溶于水配制浓溶液,加入浓
的方法是将固体溶于水配制浓溶液,加入浓__ 溶液、加热,再用__ 试纸检验产生的气体,若试纸变蓝则表明含有 。
。
(1)写出N2的电子式:
(2)将空气中的氮气转化为氮的化合物的过程称为固氮,则下列属于固氮过程的是
A.NH3经过催化氧化生成NO
B.NH3和HNO3反应生成NH4NO3
C.N2和H2在一定条件下反应生成NH3
D.雷雨闪电时空气中的N2和O2化合生成NO
(3)如图是实验室制取氨气的装置和选用试剂,其中错误的是

选取了正确的制备装置后,若想收集一试管氨气,可用
(4)NH4HCO3是常用的铵态氮肥,在施用时若受热会释放出氨气而降低肥效。检验其中
 的方法是将固体溶于水配制浓溶液,加入浓
的方法是将固体溶于水配制浓溶液,加入浓 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料.其中一个反应为3FeS2+8O2=6SO2+Fe3O4,氧化产物为____________ ,若有3mol FeS2参加反应,转移电子数为____________ .
(2)与明矾相似,硫酸铁也可用作净水剂,其原理为___________ (用离子方程表示)
(3)在热的稀硫酸溶液中溶解一定量的FeSO4后,再加入足量的KNO3溶液,可使其中的Fe2+全部转化成Fe3+,并有气体逸出,请写出相应的离子方程式___________________________
(2)与明矾相似,硫酸铁也可用作净水剂,其原理为
(3)在热的稀硫酸溶液中溶解一定量的FeSO4后,再加入足量的KNO3溶液,可使其中的Fe2+全部转化成Fe3+,并有气体逸出,请写出相应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】非金属单质A经下图所示的过程可转化为含氧酸D,已知D为强酸。请回答下列问题.

(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体;
①D的化学式为______________ ;
②在工业生产中,B气体大量排放,被雨水吸收后形成的______________ 会污染环境;
③98.3%的D溶液是常见的气体干燥剂,但它不能干燥 和
和 ,原因是
,原因是______________ ;
(2)若A在常温下为气体,C是红棕色的气体;
①A、C的化学式分别为_________ 、___________ ;
②D的浓溶液在常温下可与铜反应并生成C气体,该反应的化学方程式为________ ,该反应_______ (填“属于”或“不属于”)氧化还原反应;
③工业上利用氨制备D,写出氨被催化氧化生成B气体的化学方程式:____________ 。

(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体;
①D的化学式为
②在工业生产中,B气体大量排放,被雨水吸收后形成的
③98.3%的D溶液是常见的气体干燥剂,但它不能干燥
 和
和 ,原因是
,原因是(2)若A在常温下为气体,C是红棕色的气体;
①A、C的化学式分别为
②D的浓溶液在常温下可与铜反应并生成C气体,该反应的化学方程式为
③工业上利用氨制备D,写出氨被催化氧化生成B气体的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】研究氮及其化合物性质,可以有效改善人类的生存环境。氮元素化合价与物质类别关系图如下。

(1)在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,写出反应的化学方程式:___________ 。
(2)在加热条件下,物质C的浓溶液与碳单质反应,写出反应的化学方程式:___________ 。
(3)实验室中,检验溶液中含有 的操作方法是:
的操作方法是:___________ 。
(4)物质B为红棕色气体,写出该物质与水反应的离子方程式:___________ 。
(5)Cu与一定浓度的硝酸溶液反应生成NO时的离子反应方程式:___________ 。

(1)在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,写出反应的化学方程式:
(2)在加热条件下,物质C的浓溶液与碳单质反应,写出反应的化学方程式:
(3)实验室中,检验溶液中含有
 的操作方法是:
的操作方法是:(4)物质B为红棕色气体,写出该物质与水反应的离子方程式:
(5)Cu与一定浓度的硝酸溶液反应生成NO时的离子反应方程式:
您最近一年使用:0次



