某反应A(g)+B(g)→C(g)+D(g) 的速率方程为v=kcm(A)·cn(B), 其中k是反应速率常数,受温度、催化剂的影响。其半衰期(当剩余反应物恰好是起始的一半时所需的时间)为 0.8/k。改变反应物浓度时,反应的瞬时速率如表所示;
下列说法不正确的是
| c(A)/(mol·L-1) | 0.25 | 0.50 | 1.00 | 0.50 | 1.00 | c1 |
| c(B)/(mol·L-1) | 0.050 | 0.050 | 0.100 | 0.100 | 0.200 | c2 |
| v/(10-3mol·L-1·min-1) | 1.6 | 3.2 | v1 | 3.2 | v2 | 4.8 |
| A.上述表格中的c1=0.75、v1=6.4 |
| B.该反应的速率常数k=6.4×10-3min-1 |
| C.在过量的B 存在时,反应掉75%的A 所需的时间是250 min |
| D.升温、加入催化剂、缩小容积(加压),均可使k增大导致反应的瞬时速率加快 |
更新时间:2023-09-08 21:31:32
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】PCl3和PCl5都是重要的化工原料。将PCl3(g)和Cl2(g)充入2L的恒容密闭容器中,在一定条件下发生反应PCl3(g)+Cl2(g) PCl5(g),△H<0并于10min时达到平衡。有关数据如下:下列判断正确的是
PCl5(g),△H<0并于10min时达到平衡。有关数据如下:下列判断正确的是
 PCl5(g),△H<0并于10min时达到平衡。有关数据如下:下列判断正确的是
PCl5(g),△H<0并于10min时达到平衡。有关数据如下:下列判断正确的是| PCl3(g) | Cl2(g) | PCl5(g) | |
| 初始浓度/(mol•L-1) | 2.0 | 1.0 | 0 |
| 平衡浓度/(mol•L-1) | c1 | c2 | 0.4 |
| A.10 min内,v(Cl2)=0.02 mol/( L•min) |
| B.升高温度,反应的平衡常数增大 |
| C.反应达到平衡时容器内的压强与初始时容器的压强之比为1:2 |
| D.平衡后移走2.0 mol PCl3和1.0 mol Cl2,相同条件下再达平衡时,c(PCl5)<0.2 mol•L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
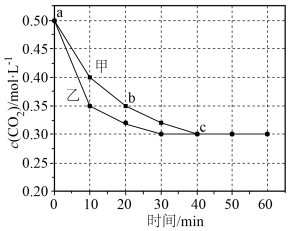
【推荐2】在恒温恒容条件下,发生反应: ,测得
,测得 与时间关系如图,下列叙述错误的是
与时间关系如图,下列叙述错误的是
 ,测得
,测得 与时间关系如图,下列叙述错误的是
与时间关系如图,下列叙述错误的是
| A.a点逆反应速率小于c点正反应速率 |
| B.其他条件不变,相对甲曲线,乙曲线加入催化剂 |
C.不同时刻存在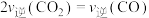 |
D.b~c段CO平均速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】在容积为1 L的恒容密闭容器中充入CO(g)和H2O(g),发生反应:CO(g) + H2O(g) CO2(g) + H2(g) ΔH<0,所得实验数据如下表:
CO2(g) + H2(g) ΔH<0,所得实验数据如下表:
下列说法正确的是
 CO2(g) + H2(g) ΔH<0,所得实验数据如下表:
CO2(g) + H2(g) ΔH<0,所得实验数据如下表:| 实验 编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
| n(CO) | n(H2O) | n(CO2) | ||
| ① | 700 | 0.40 | 0.10 | 0.090 |
| ② | 800 | 0.10 | 0.40 | 0.080 |
| ③ | 800 | 0.20 | 0.30 | a |
| ④ | 900 | 0.10 | 0.15 | b |
下列说法正确的是
| A.实验①中,若5 min时测得n (CO2) =0.050 mol,则0至5 min时间内,用H2表示的平均反应速率υ (H2) = 5.0×10-2 mol/(L·min) |
| B.实验②中,该条件下反应的平衡常数K =2.0 |
| C.实验③中,达到平衡时,CO的转化率为60% |
| D.实验④中,达到平衡时,b>0.060 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列实验过程不能达到实验目的的是
| 选项 | 实验目的 | 实验过程 |
| A | 排除碱式滴定管尖嘴处气泡 | 使尖嘴垂直向下,轻轻挤压橡胶管中玻璃球,使部分液体流出 |
| B | 配制FeCl3溶液 | 将FeCl3溶于较浓的盐酸中,然后加水稀释 |
| C | 探究盐类的水解反应为吸热反应 | 向盛有Na2CO3溶液的试管中滴入酚酞,然后微热,观察溶液颜色变化 |
| D | 探究浓度对反应速率的影响 | 向分别盛有2 mL0.1 mol/L、2 mL0.2 mol/L H2C2O4溶液的两支试管中同时加入4 mL0.01 mol/ L酸性KMnO4溶液,观察实验现象 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】恒温恒容的密闭容器中,在某催化剂表面上发生氨的分解反应: ,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下列说法不正确的是
,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下列说法不正确的是
 ,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下列说法不正确的是
,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下列说法不正确的是| 编号 | 时间/min c(NH3)/(10-3mol/L) 表面积/cm2 | 0 | 20 | 40 | 60 | 80 |
| ① | a | 2.40 | 2.00 | 1.60 | 1.20 | 0.80 |
| ② | a | 1.20 | 0.80 | 0.40 | x | |
| ③ | 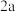 | 2.40 | 1.60 | 0.80 | 0.40 | 0.40 |
A.相同条件下,增加 的浓度,反应速率增大 的浓度,反应速率增大 |
B.实验①, , ,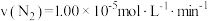 |
C.实验②, 时处于平衡状态, 时处于平衡状态, |
| D.相同条件下,增加催化剂的表面积,反应速率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】探究 2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+l0CO2↑+8H2O 反应速率的影响因素,有关实验数据如下表所示:
下列说法不正确的是
| 编号 | 温度℃ | 催化剂(g) | 酸性KMnO4溶液 | H2C2O4溶液 | KMnO4溶液褪色平均时间(min) | ||
| 体积(mL) | 浓度(mol/L) | 体积(mL) | 浓度(mol/L) | ||||
| 1 | 25 | 0.5 | 4 | 0.1 | 8 | 0.2 | 12.7 |
| 2 | 80 | 0.5 | 4 | 0.1 | 8 | 0.2 | a |
| 3 | 25 | 0.5 | 4 | 0.01 | 8 | 0.2 | 6.7 |
| 4 | 25 | 0 | 4 | 0.01 | 8 | 0.2 | b |
| A.a<12.7,b>6.7 |
| B.可通过比较收集相同体积CO2所消耗的时间来判断反应速率快慢 |
| C.用H2C2O4表示该反应速率,v(实验1)约为6.6×l0-3 mol·L-1·min-1 |
| D.用KMnO4表示该反应速率,v(实验3)>v(实验1) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】将等量的NO2气体盛装在两个连通的烧瓶里,然后用弹簧夹夹住橡皮管,把烧瓶A放入热水里,把烧瓶B放入冰水里,如图所示。一段时间后发现,A烧瓶内气体颜色变深,B烧瓶内气体颜色变浅。下列说法错误的是
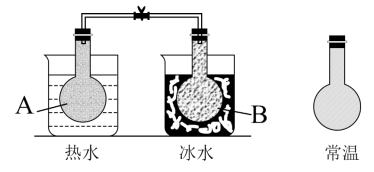

A.两烧瓶中均发生了反应:2NO2(g) N2O4(g) △H<0 N2O4(g) △H<0 |
| B.上述过程中,B烧瓶内正反应速率增大,逆反应速率减小,所以平衡正向移动 |
| C.上述过程中,A、B烧瓶内气体密度均保持不变 |
| D.由该实验可知,放热反应中,温度对逆反应速率影响更大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在有氧条件下,新型催化剂M能催化NH3与NOx反应生成N2。将-定比例的O2、NH3和NOx的混合气体,匀速通入装有催化剂M的反应器中反应,模拟NOx的去除。在不同温度下,反应相同时间,测得NOx的去除率如图所示,下列说法不合理的是( )
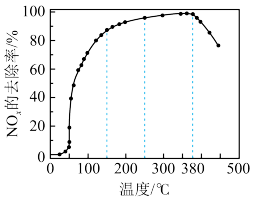

| A.低于50℃时,NOx去除率较低可能是因为反应速率较慢 |
| B.50~150℃时,NOx去除率迅速上升,只是因为温度升高导致反应速率加快引起的 |
| C.380℃以上,可能发生氨气的催化氧化反应,导致NOx的去除率降低 |
| D.无法由图象得出NH3与NOx反应生成N2的△H的正负 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】南京理工大学的科研团队发现了一种烷基锆试剂(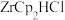 )能够用于可见光照射促进有机结构的连接,其典型反应机理推测如图。
)能够用于可见光照射促进有机结构的连接,其典型反应机理推测如图。
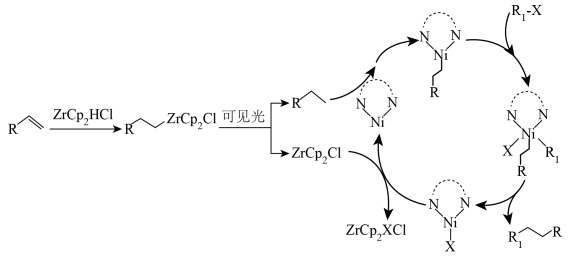
下列说法正确的是
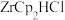 )能够用于可见光照射促进有机结构的连接,其典型反应机理推测如图。
)能够用于可见光照射促进有机结构的连接,其典型反应机理推测如图。
下列说法正确的是
| A.该反应机理的含镍物质中Ni的配位数为2、3、4 |
| B.该反应机理中只存在极性键的断裂和非极性键的生成 |
C.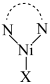 为该反应的催化剂 为该反应的催化剂 |
D.根据该反应机理,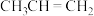 和 和 可以连接 可以连接 |
您最近一年使用:0次


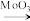 2HCHO↑+CH2 =CH2↑+2H2O
2HCHO↑+CH2 =CH2↑+2H2O

