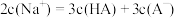乙二胺四乙酸(EDTA)可与金属离子形成稳定的配合物。常用EDTA测定水中钙含量(EDTA与钙反应时物质的量之比均为1∶1)。基本步骤如下:
①EDTA标定:取10.00 mL 0.1 标准
标准 溶液,加入3滴甲基橙溶液作指示剂,用已配制好的EDTA溶液滴定至终点,消耗EDTA溶液
溶液,加入3滴甲基橙溶液作指示剂,用已配制好的EDTA溶液滴定至终点,消耗EDTA溶液 mL。
mL。
②钙提取:取一定质量的有机物,并用酸性 溶液氧化,再经萃取、反萃取将金属转移到水中,得到提取液。加入掩蔽剂(掩蔽除钙之外的金属)并将pH调至11.3。
溶液氧化,再经萃取、反萃取将金属转移到水中,得到提取液。加入掩蔽剂(掩蔽除钙之外的金属)并将pH调至11.3。
③EDTA滴定:取20.00mL提取液,加入指示剂钙黄绿素(钙与钙黄绿素生成能发出绿色荧光的配合物),在黑色背景下用标定后的EDTA溶液滴定至终点,消耗EDTA溶液 mL。
mL。
根据上述实验原理,下列说法错误的是
①EDTA标定:取10.00 mL 0.1
 标准
标准 溶液,加入3滴甲基橙溶液作指示剂,用已配制好的EDTA溶液滴定至终点,消耗EDTA溶液
溶液,加入3滴甲基橙溶液作指示剂,用已配制好的EDTA溶液滴定至终点,消耗EDTA溶液 mL。
mL。②钙提取:取一定质量的有机物,并用酸性
 溶液氧化,再经萃取、反萃取将金属转移到水中,得到提取液。加入掩蔽剂(掩蔽除钙之外的金属)并将pH调至11.3。
溶液氧化,再经萃取、反萃取将金属转移到水中,得到提取液。加入掩蔽剂(掩蔽除钙之外的金属)并将pH调至11.3。③EDTA滴定:取20.00mL提取液,加入指示剂钙黄绿素(钙与钙黄绿素生成能发出绿色荧光的配合物),在黑色背景下用标定后的EDTA溶液滴定至终点,消耗EDTA溶液
 mL。
mL。根据上述实验原理,下列说法错误的是
| A.若对提取液的其他金属不进行掩蔽,测定的钙含量结果偏高 |
| B.EDTA标定时,滴定管尖嘴开始有气泡终点无气泡,会使钙含量测定结果偏高 |
| C.EDTA滴定若选用其他物质作指示剂,提取液的pH可能发生变化 |
| D.pH为11.3时,EDTA与钙的配合能力强于钙黄绿素与钙的配合能力 |
更新时间:2023-10-11 15:11:30
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】常温下,用0.1 mol/L NaOH溶液滴定10 mL 0.1 mol/L H2X溶液,溶液的pH与NaOH溶液的体积关系如图所示。下列说法正确的是


| A.水电离出来的c(OH -):D点<B点 |
| B.B点:c( HX -)> c (H+)> c (X2-)> c (H2X) |
| C.C点存在关系式:c (Na+) = c (HX-)+ 2c (X2-)- c(H+) |
D.A点溶液中加入少量水: 减小 减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
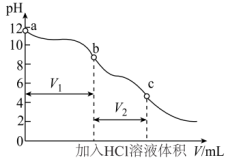
【推荐2】可用酚酞和甲基橙双指示剂法测定部分变质的烧碱中 的含量。先将部分变质的烧碱配制成一定浓度溶液并加入一种指示剂,用一定浓度的HCl溶液滴定至变色后,再加入另一种指示剂,继续用该HCl溶液滴定至变色,分别记录两个变色点加入HCl溶液体积进行计算。滴定过程中溶液pH的变化如图所示。下列说法错误的是
的含量。先将部分变质的烧碱配制成一定浓度溶液并加入一种指示剂,用一定浓度的HCl溶液滴定至变色后,再加入另一种指示剂,继续用该HCl溶液滴定至变色,分别记录两个变色点加入HCl溶液体积进行计算。滴定过程中溶液pH的变化如图所示。下列说法错误的是
 的含量。先将部分变质的烧碱配制成一定浓度溶液并加入一种指示剂,用一定浓度的HCl溶液滴定至变色后,再加入另一种指示剂,继续用该HCl溶液滴定至变色,分别记录两个变色点加入HCl溶液体积进行计算。滴定过程中溶液pH的变化如图所示。下列说法错误的是
的含量。先将部分变质的烧碱配制成一定浓度溶液并加入一种指示剂,用一定浓度的HCl溶液滴定至变色后,再加入另一种指示剂,继续用该HCl溶液滴定至变色,分别记录两个变色点加入HCl溶液体积进行计算。滴定过程中溶液pH的变化如图所示。下列说法错误的是
| A.指示剂的添加顺序为先加酚酞,后加甲基橙 |
B.b点时溶液中的溶质主要为NaCl和 |
C.若 ,则a点溶液中存在 ,则a点溶液中存在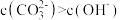 |
D.原固体混合物中碳酸钠的质量分数表示为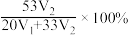 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验操作能使实验结果偏低的是
| A.用蒸馏水润湿的pH试纸所测定的某酸溶液的pH |
| B.用容量瓶配制溶液,定容后摇匀液面下降,再加蒸馏水至刻度线所配制的溶液浓度 |
| C.用仰视量筒刻度量取的一定量浓硫酸所配制的0.1mol·L-1H2SO4溶液的浓度 |
| D.用待测液润洗的锥形瓶进行中和滴定所测定的待测液浓度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
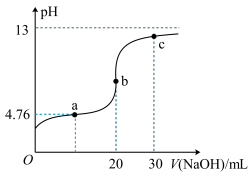
【推荐2】取 醋酸溶液加入锥形瓶中,加入1-2滴指示剂,用等浓度的
醋酸溶液加入锥形瓶中,加入1-2滴指示剂,用等浓度的 溶液进行滴定,滴定曲线如图所示,下列说法正确的是
溶液进行滴定,滴定曲线如图所示,下列说法正确的是

 醋酸溶液加入锥形瓶中,加入1-2滴指示剂,用等浓度的
醋酸溶液加入锥形瓶中,加入1-2滴指示剂,用等浓度的 溶液进行滴定,滴定曲线如图所示,下列说法正确的是
溶液进行滴定,滴定曲线如图所示,下列说法正确的是
A. 在a的左侧 在a的左侧 |
| B.A点水的电离程度最大 |
| C.指示剂可以是酚酞或甲基橙 |
D.滴定终点时, |
您最近一年使用:0次

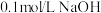 溶液滴定
溶液滴定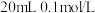 一元弱酸
一元弱酸 溶液,滴定曲线如图所示。已知:
溶液,滴定曲线如图所示。已知: ,下列说法正确的是
,下列说法正确的是