现有下列3个氧化还原反应:
① ;
;
②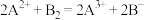 ;
;
③ ,
,
根据上述反应,判断下列结论中正确的是
①
 ;
;②
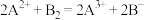 ;
;③
 ,
,根据上述反应,判断下列结论中正确的是
A.氧化性强弱顺序为: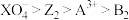 |
B.在溶液中不可能发生反应: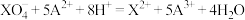 |
C. 是 是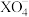 的氧化产物, 的氧化产物, 是 是 的还原产物 的还原产物 |
D.要除去含有 、 、 和 和 混合溶液中的 混合溶液中的 ,而不氧化 ,而不氧化 和 和 ,应加入 ,应加入 |
更新时间:2023-10-11 10:45:19
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】硫酸盐(含 、
、 )气溶胶是PM2.5的成分之一。近期科研人员提出了雾霾微颗粒中硫酸盐生成的转化机理,其主要过程示意图如下:
)气溶胶是PM2.5的成分之一。近期科研人员提出了雾霾微颗粒中硫酸盐生成的转化机理,其主要过程示意图如下:
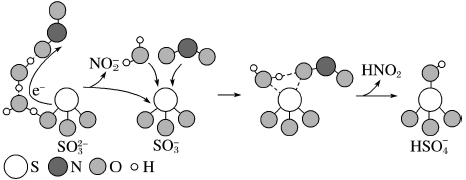
下列说法不正确的是
 、
、 )气溶胶是PM2.5的成分之一。近期科研人员提出了雾霾微颗粒中硫酸盐生成的转化机理,其主要过程示意图如下:
)气溶胶是PM2.5的成分之一。近期科研人员提出了雾霾微颗粒中硫酸盐生成的转化机理,其主要过程示意图如下:
下列说法不正确的是
| A.PM2.5指的是空气中小于等于2.5微米的颗粒物 |
B. 是生成硫酸盐的还原剂 是生成硫酸盐的还原剂 |
| C.硫酸盐气溶胶呈酸性 |
D.该过程有 参与 参与 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】向CuSO4溶液中逐滴加入KI溶液至过量,观察到有沉淀(CuI)生成,且溶液变为棕色,再向反应后的混合物中不断通入SO2气体,溶液逐渐变成无色。下列有关分析中正确的是
| A.通入SO2后溶液逐渐变成无色,体现了SO2的漂白性 |
| B.在SO2与I2反应中得到的还原产物为H2SO4 |
| C.滴加KI溶液时,每转移1mole-会生成2molCuI沉淀 |
| D.上述实验条件下,物质的氧化性:Cu2+> I2 > SO2 |
您最近一年使用:0次
【推荐3】已知HNO2在低温下较稳定,酸性比醋酸略强,既有还原性又有氧化性,其氧化产物、还原产物与溶液pH的关系如下表。下列有关说法错误的是
| pH范围 | >7 | <7 |
| 产物 |  | NO、N2O、N2中的一种 |
A.碱性条件下,NaNO2与NaClO反应的离子方程式为 + ClO- = + ClO- = +Cl- +Cl- |
| B.向冷的NaNO2溶液中加入滴有淀粉的氢碘酸,若溶液变蓝色,则证明氧化性:HNO2>I2 |
| C.向冷的NaNO2溶液中通入SO2最终可得到HNO2 |
| D.低温时不用其他试剂即可区分HNO2溶液与Na2CO3溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】根据相关的化学原理,下列判断正确的是
| A.由于氟化氢分子间存在氢键,所以稳定性:HF>HCl |
| B.由于二氧化硅的相对分子质量比二氧化碳的大,所以沸点:SiO2>CO2 |
| C.若A2+ 2D-=2A-+ D2,则氧化性D2>A2 |
| D.若R2—和M+的电子层结构相同,则离子半径R2—>M+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知反应:①SO2+2Fe3++2H2O→SO +2Fe2++W;②Cr2O
+2Fe2++W;②Cr2O +aFe2++bH+→cR3++Fe3++H2O(未配平)。下列有关说法正确的是
+aFe2++bH+→cR3++Fe3++H2O(未配平)。下列有关说法正确的是
 +2Fe2++W;②Cr2O
+2Fe2++W;②Cr2O +aFe2++bH+→cR3++Fe3++H2O(未配平)。下列有关说法正确的是
+aFe2++bH+→cR3++Fe3++H2O(未配平)。下列有关说法正确的是| A.方程式①中W为4OH- |
| B.还原性强弱:Fe2+>SO2 |
| C.a=6,b=7 |
D.反应Cr2O +3SO2+2H+→2Cr3++3SO +3SO2+2H+→2Cr3++3SO +H2O能发生 +H2O能发生 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】铋(Bi)位于元素周期表中VA族,其价态为+3价较稳定,铋酸钠(NaBiO3)溶液呈无色,取一定量的硫酸锰(MnSO4)溶液依次滴加下列溶液,对应的现象如下表所示:
则下列物质的氧化性由弱到强排列的顺序正确的是
| 加入溶液 | ①适量铋酸钠溶液 | ②过量的双氧水 | ③适量KI淀粉溶液 |
| 实验现象 | 溶液呈紫红色 | 紫红色消失,产生气泡 | 溶液变成蓝色 |
| A.I2,H2O2,KMnO4,NaBiO3 |
| B.H2O2,I2,NaBiO3,KMnO4 |
| C.NaBiO3,KMnO4,H2O2,I2 |
| D.KMnO4,NaBiO3,I2,H2O2 |
您最近一年使用:0次
【推荐2】设NA为阿伏加德罗常数的值,关于反应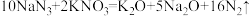 ,下列说法正确的是
,下列说法正确的是
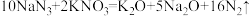 ,下列说法正确的是
,下列说法正确的是A.生成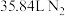 时,转移的电子数为NA 时,转移的电子数为NA |
B.等物质的量的 和 和 中所含阴离子数均为NA 中所含阴离子数均为NA |
| C.当氧化产物比还原产物多7mol时,转移的电子数为5NA |
D.含NA个 的 的 溶解于1L水中,所得溶液中 溶解于1L水中,所得溶液中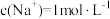 |
您最近一年使用:0次

 自由基与
自由基与 反应进程的能量变化如图所示。下列说法正确的是
反应进程的能量变化如图所示。下列说法正确的是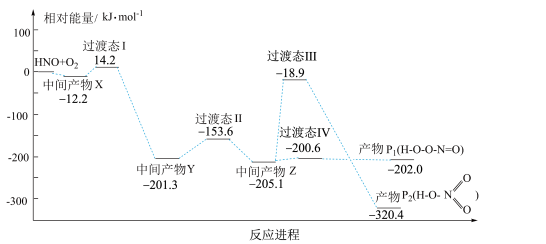
 的稳定性比产物
的稳定性比产物 的强
的强 转化为产物的速率:
转化为产物的速率:
 的键能总和
的键能总和

