请根据已知信息回答下列各问:
Ⅰ.已知H3PO2(次磷酸)是一元酸,H3PO2水溶液中存在H3PO2分子。
(1)写出 H3PO2溶液与足量NaOH溶液反应的离子方程式___________ 。
(2)磷酸(H3PO4)、亚磷酸(H3PO3)、次磷酸都是重要的化工产品。已知:1 mol磷酸、亚磷酸、次磷酸最多消耗NaOH的物质的量依次为3 mol、2 mol、1 mol。则NaH2PO4、NaH2PO2、NaH2PO3中属于正盐的是___________ (填化学式)。
Ⅱ. 可用作清洁剂、防腐剂等。
可用作清洁剂、防腐剂等。
(3)下列关于NaHSO4的说法正确的是___________ ;
a.NaHSO4固体不能导电 b.NaHSO4溶液的导电性一定强于CH3COOH溶液
c.NaHSO4属于电解质 d.NaHSO4溶液显中性
(4) 溶液与NaHCO3溶液反应的离子方程式为
溶液与NaHCO3溶液反应的离子方程式为___________ 。
Ⅲ.有以下物质:
①石墨、②铁、③蔗糖、④一氧化碳、⑤氯化铁固体、⑥碳酸氢钠固体、⑦氢氧化钡溶液、⑧纯醋酸、⑨熔融氯化钠、⑩液态氯化氢
(5)以上物质属于电解质的是___________ ;能导电的是___________
(6)写出用⑤的饱和溶液制备Fe(OH)3胶体的离子反应方程式:___________ 。
(7)将物质⑥配制成溶液,逐滴加入⑦溶液中至沉淀量最大,写出离子方程式:___________ 。
Ⅰ.已知H3PO2(次磷酸)是一元酸,H3PO2水溶液中存在H3PO2分子。
(1)写出 H3PO2溶液与足量NaOH溶液反应的离子方程式
(2)磷酸(H3PO4)、亚磷酸(H3PO3)、次磷酸都是重要的化工产品。已知:1 mol磷酸、亚磷酸、次磷酸最多消耗NaOH的物质的量依次为3 mol、2 mol、1 mol。则NaH2PO4、NaH2PO2、NaH2PO3中属于正盐的是
Ⅱ.
 可用作清洁剂、防腐剂等。
可用作清洁剂、防腐剂等。(3)下列关于NaHSO4的说法正确的是
a.NaHSO4固体不能导电 b.NaHSO4溶液的导电性一定强于CH3COOH溶液
c.NaHSO4属于电解质 d.NaHSO4溶液显中性
(4)
 溶液与NaHCO3溶液反应的离子方程式为
溶液与NaHCO3溶液反应的离子方程式为Ⅲ.有以下物质:
①石墨、②铁、③蔗糖、④一氧化碳、⑤氯化铁固体、⑥碳酸氢钠固体、⑦氢氧化钡溶液、⑧纯醋酸、⑨熔融氯化钠、⑩液态氯化氢
(5)以上物质属于电解质的是
(6)写出用⑤的饱和溶液制备Fe(OH)3胶体的离子反应方程式:
(7)将物质⑥配制成溶液,逐滴加入⑦溶液中至沉淀量最大,写出离子方程式:
更新时间:2023-10-23 08:51:07
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】现有以下物质:①氢氧化钡②Cu③BaCO3④Fe(OH)3胶体⑤酒精⑥NH3⑦稀硫酸⑧Al2(SO4)3
(1)以上物质中属于混合物的是_______ (填序号,下空同),属于电解质的是_______ 能导电的是_______
(2)向④中逐滴滴加⑦,可观察到的现象是_______ 。
(3)写出物质⑧在水中的电离方程式:_______ 。
(4)写出物质①和⑦反应的离子方程式:_______ 。
(5)8.5g⑥约含有_______ 个分子,含_______ mol质子。
(1)以上物质中属于混合物的是
(2)向④中逐滴滴加⑦,可观察到的现象是
(3)写出物质⑧在水中的电离方程式:
(4)写出物质①和⑦反应的离子方程式:
(5)8.5g⑥约含有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】日常消毒应做到安全消毒、有效消毒、绿色消毒。下列是我们常见的几种消毒剂:
①“84”消毒液、②高铁酸钠 、③漂白粉、④
、③漂白粉、④ 、⑤
、⑤ 、⑥碘酒、⑦75%的酒精、⑧过氧乙酸(
、⑥碘酒、⑦75%的酒精、⑧过氧乙酸( ,是一种弱酸)。回答下列问题:
,是一种弱酸)。回答下列问题:
(1)上述物质中属于电解质的是______ (填标号);“84”消毒液的有效成分NaClO在水中的电离方程式为______ 。
(2)已知反应 ,则在该反应的条件下,氧化性:
,则在该反应的条件下,氧化性:
______ (填“>”或“<”) ,当反应中转移电子的数目为
,当反应中转移电子的数目为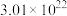 时,生成的氧气在标准状况下的体积为
时,生成的氧气在标准状况下的体积为______ L。
(3)高铁酸钠是一种新型净水剂,在水中发生反应: (胶体)
(胶体)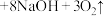 。
。
①该反应中,高铁酸钠中铁元素被______ (填“还原”或“氧化”)。
②某课外活动小组进行 胶体的制备及相关性质实验。
胶体的制备及相关性质实验。
制备:若将饱和 溶液分别滴入下列物质中,能形成胶体的是
溶液分别滴入下列物质中,能形成胶体的是______ (填标号)。
A.冷水 B.沸水 C. 浓溶液 D.
浓溶液 D. 浓溶液
浓溶液
鉴别: 胶体与
胶体与 溶液的鉴别方法是
溶液的鉴别方法是______ 。
 胶体区别于
胶体区别于 溶液最本质的特征是
溶液最本质的特征是______ 。
①“84”消毒液、②高铁酸钠
 、③漂白粉、④
、③漂白粉、④ 、⑤
、⑤ 、⑥碘酒、⑦75%的酒精、⑧过氧乙酸(
、⑥碘酒、⑦75%的酒精、⑧过氧乙酸( ,是一种弱酸)。回答下列问题:
,是一种弱酸)。回答下列问题:(1)上述物质中属于电解质的是
(2)已知反应
 ,则在该反应的条件下,氧化性:
,则在该反应的条件下,氧化性:
 ,当反应中转移电子的数目为
,当反应中转移电子的数目为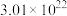 时,生成的氧气在标准状况下的体积为
时,生成的氧气在标准状况下的体积为(3)高铁酸钠是一种新型净水剂,在水中发生反应:
 (胶体)
(胶体)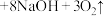 。
。①该反应中,高铁酸钠中铁元素被
②某课外活动小组进行
 胶体的制备及相关性质实验。
胶体的制备及相关性质实验。制备:若将饱和
 溶液分别滴入下列物质中,能形成胶体的是
溶液分别滴入下列物质中,能形成胶体的是A.冷水 B.沸水 C.
 浓溶液 D.
浓溶液 D. 浓溶液
浓溶液鉴别:
 胶体与
胶体与 溶液的鉴别方法是
溶液的鉴别方法是 胶体区别于
胶体区别于 溶液最本质的特征是
溶液最本质的特征是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】Ⅰ.① ②
②  ③液氨 ④
③液氨 ④ ⑤乙醇 ⑥
⑤乙醇 ⑥ 溶液 ⑦水 ⑧
溶液 ⑦水 ⑧ 固体。
固体。
(1)上述物质中属于电解质的是_______  填序号,下同
填序号,下同 ,属于非电解质的是
,属于非电解质的是_______ 。
(2)常温下,②⑦⑧这三种物质相互作用可生成一种新物质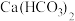 ,该反应
,该反应_______ (填“是”或“不是”)氧化还原反应。
(3)写出④和⑧分别在水中的电离方程式:_______ 、_______ 。
Ⅱ 完成下列填空。
完成下列填空。
(4) 的
的 中含有的分子数为
中含有的分子数为_______ (用 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
(5)要使 与
与 含相同数目的氢原子,则
含相同数目的氢原子,则 和
和 的质量之比为
的质量之比为_______ 。
(6)已知CO、CO2的混合气体质量12.8g,标准状况下的体积为8.96L,则混合气体的平均相对分子质量为_______ ,CO、CO2的物质的量之比为_______ 。
 ②
②  ③液氨 ④
③液氨 ④ ⑤乙醇 ⑥
⑤乙醇 ⑥ 溶液 ⑦水 ⑧
溶液 ⑦水 ⑧ 固体。
固体。(1)上述物质中属于电解质的是
 填序号,下同
填序号,下同 ,属于非电解质的是
,属于非电解质的是(2)常温下,②⑦⑧这三种物质相互作用可生成一种新物质
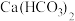 ,该反应
,该反应(3)写出④和⑧分别在水中的电离方程式:
Ⅱ
 完成下列填空。
完成下列填空。(4)
 的
的 中含有的分子数为
中含有的分子数为 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。(5)要使
 与
与 含相同数目的氢原子,则
含相同数目的氢原子,则 和
和 的质量之比为
的质量之比为(6)已知CO、CO2的混合气体质量12.8g,标准状况下的体积为8.96L,则混合气体的平均相对分子质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】现有以下物质:①碳酸钠 ②KOH溶液 ③Fe(OH)3固体 ④甲烷 ⑤铁或石墨 ⑥盐酸⑦CO2 ⑧熔融CuSO4。
(1)①属于电解质的有___ (填序号,下同)。
②属于非电解质的有___ 。
③能导电的有___ 。
④既不是电解质又不是非电解质的是___ 。
(2)写出下列物质在水溶液中的电离方程式:
①Na2CO3:___ 。
②KOH:___ 。
③CuSO4:___ 。
④HCl:___ 。
(3)制备Fe(OH)3胶体的化学方程式是___ 。
(4)写出实验室检验CO2的离子方程式:___ 。
(1)①属于电解质的有
②属于非电解质的有
③能导电的有
④既不是电解质又不是非电解质的是
(2)写出下列物质在水溶液中的电离方程式:
①Na2CO3:
②KOH:
③CuSO4:
④HCl:
(3)制备Fe(OH)3胶体的化学方程式是
(4)写出实验室检验CO2的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.有下列物质:①氢氧化钠固体 ②铜丝 ③氯化氢气体 ④稀硫酸 ⑤二氧化碳气体 ⑥氨水 ⑦碳酸钠粉末 ⑧蔗糖晶体 ⑨熔融氯化钠 ⑩CuSO4•5H2O晶体.请用序号填空:
(1)上述状态下可导电的是:________________________ ;
(2)属于电解质的是________________________________ ;
(3)属于非电解质的是______________________________ 。
Ⅱ.从下列各组反应对比中,判断哪种粒子的氧化性最强,哪种粒子还原性最强。
(4)铁钉浸入CuSO4溶液后,表面会附有红色物质;铜丝浸入AgNO3溶液后,表面会附有银白色物质。则在Cu、Fe、Ag中,________ 的还原性最强;在Cu2+、Fe2+、Ag+中,________ 的氧化性最强;
(5)铁钉在氯气中被锈蚀为棕褐色物质(FeCl3),而在盐酸中生成淡绿色溶液(FeCl2)。则在氯气分子(Cl2)、Cl-、H+中,______________ 具有氧化性,_____________ 的氧化性最强。
(1)上述状态下可导电的是:
(2)属于电解质的是
(3)属于非电解质的是
Ⅱ.从下列各组反应对比中,判断哪种粒子的氧化性最强,哪种粒子还原性最强。
(4)铁钉浸入CuSO4溶液后,表面会附有红色物质;铜丝浸入AgNO3溶液后,表面会附有银白色物质。则在Cu、Fe、Ag中,
(5)铁钉在氯气中被锈蚀为棕褐色物质(FeCl3),而在盐酸中生成淡绿色溶液(FeCl2)。则在氯气分子(Cl2)、Cl-、H+中,
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题。
(1)今有11种物质:①铝线;②石墨;③氯气;④BaSO4晶体;⑤纯硫酸;⑥金刚石;⑦石灰水;⑧乙醇;⑨熔融的KNO3;⑩NH3;⑪盐酸。其中:
ⅰ.能导电的是(填序号,下同)___________ ;
ⅱ.属于电解质的是___________ ;
ⅲ.属于非电解质的是___________ ;
ⅳ.既不是电解质又不是非电解质的是___________ 。
(2)ⅰ.配平下列离子方程式:___________ 。___________ 。
_____Fe(NO3)3+_______NaOH+______Cl2=____Na2FeO4+_____NaNO3+____NaCl+_____H2O
反应中___________ 元素被氧化,氧化剂与氧化产物的个数比为___________ 。
(1)今有11种物质:①铝线;②石墨;③氯气;④BaSO4晶体;⑤纯硫酸;⑥金刚石;⑦石灰水;⑧乙醇;⑨熔融的KNO3;⑩NH3;⑪盐酸。其中:
ⅰ.能导电的是(填序号,下同)
ⅱ.属于电解质的是
ⅲ.属于非电解质的是
ⅳ.既不是电解质又不是非电解质的是
(2)ⅰ.配平下列离子方程式:
______MnO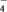 +_____H++______Cl-=_____Mn2++_____Cl2↑+_____H2O
+_____H++______Cl-=_____Mn2++_____Cl2↑+_____H2O
_____Fe(NO3)3+_______NaOH+______Cl2=____Na2FeO4+_____NaNO3+____NaCl+_____H2O
反应中
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】化学是一门研究物质的组成结构、性质及变化规律的自然学科。
Ⅰ.现有下列10种物质:①铝,②纯醋酸,③ ,④
,④ ,⑤
,⑤ ,⑥氢氧化钡固体,⑦盐酸,⑧
,⑥氢氧化钡固体,⑦盐酸,⑧ ,⑨
,⑨ 晶体,⑩乙醇。
晶体,⑩乙醇。
(1)上述物质中属于电解质的有___________ 。
(2)已知 为一元弱酸,则⑤在物质的分类中属于
为一元弱酸,则⑤在物质的分类中属于___________ (填“酸式盐”“正盐”或“碱式盐”)。
(3)⑥与⑧在溶液中反应使溶液呈中性的离子方程式为___________ 。
(4)Ⅱ.已知离子还原性 ,则氧化性
,则氧化性
___________  (填“>”“=”或“<”)。有一混合溶液,其中只含有
(填“>”“=”或“<”)。有一混合溶液,其中只含有 、
、 、
、 ,其中
,其中 、
、 的个数比为
的个数比为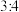 ,向该溶液中通入少量氯气,定会发生的反应的离子方程式是
,向该溶液中通入少量氯气,定会发生的反应的离子方程式是___________ 。如果要使上述溶液中 、
、 的个数比为
的个数比为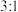 ,通入氯气与溶液中剩余
,通入氯气与溶液中剩余 的物质的量之比为
的物质的量之比为___________ 。
Ⅰ.现有下列10种物质:①铝,②纯醋酸,③
 ,④
,④ ,⑤
,⑤ ,⑥氢氧化钡固体,⑦盐酸,⑧
,⑥氢氧化钡固体,⑦盐酸,⑧ ,⑨
,⑨ 晶体,⑩乙醇。
晶体,⑩乙醇。(1)上述物质中属于电解质的有
(2)已知
 为一元弱酸,则⑤在物质的分类中属于
为一元弱酸,则⑤在物质的分类中属于(3)⑥与⑧在溶液中反应使溶液呈中性的离子方程式为
(4)Ⅱ.已知离子还原性
 ,则氧化性
,则氧化性
 (填“>”“=”或“<”)。有一混合溶液,其中只含有
(填“>”“=”或“<”)。有一混合溶液,其中只含有 、
、 、
、 ,其中
,其中 、
、 的个数比为
的个数比为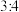 ,向该溶液中通入少量氯气,定会发生的反应的离子方程式是
,向该溶液中通入少量氯气,定会发生的反应的离子方程式是 、
、 的个数比为
的个数比为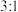 ,通入氯气与溶液中剩余
,通入氯气与溶液中剩余 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)写出下列物质在水溶液中的电离方程式:
①H2SO3_______ 、_______ 。
②Fe(OH)2_______ 。
③KHSO4:_______ 。
④NaHSO3_______
(2)写出下列反应的离子方程式
①少量CO2通入Ba(OH)2溶液中:_______ 。
②NH4HCO3溶液与少量NaOH溶液反应:_______ 。
③醋酸溶液与碳酸钙反应:_______ 。
④NaHCO3溶液与少量氢氧化钙溶液反应:_______
(3)用一种试剂除去下列各物质中的杂质(括号内的物质),写出所用的试剂及反应的离子方程式或除杂方法。
①BaCl2(HCl):试剂_______ ,离子方程式_______ 。
②CO2(HCl):试剂_______ ,除杂方法_______ 。
(1)写出下列物质在水溶液中的电离方程式:
①H2SO3
②Fe(OH)2
③KHSO4:
④NaHSO3
(2)写出下列反应的离子方程式
①少量CO2通入Ba(OH)2溶液中:
②NH4HCO3溶液与少量NaOH溶液反应:
③醋酸溶液与碳酸钙反应:
④NaHCO3溶液与少量氢氧化钙溶液反应:
(3)用一种试剂除去下列各物质中的杂质(括号内的物质),写出所用的试剂及反应的离子方程式或除杂方法。
①BaCl2(HCl):试剂
②CO2(HCl):试剂
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下列几种物质:①NaHCO3;②Na2CO3;③NaHSO4溶液;④CO2;⑤Ba(OH)2溶液;⑥C2H5OH(酒精);⑦KMnO4;⑧NH3·H2O;⑨饱和FeCl3溶液。根据要求回答下列问题:
(1)上述各物质属于电解质的是_______ (填物质编号,下同);属于非电解质的是_______ 。
(2)③中盐的电离方程式为_______ ;⑦在水中的电离方程式为_______ 。
(3)写出少量④通入⑤中反应的离子方程式:_______ ;
③和⑧在水溶液中反应的离子方程式:_______ 。
(4)向②的水溶液中加入⑤,生成白色沉淀,写出该反应的化学方程式:_______ 。
(5)①既能与酸反应,也能与碱反应,请写出①与NaOH溶液反应的离子方程式:_______ 。
(1)上述各物质属于电解质的是
(2)③中盐的电离方程式为
(3)写出少量④通入⑤中反应的离子方程式:
③和⑧在水溶液中反应的离子方程式:
(4)向②的水溶液中加入⑤,生成白色沉淀,写出该反应的化学方程式:
(5)①既能与酸反应,也能与碱反应,请写出①与NaOH溶液反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】完成下列反应离子方程式:
(1)碳酸钙与盐酸反应__ ;
(2)钠投入到水中___ ;
(3)碳酸氢钠与氢氧化钠溶液反应___ ;
(4)过氧化钠粉末加入到水中___ 。
(1)碳酸钙与盐酸反应
(2)钠投入到水中
(3)碳酸氢钠与氢氧化钠溶液反应
(4)过氧化钠粉末加入到水中
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】填空
(1)书写下列反应的化学方程式:
①用氯气制备漂白粉:______ 。
②KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2气体,还生成CO2和KHSO4等物质。写出该反应的化学方程式______ 。
(2)书写下列反应的离子方程式:
③少量澄清石灰水与NaHCO3混合:______ 。
④碘化亚铁溶液中加入少量氯水:______ 。
⑤硫酸亚铁酸性溶液在空气中变黄色:______ 。
⑥Fe3O4溶于过量稀硝酸的离子方程式为:______ 。
⑦在酸性条件,向含铬废水中加入FeSO4,可将 还原为Cr3+,该过程的离子反应方程式为
还原为Cr3+,该过程的离子反应方程式为______ 。
(1)书写下列反应的化学方程式:
①用氯气制备漂白粉:
②KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2气体,还生成CO2和KHSO4等物质。写出该反应的化学方程式
(2)书写下列反应的离子方程式:
③少量澄清石灰水与NaHCO3混合:
④碘化亚铁溶液中加入少量氯水:
⑤硫酸亚铁酸性溶液在空气中变黄色:
⑥Fe3O4溶于过量稀硝酸的离子方程式为:
⑦在酸性条件,向含铬废水中加入FeSO4,可将
 还原为Cr3+,该过程的离子反应方程式为
还原为Cr3+,该过程的离子反应方程式为
您最近一年使用:0次


 可制取“84”消毒液,实验室制取
可制取“84”消毒液,实验室制取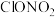 可与水反应生成两种酸,请写出对应化学方程式
可与水反应生成两种酸,请写出对应化学方程式

