填空
(1)书写下列反应的化学方程式:
①用氯气制备漂白粉:______ 。
②KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2气体,还生成CO2和KHSO4等物质。写出该反应的化学方程式______ 。
(2)书写下列反应的离子方程式:
③少量澄清石灰水与NaHCO3混合:______ 。
④碘化亚铁溶液中加入少量氯水:______ 。
⑤硫酸亚铁酸性溶液在空气中变黄色:______ 。
⑥Fe3O4溶于过量稀硝酸的离子方程式为:______ 。
⑦在酸性条件,向含铬废水中加入FeSO4,可将 还原为Cr3+,该过程的离子反应方程式为
还原为Cr3+,该过程的离子反应方程式为______ 。
(1)书写下列反应的化学方程式:
①用氯气制备漂白粉:
②KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2气体,还生成CO2和KHSO4等物质。写出该反应的化学方程式
(2)书写下列反应的离子方程式:
③少量澄清石灰水与NaHCO3混合:
④碘化亚铁溶液中加入少量氯水:
⑤硫酸亚铁酸性溶液在空气中变黄色:
⑥Fe3O4溶于过量稀硝酸的离子方程式为:
⑦在酸性条件,向含铬废水中加入FeSO4,可将
 还原为Cr3+,该过程的离子反应方程式为
还原为Cr3+,该过程的离子反应方程式为
更新时间:2024-01-11 17:31:52
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】合成氨工业对人类社会的发展具有里程碑式意义。
(1)工业常用CH4与H2O高温下制合成氨的原料气H2,1molCH4完全转化为CO2时理论能制得H2的物质的量为___________ 。
(2)等离子体合成氨使用H2O代替H2作为氢源,模拟制备原理如图所示,在高压电场作用下,N2与H2O以一定流速通过反应器,主要得到NH3与HNO2(弱酸),气体流出反应器后,经过一定长度的导管进入成分分析装置。

①等离子体合成氨反应的化学方程式为___________ 。
②成分分析表明,连接反应器与成分分析装置的导管的长度d越长,测得气体中NH3与HNO2的含量越低,其原因可能是___________ 。
③若将原料气中N2替换为空气,反应器流出气体中NH3及NOx浓度随原料气相对湿度(水蒸气含量)的变化如图所示,流出气体中NH3的浓度几乎为0的原因可能是___________ 。

(1)工业常用CH4与H2O高温下制合成氨的原料气H2,1molCH4完全转化为CO2时理论能制得H2的物质的量为
(2)等离子体合成氨使用H2O代替H2作为氢源,模拟制备原理如图所示,在高压电场作用下,N2与H2O以一定流速通过反应器,主要得到NH3与HNO2(弱酸),气体流出反应器后,经过一定长度的导管进入成分分析装置。

①等离子体合成氨反应的化学方程式为
②成分分析表明,连接反应器与成分分析装置的导管的长度d越长,测得气体中NH3与HNO2的含量越低,其原因可能是
③若将原料气中N2替换为空气,反应器流出气体中NH3及NOx浓度随原料气相对湿度(水蒸气含量)的变化如图所示,流出气体中NH3的浓度几乎为0的原因可能是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】过氧化氢俗名双氧水,医疗上利用它有杀菌消毒的作用来清洗伤口。针对以下A—D四个涉及H2O2的反应(未配平)填空:
A.Na2O2+HCl→NaCl+H2O2
B.Ag2O+H2O2→Ag+O2↑+H2O
C.H2O2→H2O+O2↑
D.H2O2+Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O
(1)上述反应中,H2O2仅体现氧化性的反应是____ (填字母,下同),H2O2仅体现还原性的反应是____ ,H2O2既体现氧化性又体现还原性的反应是____ 。
(2)请将D反应配平,并用单线桥标出D反应中电子转移的方向合数目:____ ,反应中氧化剂是____ ,被氧化的元素是____ ,氧化产物是____ 。
(3)某酸性反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:Fe3+、Mn2+、MnO 、H2O、Fe2+、H+,则反应的离子方程式为
、H2O、Fe2+、H+,则反应的离子方程式为____ 。
A.Na2O2+HCl→NaCl+H2O2
B.Ag2O+H2O2→Ag+O2↑+H2O
C.H2O2→H2O+O2↑
D.H2O2+Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O
(1)上述反应中,H2O2仅体现氧化性的反应是
(2)请将D反应配平,并用单线桥标出D反应中电子转移的方向合数目:
(3)某酸性反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:Fe3+、Mn2+、MnO
 、H2O、Fe2+、H+,则反应的离子方程式为
、H2O、Fe2+、H+,则反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】金属钠及其化合物在人类生产生活中起着重要作用。回答下列问题:
(1)基态Na原子的价层电子轨道表示式为___________ 。
(2)NaCl熔点为800.8℃,工业上采用电解熔融NaCl制备金属Na。电解反应方程式如下: ,加入
,加入 的目的是
的目的是___________ 。
(3) 的电子式为
的电子式为___________ 。在25℃和101kPa时,Na与 反应生成1mol
反应生成1mol 放热510.9kJ,写出该反应的热化学方程式:
放热510.9kJ,写出该反应的热化学方程式:___________ 。 可作供氧剂,写出
可作供氧剂,写出 与CO2反应的化学方程式
与CO2反应的化学方程式___________ 。若有1mol 参加反应则转移电子的物质的量为
参加反应则转移电子的物质的量为___________ mol。
(4)采用空气和Na为原料可直接制备 。空气与熔融金属Na反应前需依次通过
。空气与熔融金属Na反应前需依次通过___________ 、___________ (填序号)。
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d. 溶液
溶液
(5)向酸性KMnO4溶液中加入 粉末,观察到溶液褪色,发生如下反应: ______MnO
粉末,观察到溶液褪色,发生如下反应: ______MnO +_____H++_____Na2O2=_____Mn2+_____O2↑+_____H2O+_____Na+,配平该离子方程式:
+_____H++_____Na2O2=_____Mn2+_____O2↑+_____H2O+_____Na+,配平该离子方程式:___________ ,该反应说明 具有
具有___________ 性(选填“氧化”,“还原”或“漂白”)。
(6)钠的某氧化物晶胞如下图,图中所示钠离子全部位于晶胞内。由晶胞图判断该氧化物的化学式为___________ 。

(7)天然碱的主要成分为 ,1mol
,1mol 经充分加热得到
经充分加热得到 的质量为
的质量为___________ g。
(1)基态Na原子的价层电子轨道表示式为
(2)NaCl熔点为800.8℃,工业上采用电解熔融NaCl制备金属Na。电解反应方程式如下:
 ,加入
,加入 的目的是
的目的是(3)
 的电子式为
的电子式为 反应生成1mol
反应生成1mol 放热510.9kJ,写出该反应的热化学方程式:
放热510.9kJ,写出该反应的热化学方程式: 可作供氧剂,写出
可作供氧剂,写出 与CO2反应的化学方程式
与CO2反应的化学方程式 参加反应则转移电子的物质的量为
参加反应则转移电子的物质的量为(4)采用空气和Na为原料可直接制备
 。空气与熔融金属Na反应前需依次通过
。空气与熔融金属Na反应前需依次通过a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.
 溶液
溶液(5)向酸性KMnO4溶液中加入
 粉末,观察到溶液褪色,发生如下反应: ______MnO
粉末,观察到溶液褪色,发生如下反应: ______MnO +_____H++_____Na2O2=_____Mn2+_____O2↑+_____H2O+_____Na+,配平该离子方程式:
+_____H++_____Na2O2=_____Mn2+_____O2↑+_____H2O+_____Na+,配平该离子方程式: 具有
具有(6)钠的某氧化物晶胞如下图,图中所示钠离子全部位于晶胞内。由晶胞图判断该氧化物的化学式为

(7)天然碱的主要成分为
 ,1mol
,1mol 经充分加热得到
经充分加热得到 的质量为
的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】请回答下列问题:
(1)海洋是资源的宝库,与“海水晒盐”相仿的实验操作是
(2)粗盐中会含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是一种制备精盐的实验方案(用于沉淀的试剂稍过量):

操作①能否改用Ba(NO3)2?_______ (填“是”或“否”),原因_______ 。此实验方案尚需完善,具体步骤是_______ 。
(3)电解饱和食盐水的化学方程式:_______ ,电解一段时间后用湿润的_______ 试纸检验阳极生成的气体,现象:_______ ,
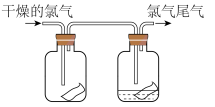
(4)将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是_______ 。
(5)工业上制取漂白粉的化学方程式:_______ 。
(1)海洋是资源的宝库,与“海水晒盐”相仿的实验操作是
| A.蒸馏 | B.萃取 | C.蒸发结晶 | D.分液 |

操作①能否改用Ba(NO3)2?
(3)电解饱和食盐水的化学方程式:
(4)将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是

(5)工业上制取漂白粉的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)钠及其化合物在生产和生活中有着重要的应用,体现了化学的魅力。按要求写出下列反应的方程式:
①钠与水反应离子方程式:___________ 。
②过氧化钠可用干呼吸面具的供氧剂,其主要反应原理的化学方程式:___________ 。
③氢氧化钠溶液吸收过量的二氧化碳的离子方程式:___________ 。
(2)最初,人们直按用氯水作漂白剂,但因 溶解度不大,而且生成的次氯酸不稳定,难以保存,使用起来不方便。在氯气与水反应原理的基础上,人们将
溶解度不大,而且生成的次氯酸不稳定,难以保存,使用起来不方便。在氯气与水反应原理的基础上,人们将 通入冷的石灰乳中,可以得到一种漂白粉,该反应的化学方程式为
通入冷的石灰乳中,可以得到一种漂白粉,该反应的化学方程式为___________ ,该漂白粉的有效成分是___________ (填名称)。
(3)检验某溶液中含有 的方法是
的方法是___________ ,有关反应的离子方程式___________ 。
(1)钠及其化合物在生产和生活中有着重要的应用,体现了化学的魅力。按要求写出下列反应的方程式:
①钠与水反应离子方程式:
②过氧化钠可用干呼吸面具的供氧剂,其主要反应原理的化学方程式:
③氢氧化钠溶液吸收过量的二氧化碳的离子方程式:
(2)最初,人们直按用氯水作漂白剂,但因
 溶解度不大,而且生成的次氯酸不稳定,难以保存,使用起来不方便。在氯气与水反应原理的基础上,人们将
溶解度不大,而且生成的次氯酸不稳定,难以保存,使用起来不方便。在氯气与水反应原理的基础上,人们将 通入冷的石灰乳中,可以得到一种漂白粉,该反应的化学方程式为
通入冷的石灰乳中,可以得到一种漂白粉,该反应的化学方程式为(3)检验某溶液中含有
 的方法是
的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】“化学——我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。请填空:
(1)在呼吸面具和潜水艇中可用过氧化钠作为供氧剂,请写出其中一个反应的化学方程式___________ 。
(2)氯水和漂白粉都有漂白作用,也可用于水体的杀菌消毒。
①工业上利用氯气和氢氧化钙反应可制得漂白粉,其化学方程式___________ 。
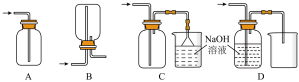
②下列收集Cl2的正确装置是___________ 。
③将灼热的铜丝伸入盛有氯气的集气瓶中,反应的方程式为___________ 。将反应后的产物溶于水配成饱和溶液,向溶液中加入一小块金属钠,发生反应的离子方程式为________ 、_________ 。
④某同学设计了下图实验装置进一步研究氯气的漂白性,已知通入的氯气中还含有空气和水蒸气。回答下列问题:
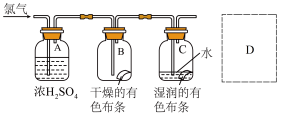
i.浓H2SO4的作用是___________ 。
ii.与研究目的直接相关的实验现象是___________ 。
iii.该实验设计存在事故隐患,应在D处增加一装置,该装置中应加入烧碱溶液以除去多余的氯气,该反应的离子方程式为___________ 。
(1)在呼吸面具和潜水艇中可用过氧化钠作为供氧剂,请写出其中一个反应的化学方程式
(2)氯水和漂白粉都有漂白作用,也可用于水体的杀菌消毒。
①工业上利用氯气和氢氧化钙反应可制得漂白粉,其化学方程式
②下列收集Cl2的正确装置是

③将灼热的铜丝伸入盛有氯气的集气瓶中,反应的方程式为
④某同学设计了下图实验装置进一步研究氯气的漂白性,已知通入的氯气中还含有空气和水蒸气。回答下列问题:

i.浓H2SO4的作用是
ii.与研究目的直接相关的实验现象是
iii.该实验设计存在事故隐患,应在D处增加一装置,该装置中应加入烧碱溶液以除去多余的氯气,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】阅读下列科普短文并填空:
海洋的水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如 、
、 等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和
等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和 用以生产
用以生产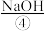 、
、 、
、 、
、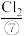 、
、 等,苦卤经过氯气氧化、热空气吹出、
等,苦卤经过氯气氧化、热空气吹出、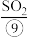 吸收等一系列操作可获得Br2。电解熔融氯化钠可冶炼
吸收等一系列操作可获得Br2。电解熔融氯化钠可冶炼 。海底埋藏大量可燃冰资源,
。海底埋藏大量可燃冰资源, 是一种清洁能源。
是一种清洁能源。
(1)上述标有序号的物质中属于电解质的是___________ (填序号,下同):属于非电解质的是___________ 。
(2)写出⑤溶于水的电离方程式:___________ 。
将⑧与④混合,写出离子反应方程式___________ 。
将⑨通入足量④的溶液中,写出离子反应方程式___________ 。
将⑤与④的溶液混合,写出离子反应方程式___________ 。
(3)海水提溴的过程中涉及的反应有 ,
, ,根据上述反应可判断Cl-、Br-、SO2的还原性由强到弱的顺序为
,根据上述反应可判断Cl-、Br-、SO2的还原性由强到弱的顺序为___________ 。
(4)实验室检验自来水中含有氯离子的化学试剂为___________ 。
(5)元素 的一种含氧酸化学式为H3GO3,属于二元酸,则H3GO3与过量氢氧化钠溶液反应,生成的正盐的化学式
的一种含氧酸化学式为H3GO3,属于二元酸,则H3GO3与过量氢氧化钠溶液反应,生成的正盐的化学式___________ 。
海洋的水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如
 、
、 等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和
等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和 用以生产
用以生产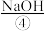 、
、 、
、 、
、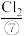 、
、 等,苦卤经过氯气氧化、热空气吹出、
等,苦卤经过氯气氧化、热空气吹出、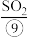 吸收等一系列操作可获得Br2。电解熔融氯化钠可冶炼
吸收等一系列操作可获得Br2。电解熔融氯化钠可冶炼 。海底埋藏大量可燃冰资源,
。海底埋藏大量可燃冰资源, 是一种清洁能源。
是一种清洁能源。(1)上述标有序号的物质中属于电解质的是
(2)写出⑤溶于水的电离方程式:
将⑧与④混合,写出离子反应方程式
将⑨通入足量④的溶液中,写出离子反应方程式
将⑤与④的溶液混合,写出离子反应方程式
(3)海水提溴的过程中涉及的反应有
 ,
, ,根据上述反应可判断Cl-、Br-、SO2的还原性由强到弱的顺序为
,根据上述反应可判断Cl-、Br-、SO2的还原性由强到弱的顺序为(4)实验室检验自来水中含有氯离子的化学试剂为
(5)元素
 的一种含氧酸化学式为H3GO3,属于二元酸,则H3GO3与过量氢氧化钠溶液反应,生成的正盐的化学式
的一种含氧酸化学式为H3GO3,属于二元酸,则H3GO3与过量氢氧化钠溶液反应,生成的正盐的化学式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求回答下列问题:
(1)①水银 ②烧碱 ③大理石 ④氯化钠晶体 ⑤盐酸 ⑥氨气 ⑦蔗糖 ⑧二氧化碳 ⑨液态氯化氢 ⑩澄清石灰水。
上述物质中能导电的是___________ ,属于电解质的是___________ ,属于非电解质的是___________ (填编号)
(2)按要求写出下列方程式:
①KAl(SO4)2电离的电离方程式:___________ 。
②碳酸钙与盐酸反应的离子有程式:___________ 。
③碳酸氢钠与氢氧化钡反应至溶液恰好为中性,反应的离子方程式:___________ 。
(1)①水银 ②烧碱 ③大理石 ④氯化钠晶体 ⑤盐酸 ⑥氨气 ⑦蔗糖 ⑧二氧化碳 ⑨液态氯化氢 ⑩澄清石灰水。
上述物质中能导电的是
(2)按要求写出下列方程式:
①KAl(SO4)2电离的电离方程式:
②碳酸钙与盐酸反应的离子有程式:
③碳酸氢钠与氢氧化钡反应至溶液恰好为中性,反应的离子方程式:
您最近一年使用:0次
【推荐3】(1)在下列反应中:
A.2F2+2H2O=4HF+O2 B.2Na+2H2O=2NaOH+H2↑
C.3NO2+H2O=2HNO3+NO D.2H2O 2H2↑+O2↑
2H2↑+O2↑
其中水只作氧化剂的是__________ ,水只作还原剂的是__________ ,水既作氧化剂又作还原剂的是__________ ,水既不作氧化剂又不作还原剂的是________
(2)新制氯水中含有多种成分:将紫色石蕊试液滴入氯水中,溶液显红色,起作用的成分是_____ ;过一会儿,溶液的颜色逐渐褪去,起作用的成分是_________ ;往氯水中滴入硝酸银溶液,产生白色沉淀,起作用的成分是________ ;氯水能使淀粉碘化钾试纸变蓝,起作用的成分是________ 。
(3)将过量的二氧化碳气体通入烧碱溶液中,然后将反应后的溶液分成二等份,分别加入与所得溶液溶质等物质的量的硝酸、氢氧化钙溶液。请分别写出发生反应的离子方程式:
①________________________________ 。
②_____________________________________ 。
A.2F2+2H2O=4HF+O2 B.2Na+2H2O=2NaOH+H2↑
C.3NO2+H2O=2HNO3+NO D.2H2O
 2H2↑+O2↑
2H2↑+O2↑其中水只作氧化剂的是
(2)新制氯水中含有多种成分:将紫色石蕊试液滴入氯水中,溶液显红色,起作用的成分是
(3)将过量的二氧化碳气体通入烧碱溶液中,然后将反应后的溶液分成二等份,分别加入与所得溶液溶质等物质的量的硝酸、氢氧化钙溶液。请分别写出发生反应的离子方程式:
①
②
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】钴在硬质高温合金、催化剂等高新技术领域有广泛应用。从某炼锌厂的废渣(含Zn、Co、Fe、ZnO、SiO2等)中回收钴的一种工艺流程如图:
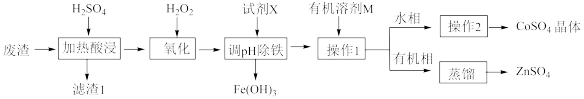
相关金属离子[Co(Mn+ )=0.1mol·L-1]形成氢氧化物沉淀的pH范围如表:
(1)若无氧化步骤,对实验的影响是_____ 。试剂X可以为下列物质中的_____ 。
A.KOH B.Zn(OH)2 C.ZnO D.Na2CO3
(2)常温下,已知Co(OH)3的溶度积常数为Ksp,则Co3+完全沉淀时[c(Co3+)<10-5mol·L-1],溶液的pH至少为_____ (用含Ksp的式子表示)。

相关金属离子[Co(Mn+ )=0.1mol·L-1]形成氢氧化物沉淀的pH范围如表:
| 金属离子 | Co2+ | Fe2+ | Fe3+ | Zn2+ |
| 开始沉淀的pH | 7.15 | 6.3 | 1.5 | 6.2 |
| 沉淀完全的pH | 9.15 | 8.3 | 2.8 | 8.2 |
A.KOH B.Zn(OH)2 C.ZnO D.Na2CO3
(2)常温下,已知Co(OH)3的溶度积常数为Ksp,则Co3+完全沉淀时[c(Co3+)<10-5mol·L-1],溶液的pH至少为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】对化学反应的原理及物质的性质的认识离不开化学实验。回答下列问题。
(1)探究Ba(OH)2溶液与稀硫酸反应的实质。
向20mL0.01mol·L-1Ba(OH)2溶液中滴入几滴酚酞溶液,然后向其中匀速逐滴加入0.2 mol·L-1H2SO4溶液。测定电导率的变化如图所示。

①Ba(OH)2在水中的电离方程式是_______ 。
②A-B段,除电导率下降外,还能观察到的现象是_______ ,用离子方程式表示有关实验现象的原因_______ 。
(2)探究FeSO4溶液的性质。
①性质预测:从物质类别角度分析FeSO4属于盐,可以与某些碱反应;从元素化合价变化的角度分析FeCl2具有的性质是_______ 。
②实验探究:
i中的现象是_______ ,ii中的离子方程式是_______ ,iii中的现象是_______ 。
(1)探究Ba(OH)2溶液与稀硫酸反应的实质。
向20mL0.01mol·L-1Ba(OH)2溶液中滴入几滴酚酞溶液,然后向其中匀速逐滴加入0.2 mol·L-1H2SO4溶液。测定电导率的变化如图所示。

①Ba(OH)2在水中的电离方程式是
②A-B段,除电导率下降外,还能观察到的现象是
(2)探究FeSO4溶液的性质。
①性质预测:从物质类别角度分析FeSO4属于盐,可以与某些碱反应;从元素化合价变化的角度分析FeCl2具有的性质是
②实验探究:
 FeSO4溶液 | 序号 | 操作 |
| i | 滴加NaOH溶液 | |
| ii | 加入少量锌粉 | |
| iii | 加入几滴酸性KMnO4溶液 |
i中的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】铝、铁是常见的两种金属,它们的单质及化合物在生活生产中处处可见。
(1)过量的铁和稀硝酸发生反应,产物是Fe(NO3)2和NO,写出该反应的化学方程式_________________________________________________ 。
(2)实验室配制FeSO4溶液时,如果没有隔绝空气,FeSO4会被氧化为___________ (填化学式)。在该溶液中加入___________ 试剂,看到_____________________ 现象,证明溶液变质。
(3)已知:Ba(AlO2)2可溶于水,下图表示的是向Al2(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系。

由图可知c点的沉淀是___________ (填化学式),已知a-b时存在的沉淀是Al(OH)3和BaSO4,a点时,n(BaSO4)_____ n(Al(OH)3)(填“>”“<”“=”)。
(1)过量的铁和稀硝酸发生反应,产物是Fe(NO3)2和NO,写出该反应的化学方程式
(2)实验室配制FeSO4溶液时,如果没有隔绝空气,FeSO4会被氧化为
(3)已知:Ba(AlO2)2可溶于水,下图表示的是向Al2(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系。

由图可知c点的沉淀是
您最近一年使用:0次



