现有4组标准电极电势:①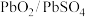 ,
,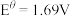 ;②
;②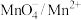 ,
,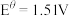 ;②
;② ,
,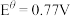 ;④
;④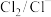 ,
,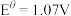 。已知电势越高对应物质的氧化性越强,则下列离子方程式或相应的描述中正确的是
。已知电势越高对应物质的氧化性越强,则下列离子方程式或相应的描述中正确的是
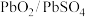 ,
,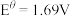 ;②
;②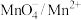 ,
,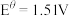 ;②
;② ,
,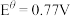 ;④
;④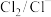 ,
,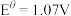 。已知电势越高对应物质的氧化性越强,则下列离子方程式或相应的描述中正确的是
。已知电势越高对应物质的氧化性越强,则下列离子方程式或相应的描述中正确的是A.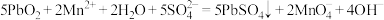 |
B.向含 的溶液中加 的溶液中加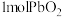 不能观察到黄绿色气体 不能观察到黄绿色气体 |
| C.酸化高锰酸钾时既可以用硫酸也可以用盐酸 |
D.氧化性由强到弱的顺序为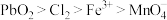 |
更新时间:2023-10-11 08:58:18
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】已知还原性: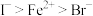 ,下列离子方程式正确的是
,下列离子方程式正确的是
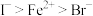 ,下列离子方程式正确的是
,下列离子方程式正确的是A.将少量 通入 通入 溶液中: 溶液中: |
B.将足量 通入 通入 溶液中: 溶液中: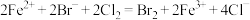 |
C.将少量 通入 通入 溶液中: 溶液中: |
D.将  通入 通入  溶液中: 溶液中: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于氧化还原反应的说法正确的是
| A.物质失电子越多,还原性越强;得电子越多,氧化性越强 |
| B.具有氧化性和还原性的物质放在一起就一定能发生氧化还原反应 |
| C.反应中肯定有一种元素被氧化,另一种元素被还原 |
| D.已知Fe+Cu2+===Fe2++Cu,2Fe3++Cu===2Fe2++Cu2+;则氧化性:Fe3+>Cu2+>Fe2+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】亚砷酸(H3AsO3)与氯化亚锡(SnCl2)在浓盐酸中发生反应的离子方程式为:3Sn2++2H3AsO3+6H++18Cl-=2As+3SnCl62-+6M下列关于该反应的说法错误的是
| A.M为H2O |
| B.还原性:Sn2+>As |
| C.SnCl62-是氧化反应的产物 |
| D.每生成1.5 mol SnCl62-,H3AsO3失去电子的物质的量为4mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】工业上用二氧化硫制取氢气的流程如下,下列有关说法不正确的是


| A.反应器中硫元素的化合价升高 |
| B.分离器中分离出的副产品为硫酸 |
C.膜反应器中反应为2HI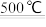 H2+I2 H2+I2 |
| D.生产流程中,循环利用的物质是氢气 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:Al2O3+N2+3C 2AlN+3CO,下列叙述正确的是
2AlN+3CO,下列叙述正确的是
 2AlN+3CO,下列叙述正确的是
2AlN+3CO,下列叙述正确的是| A.在氮化铝的合成反应中,N2是还原剂,Al2O3是氧化剂 |
| B.上述反应中每生成2molAlN,N2得到3mol电子 |
| C.氮化铝中氮元素的化合价为-3价 |
| D.反应的电子转移数为3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3=K2O+5Na2O+16N2↑。若氧化产物比还原产物多1.75mol,则下列判断正确的是
| A.生成40.0L N2(标准状况) | B.有0.250mol KNO3被氧化 |
| C.转移电子的物质的量为1.25mol | D.被氧化的N原子的物质的量为4.75mol |
您最近一年使用:0次

 溶液反应:
溶液反应: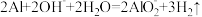
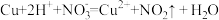
 氧化酸性溶液中的
氧化酸性溶液中的 :
: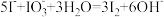
 +OH-
+OH- NH3↑+H2O
NH3↑+H2O +3Fe2++4H+=3Fe3++NO↑+2H2O
+3Fe2++4H+=3Fe3++NO↑+2H2O

