物质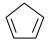 、
、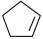 与
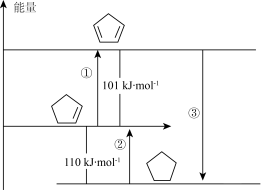
与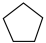 的能量存在如图所示的相互关系。人为规定H2(g)的能量为0kJ·mol-1。下列有关说法
的能量存在如图所示的相互关系。人为规定H2(g)的能量为0kJ·mol-1。下列有关说法错误 的是
 、
、 与
与 的能量存在如图所示的相互关系。人为规定H2(g)的能量为0kJ·mol-1。下列有关说法
的能量存在如图所示的相互关系。人为规定H2(g)的能量为0kJ·mol-1。下列有关说法
A.物质 是图示三种物质中最稳定的 是图示三种物质中最稳定的 |
| B.过程①属于吸热反应 |
| C.过程③的ΔH=+211kJ·mol-1 |
| D.物质变化过程中所放出或吸收的热量的多少与路径无关 |
更新时间:2023-10-11 19:44:53
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】已知25℃、101kPa条件下:
①4Al(s)+3O2(g) 2Al2O3(s) ΔH=-2834.9 kJ•mol-1
2Al2O3(s) ΔH=-2834.9 kJ•mol-1
②4Al(s)+2O3(g) 2Al2O3(s) ΔH=-3119.1 kJ•mol-1
2Al2O3(s) ΔH=-3119.1 kJ•mol-1
由此得出的正确结论是
①4Al(s)+3O2(g)
 2Al2O3(s) ΔH=-2834.9 kJ•mol-1
2Al2O3(s) ΔH=-2834.9 kJ•mol-1②4Al(s)+2O3(g)
 2Al2O3(s) ΔH=-3119.1 kJ•mol-1
2Al2O3(s) ΔH=-3119.1 kJ•mol-1由此得出的正确结论是
| A.O3比O2稳定,由O2变O3为放热反应 |
| B.由反应①可确定铝的燃烧热是708.7kJ |
| C.等质量的O2比O3能量低,O2变O3为吸热反应 |
| D.由反应②可确定铝的燃烧热是779.78 kJ•mol-1 |
您最近一年使用:0次
【推荐2】某反应由两步反应A→B→C构成,它的反应过程中能量变化曲线如下图所示(E1、E2、E3、E4表示活化能)。下列有关叙述正确的是
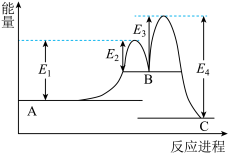

| A.两步反应均为吸热反应 | B.加入催化剂会改变反应的焓变 |
| C.三种物质中C最稳定 | D.A→C反应中ΔH=E1-E2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】下列说法正确的是
| A.已知25℃、101kPa条件下:4Al(s)+3O2(g)=2Al2O3(s) ΔH=-2834.9kJ/mol,4Al(s)+2O3(g)=2Al2O3(s) ΔH=-3119.1kJ/mol,则O3比O2稳定 |
| B.C2H5OH(l)的燃烧热是1366.8kJ/mol,则反应C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)的ΔH=-1366.8kJ/mol |
| C.已知中和热为57.3kJ/mol,则反应H2SO4(aq)+Ba(OH)2(aq)=2H2O(l)+BaSO4(s)的ΔH=-114.6kJ/mol |
| D.在一定温度和压强下,将0.5mol N2和1.5molH2置于密闭容器中充分反应生成NH3(g),放出热量19.3kJ,则其热化学方程式为N2(g)+3H2(g)⇌2NH3(g) ΔH=-38.6kJ/mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】Burns和Dainton研究发现 与CO合成
与CO合成 的反应机理如下:
的反应机理如下:
① 快
快
②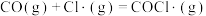 快
快
③ 慢,下列说法错误的是
慢,下列说法错误的是
 与CO合成
与CO合成 的反应机理如下:
的反应机理如下:①
 快
快②
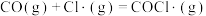 快
快③
 慢,下列说法错误的是
慢,下列说法错误的是| A.反应①发生时需要吸收能量 |
| B.反应①的活化能小于反应③的活化能 |
C.要提高合成 速率,关键是提高反应②的速率 速率,关键是提高反应②的速率 |
D.选择合适的催化剂能提高单位时间内 的产率 的产率 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列变化过程符合如图能量变化规律的是
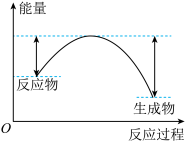

A.灼热的木炭与 的反应 的反应 | B.金属铝与盐酸反应 |
C. 晶体与 晶体与 晶体混合搅拌 晶体混合搅拌 | D.碳酸氢钠受热分解 |
您最近一年使用:0次
【推荐1】已知:
 ,
,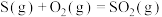
 ,下列说法正确的是
,下列说法正确的是

 ,
,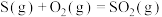
 ,下列说法正确的是
,下列说法正确的是A.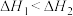 | B. 表示 表示 的燃烧热 的燃烧热 |
C. 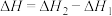 | D. 比 比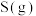 稳定 稳定 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列说法或表示方法不正确的是( )
| A.盖斯定律实质上是能量守恒定律的体现 |
| B.在稀溶液中:H+(aq)+OH-(aq)=H2O(l) ΔH= -57.3kJ/mol,若将含0.5mol H2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量大于57.3kJ |
| C.由C(石墨,s)=C(金刚石,s) ΔH= +1.9kJ/mol,可知石墨比金刚石稳定 |
D.已知H2(g)+Cl2(g)=2HCl(g) ΔH1= -184.6kJ/mol,则反应HCl(g)= H2(g)+ H2(g)+ Cl2(g)的ΔH= -92.3kJ/mol Cl2(g)的ΔH= -92.3kJ/mol |
您最近一年使用:0次

 ,强酸、强碱的稀溶液反应的中和热
,强酸、强碱的稀溶液反应的中和热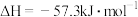 。则
。则 电离时的
电离时的 为
为





