Ⅰ.已知A、B、C、D四种可溶性物质,它们的阳离子可能分别是 、
、 、
、 、
、 中的某一种,阴离子可能分别是
中的某一种,阴离子可能分别是 、
、 、
、 、
、 中的某一种。
中的某一种。
①若把4种物质分别溶解于盛有蒸馏水的4支试管中,均得澄清溶液,只有B溶液呈蓝色。
②若向①的4支试管中分别加盐酸,C溶液中有沉淀产生,A溶液中有无色无味气体逸出。
(1)根据①②的事实推断B、C的化学式分别为_____ 、_____ 。
(2)写出少量D溶液与小苏打溶液反应的离子方程式_____ 。
Ⅱ.下面三个方法都可以用来制氯气:
①
②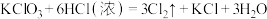
③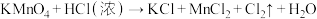 (未配平)
(未配平)
根据以上三个反应,回答下列有关问题:
(3)反应②中,氧化产物与还原产物的质量比为_____ 。
(4)若要制得相同质量的氯气,①②③反应中电子转移的数目之比为_____ 。
(5)请将反应③配平:_____ 。
_____ _____
_____ _____
_____ _____
_____ _____
_____ _____
_____ 。
。
(6)将离子方程式补充完成并配平:_____ 。
_____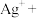 _____
_____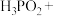 _____
_____ _____
_____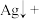 _____
_____ _____
_____
 、
、 、
、 、
、 中的某一种,阴离子可能分别是
中的某一种,阴离子可能分别是 、
、 、
、 、
、 中的某一种。
中的某一种。①若把4种物质分别溶解于盛有蒸馏水的4支试管中,均得澄清溶液,只有B溶液呈蓝色。
②若向①的4支试管中分别加盐酸,C溶液中有沉淀产生,A溶液中有无色无味气体逸出。
(1)根据①②的事实推断B、C的化学式分别为
(2)写出少量D溶液与小苏打溶液反应的离子方程式
Ⅱ.下面三个方法都可以用来制氯气:
①

②
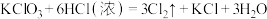
③
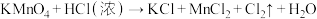 (未配平)
(未配平)根据以上三个反应,回答下列有关问题:
(3)反应②中,氧化产物与还原产物的质量比为
(4)若要制得相同质量的氯气,①②③反应中电子转移的数目之比为
(5)请将反应③配平:
_____
 _____
_____ _____
_____ _____
_____ _____
_____ _____
_____ 。
。(6)将离子方程式补充完成并配平:
_____
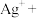 _____
_____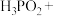 _____
_____ _____
_____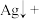 _____
_____ _____
_____
更新时间:2023-10-13 19:58:35
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下列为元素周期表中的一部分,用化学式或元素符号回答下列问题。
(1)③~⑤对应简单离子半径最大的离子是_______ ,其所对应元素在周期表中的位置是_______ 。
(2)③和⑤两元素按原子个数比1:1形成的化合物的电子式为_______ ,其中存在的化学键类型有_______ (填“离子键”、“极性键”、“非极性键”)。
(3)③和⑧形成的简单氢化物中,沸点较高的是:_______ (填化学式),原因是:_______ 。
(4)⑤和⑦最高价氧化物对应的水化物相互反应的离子方程式为:_______ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)③和⑤两元素按原子个数比1:1形成的化合物的电子式为
(3)③和⑧形成的简单氢化物中,沸点较高的是:
(4)⑤和⑦最高价氧化物对应的水化物相互反应的离子方程式为:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】软锰矿(主要成分是 ,含有
,含有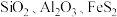 杂质)在生产中有广泛的应用。
杂质)在生产中有广泛的应用。
(1)过程Ⅰ:由软锰矿经酸浸、除杂等操作制备硫酸锰
①酸浸过程中,体系中有黄色沉淀产生,此过程中氧化剂与还原剂的比例为___________ 。
②生成的硫附着在矿粉颗粒表面使上述反应受阻,此时加入 可缓解上述问题,其原因为
可缓解上述问题,其原因为___________ 。
③ 也可以继续与
也可以继续与 反应,从而提高锰元素的浸出率,该反应的离子方程式是
反应,从而提高锰元素的浸出率,该反应的离子方程式是___________ 。
(2)过程Ⅲ:制备
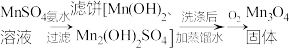
如图表示通入 时
时 随时间的变化。15~150分钟滤饼中一定参与反应的成分是
随时间的变化。15~150分钟滤饼中一定参与反应的成分是___________ ,判断的理由是___________ 。

(3)过程Ⅳ:制备
 难溶于水、能溶于强酸,可用
难溶于水、能溶于强酸,可用 溶液和
溶液和 溶液混合制备。每制得
溶液混合制备。每制得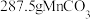 ,至少消耗
,至少消耗 溶液的体积为
溶液的体积为___________ L。
 ,含有
,含有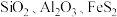 杂质)在生产中有广泛的应用。
杂质)在生产中有广泛的应用。| 软锰矿 (含 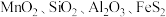 ) ) | Ⅱ | 锰钢原料: 单质 单质 | ||
| Ⅰ |  溶液 溶液 | Ⅲ | 软磁原料: | |
| Ⅳ | 锂电池电极原料: |
①酸浸过程中,体系中有黄色沉淀产生,此过程中氧化剂与还原剂的比例为
②生成的硫附着在矿粉颗粒表面使上述反应受阻,此时加入
 可缓解上述问题,其原因为
可缓解上述问题,其原因为③
 也可以继续与
也可以继续与 反应,从而提高锰元素的浸出率,该反应的离子方程式是
反应,从而提高锰元素的浸出率,该反应的离子方程式是(2)过程Ⅲ:制备

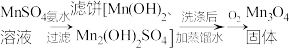
如图表示通入
 时
时 随时间的变化。15~150分钟滤饼中一定参与反应的成分是
随时间的变化。15~150分钟滤饼中一定参与反应的成分是
(3)过程Ⅳ:制备

 难溶于水、能溶于强酸,可用
难溶于水、能溶于强酸,可用 溶液和
溶液和 溶液混合制备。每制得
溶液混合制备。每制得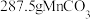 ,至少消耗
,至少消耗 溶液的体积为
溶液的体积为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】“价-类”二维图是我们认识物质性质、实现物质转化的重要工具,钠及其化合物的“价-类”二维图及部分转化关系如图所示,其中B为钠的另一种氧化物。

(1)B为___________ ,属于___________ (填“酸性氧化物”、“碱性氧化物”、“两性氧化物”);
(2)上述反应中属于氧化还原反应的是___________ (填序号);
(3)请写出②的离子方程式___________ ;
(4)纯碱和小苏打都是重要的化工原料,在生产和生活中有着广泛的应用。
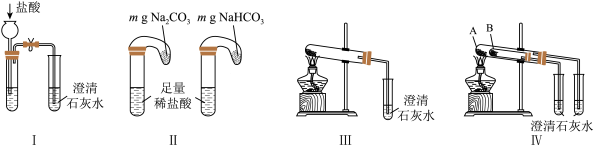
①只根据图Ⅰ、Ⅱ所示实验,能够达到鉴别目的的是___________ (填装置序号),对应的现象是___________ 。
②Ⅳ可用来鉴别Na2CO3和NaHCO3的稳定性,其中B中装的是___________ ,Ⅳ中受热处发生反应的化学方程式:___________ 。

(1)B为
(2)上述反应中属于氧化还原反应的是
(3)请写出②的离子方程式
(4)纯碱和小苏打都是重要的化工原料,在生产和生活中有着广泛的应用。
①只根据图Ⅰ、Ⅱ所示实验,能够达到鉴别目的的是
②Ⅳ可用来鉴别Na2CO3和NaHCO3的稳定性,其中B中装的是

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】某无色透明溶液,仅仅由 中的若干种离子组成,取适量该溶液进行如下实验:
中的若干种离子组成,取适量该溶液进行如下实验:

(1)不做任何实验,即可确定一定不含有的离子为_______ ,由实验①确定一定不含有的离子为_______ 。
(2)实验③确定一定不含有的离子为_______ 。
(3)设计实验方案检验可能存在的阴离子_______ 。
(4)若向原溶液中加入足量的 溶液,生成沉淀有
溶液,生成沉淀有_______ 种。
 中的若干种离子组成,取适量该溶液进行如下实验:
中的若干种离子组成,取适量该溶液进行如下实验:
(1)不做任何实验,即可确定一定不含有的离子为
(2)实验③确定一定不含有的离子为
(3)设计实验方案检验可能存在的阴离子
(4)若向原溶液中加入足量的
 溶液,生成沉淀有
溶液,生成沉淀有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】现有一包白色粉末,可能含有氯化钡、氯化钠、碳酸钾、硫酸钾、硫酸铜中的一种或几种,现做以下实验来确定粉末的成分
①将白色粉末溶于水,生成无色溶液和白色沉淀;
②过滤得到沉淀和滤液,将洗涤后的沉淀加入到稀硝酸中,发现沉淀全部溶解;
③向滤液中加入硝酸银溶液,发现生成了白色沉淀;
请回答下列问题:
(1)该白色粉末中一定含有___________ ,一定不含有___________
(2)写出②中发生的反应的化学方程式___________
(3)能否把②中的稀硝酸改成稀硫酸?并说明理由___________
①将白色粉末溶于水,生成无色溶液和白色沉淀;
②过滤得到沉淀和滤液,将洗涤后的沉淀加入到稀硝酸中,发现沉淀全部溶解;
③向滤液中加入硝酸银溶液,发现生成了白色沉淀;
请回答下列问题:
(1)该白色粉末中一定含有
(2)写出②中发生的反应的化学方程式
(3)能否把②中的稀硝酸改成稀硫酸?并说明理由
您最近一年使用:0次
【推荐3】去除粗盐中少量 、
、 和
和 的实验步骤如下:
的实验步骤如下:
Ⅰ.取一定量粗盐于烧杯中,加蒸馏水搅拌,使粗盐全部溶解,得到粗盐水。
Ⅱ.在粗盐水依次加入适当过量的试剂A、试剂B和试剂C,静置后过滤,除去沉淀,得到滤液。
Ⅲ.向所得滤液加盐酸,蒸发结晶可得到去除杂质离子的精盐。
提供的试剂:粗食盐、饱和 溶液、20%
溶液、20% 溶液、
溶液、
 溶液、
溶液、 盐酸、蒸馏水、pH试纸。
盐酸、蒸馏水、pH试纸。
请回答:
(1)步骤Ⅱ,试剂A、B、C分别是_______ 、 、
、_______ (只需填化学式)。
(2)步骤Ⅱ,证明 已沉淀完全的方法
已沉淀完全的方法_______ 。
(3)步骤Ⅲ,加入盐酸的目的_______ 。
(4)步骤Ⅲ,用_______ (填仪器名称)将蒸发皿夹持到陶土网上冷却。
 、
、 和
和 的实验步骤如下:
的实验步骤如下:Ⅰ.取一定量粗盐于烧杯中,加蒸馏水搅拌,使粗盐全部溶解,得到粗盐水。
Ⅱ.在粗盐水依次加入适当过量的试剂A、试剂B和试剂C,静置后过滤,除去沉淀,得到滤液。
Ⅲ.向所得滤液加盐酸,蒸发结晶可得到去除杂质离子的精盐。
提供的试剂:粗食盐、饱和
 溶液、20%
溶液、20% 溶液、
溶液、
 溶液、
溶液、 盐酸、蒸馏水、pH试纸。
盐酸、蒸馏水、pH试纸。请回答:
(1)步骤Ⅱ,试剂A、B、C分别是
 、
、(2)步骤Ⅱ,证明
 已沉淀完全的方法
已沉淀完全的方法(3)步骤Ⅲ,加入盐酸的目的
(4)步骤Ⅲ,用
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】现有金属单质 A 和气体甲、乙、丙及物质 B、C、D、E、F、G, 它们之间能发生如下反应,其中乙是黄绿色气体,图中有些反应的产物和反应的条件没有全部标出。
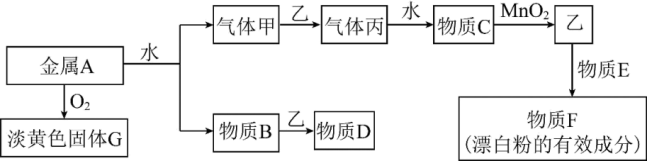
请根据以上信息回答下列问题:
(1)写出下列物质的名称:气体甲___________ ; 气体乙___________ ;
(2)写出下列物质的化学式:F___________ ; G:___________ ;
(3)写出固体 G 与二氧化碳反应的化学方程式___________ 。
(4)气体乙是一种重要的化工原料,在工农业生产、生活中有着重要的应用。请你根据所学知识回答下列问题:某化学兴趣小组计划用气体乙和物质 B 制取简易消毒液 D, 其反应原理为:(用离子方程式表示)___________ ;从氧化剂和还原剂的角度分析,该反应中乙的作 用是___________ 。

请根据以上信息回答下列问题:
(1)写出下列物质的名称:气体甲
(2)写出下列物质的化学式:F
(3)写出固体 G 与二氧化碳反应的化学方程式
(4)气体乙是一种重要的化工原料,在工农业生产、生活中有着重要的应用。请你根据所学知识回答下列问题:某化学兴趣小组计划用气体乙和物质 B 制取简易消毒液 D, 其反应原理为:(用离子方程式表示)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】氮在自然界中的转化是一个复杂的过程,氮循环是生态系统物质循环的重要组成部分。
(1)在一定条件下, 可用于脱除氮氧化物的烟气,其反应原理为
可用于脱除氮氧化物的烟气,其反应原理为 。该反应中的还原剂为
。该反应中的还原剂为_______ (填化学式)。
(2)氨的催化氧化是制备硝酸的重要过程,实验室按如图所示装置进行氨的催化氧化实验。

实验操作:将浓氨水倒入锥形瓶中,从导气管通入热空气,将红热的铂丝伸入锥形瓶中。
实验现象:a.红热的铂丝始终保持红热状态;b.瓶中有红棕色气体生成,瓶内还有白烟生成。
回答下列问题:
①铂丝始终保持红热状态的可能原因是_______
②请写出氨气的催化氧化反应的化学方程式:_______
③红棕色气体可用NaOH溶液吸收,有 和
和 生成,写出该反应的离子方程式:
生成,写出该反应的离子方程式:_______
(3)氨是氮循环中的重要物质,在人类的生产和生活中有着广泛的应用。高浓度的氨氮废水是造成河流及湖泊富营养化的主要因素,研究表明在微生物作用下,可实现 的转化。写出在碱性条件下,
的转化。写出在碱性条件下, 被氧气氧化为
被氧气氧化为 的反应的离子方程式:
的反应的离子方程式:_______
(4)每生成1mol ,转移的电子的物质的量为
,转移的电子的物质的量为_______ mol。
(1)在一定条件下,
 可用于脱除氮氧化物的烟气,其反应原理为
可用于脱除氮氧化物的烟气,其反应原理为 。该反应中的还原剂为
。该反应中的还原剂为(2)氨的催化氧化是制备硝酸的重要过程,实验室按如图所示装置进行氨的催化氧化实验。

实验操作:将浓氨水倒入锥形瓶中,从导气管通入热空气,将红热的铂丝伸入锥形瓶中。
实验现象:a.红热的铂丝始终保持红热状态;b.瓶中有红棕色气体生成,瓶内还有白烟生成。
回答下列问题:
①铂丝始终保持红热状态的可能原因是
②请写出氨气的催化氧化反应的化学方程式:
③红棕色气体可用NaOH溶液吸收,有
 和
和 生成,写出该反应的离子方程式:
生成,写出该反应的离子方程式:(3)氨是氮循环中的重要物质,在人类的生产和生活中有着广泛的应用。高浓度的氨氮废水是造成河流及湖泊富营养化的主要因素,研究表明在微生物作用下,可实现
 的转化。写出在碱性条件下,
的转化。写出在碱性条件下, 被氧气氧化为
被氧气氧化为 的反应的离子方程式:
的反应的离子方程式:(4)每生成1mol
 ,转移的电子的物质的量为
,转移的电子的物质的量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】NaNO2易溶于水,外观和食盐相似,有咸味,人误食会中毒。已知NaNO2能发生反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。请回答下列问题:
(1)上述反应中NaI___________ (填序号)。
①是氧化产物 ②是还原产物
③既不是氧化产物,又不是还原产物 ④既是氧化产物,又是还原产物
(2)某厂废液中含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是___________。
(3)NaNO2也可作为食品防腐剂,但由于亚硝酸钠具有一定的毒性,因此食品中用量和残留量均有严格规定。某实验小组欲用酸性KMnO4测定NaNO2样品纯度,所涉及到的反应有:
(a)
(b)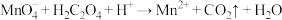
①配平反应(a),写出(a)的离子方程式___________ 。
②误食NaNO2会导致血红蛋白中的 转化为
转化为 而中毒,可服用维生素C解毒。下列分析错误的是
而中毒,可服用维生素C解毒。下列分析错误的是___________ 。
A.NaNO2被氧化 B.维生素C具有还原性
C.还原性:维生素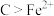 D.NaNO2是氧化剂
D.NaNO2是氧化剂
(4)用含铬不锈钢废渣(含SiO2、Cr2O3、Fe2O3、Al2O3等)制取Cr2O3(铬绿)的工艺流程如图所示:

回答下列问题:
①Cr2O3、KOH、O2反应生成K2CrO4的化学方程式为___________ 。
②“水浸”时,碱熔渣中的KFeO2强烈水解生成的难溶物为___________ (填化学式)。
③“还原”时发生反应的离子方程式为___________ 。
(1)上述反应中NaI
①是氧化产物 ②是还原产物
③既不是氧化产物,又不是还原产物 ④既是氧化产物,又是还原产物
(2)某厂废液中含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是___________。
| A.NaCl | B.NH4Cl | C.HNO3 | D.浓H2SO4 |
(3)NaNO2也可作为食品防腐剂,但由于亚硝酸钠具有一定的毒性,因此食品中用量和残留量均有严格规定。某实验小组欲用酸性KMnO4测定NaNO2样品纯度,所涉及到的反应有:
(a)

(b)
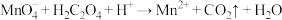
①配平反应(a),写出(a)的离子方程式
②误食NaNO2会导致血红蛋白中的
 转化为
转化为 而中毒,可服用维生素C解毒。下列分析错误的是
而中毒,可服用维生素C解毒。下列分析错误的是A.NaNO2被氧化 B.维生素C具有还原性
C.还原性:维生素
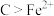 D.NaNO2是氧化剂
D.NaNO2是氧化剂(4)用含铬不锈钢废渣(含SiO2、Cr2O3、Fe2O3、Al2O3等)制取Cr2O3(铬绿)的工艺流程如图所示:

回答下列问题:
①Cr2O3、KOH、O2反应生成K2CrO4的化学方程式为
②“水浸”时,碱熔渣中的KFeO2强烈水解生成的难溶物为
③“还原”时发生反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D四种物质之间的转化关系如图所示(部分产物略去),根据所学知识回答下列问题:

(1)若A为NaAlO2溶液,写出A与过量B反应的离子方程式____ 。
(2)若A为Fe,B为稀HNO3,则反应①(还原产物为NO)中氧化剂与还原剂的物质的量之比为____ ,稀硝酸在反应过程中除了起氧化剂的作用外,还有____ 的作用。
(3)若A为Cl2,B为NH3,当NH3过量时,则二者相遇有白烟生成,写出反应①的化学方程式:_____ 。
(4)若A为1L0.1mol·L-1NaOH溶液,B为SO2,当向A中通入0.07molSO2气体时,溶液中的溶质为_____ (填化学式,下同)、____ ,物质的量分别为____ 、___ 。

(1)若A为NaAlO2溶液,写出A与过量B反应的离子方程式
(2)若A为Fe,B为稀HNO3,则反应①(还原产物为NO)中氧化剂与还原剂的物质的量之比为
(3)若A为Cl2,B为NH3,当NH3过量时,则二者相遇有白烟生成,写出反应①的化学方程式:
(4)若A为1L0.1mol·L-1NaOH溶液,B为SO2,当向A中通入0.07molSO2气体时,溶液中的溶质为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】氯及其化合物在工业生产生活中有很重要的作用。已知:实验室中可用KMnO4与浓盐酸发生如下反应:KMnO4+HCl(浓)—KCl+Cl2↑+H2O +MnCl2
(1)配平该反应______ ,该反应中氧化剂为____ ;氧化剂与还原剂的物质的量之比为____ ;
(2)标况下反应生成11.2L的Cl2,则该反应转移的电子的数目为_______ ;被氧化的HCl的物质的量为_______ mol,参加反应的HCl的物质的量为_______ mol。
(3)图中为实验室制取氯气及性质验证的装置图:

在装置D中可观察到的现象是_______ ,装置F中可观察到的现象是_______ ,装置G中发生的离子方程式_______ 。
(1)配平该反应
(2)标况下反应生成11.2L的Cl2,则该反应转移的电子的数目为
(3)图中为实验室制取氯气及性质验证的装置图:

在装置D中可观察到的现象是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】钒铬还原渣是钠化提钒过程的固体废弃物,其主要成分为VO2·xH2O、Cr(OH)3及少量的SiO2.一种初步分离钒铬还原渣中钒铬并获得Na2Cr2O7的工艺流程如下:

已知:①“酸浸”后VO2·xH2O转化为VO2+;②Cr(OH)3的Ksp近似为1×10-30;③ 有关物质的溶解度(g/100 g H2O)如下表所示:
回答下列问题:
(1)“氧化”生成VO ,发生反应的离子方程式为
,发生反应的离子方程式为___________ 。
(2)若“含Cr3+净化液”中c(Cr3+)=0.1 mol/L,则“水解沉钒”调pH的范围是2.5~___________ 。
(3)“溶液1”中含CrO ,加入H2O2后发生反应的离子方程式为
,加入H2O2后发生反应的离子方程式为___________ ,该反应中氧化剂与还原剂的物质的量之比为___________ 。
(4)经“多步操作”得两种晶体,则“多步操作”包括蒸发浓缩、___________ 、冷却结晶、过滤、洗涤等步骤。
(5)研究温度对Na2S2O8与H2O2的氧化—水解沉钒率的影响,得到如图所示结果。

钒铬还原渣酸浸液初始温度在90 ℃左右,降低温度能耗增加。由图可知,分别采用H2O2、Na2S2O8进行“氧化”时,应选择的适宜温度分别是___________ 、___________ ,与Na2S2O8相比,采用H2O2氧化的主要不足之处有___________ (写出两点)。

已知:①“酸浸”后VO2·xH2O转化为VO2+;②Cr(OH)3的Ksp近似为1×10-30;③ 有关物质的溶解度(g/100 g H2O)如下表所示:
| 温度/℃ | 20 | 40 | 60 | 80 | 100 |
| Na2Cr2O7 | 183.6 | 215.1 | 269.2 | 376.4 | 415.0 |
| Na2SO4 | 19.5 | 48.8 | 45.3 | 43.7 | 42.5 |
回答下列问题:
(1)“氧化”生成VO
 ,发生反应的离子方程式为
,发生反应的离子方程式为(2)若“含Cr3+净化液”中c(Cr3+)=0.1 mol/L,则“水解沉钒”调pH的范围是2.5~
(3)“溶液1”中含CrO
 ,加入H2O2后发生反应的离子方程式为
,加入H2O2后发生反应的离子方程式为(4)经“多步操作”得两种晶体,则“多步操作”包括蒸发浓缩、
(5)研究温度对Na2S2O8与H2O2的氧化—水解沉钒率的影响,得到如图所示结果。

钒铬还原渣酸浸液初始温度在90 ℃左右,降低温度能耗增加。由图可知,分别采用H2O2、Na2S2O8进行“氧化”时,应选择的适宜温度分别是
您最近一年使用:0次



