已知: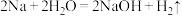 ,将
,将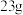 钠与过量的重水
钠与过量的重水 反应,产生气体的质量是
反应,产生气体的质量是___________ 。
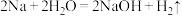 ,将
,将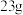 钠与过量的重水
钠与过量的重水 反应,产生气体的质量是
反应,产生气体的质量是
更新时间:2023-10-18 15:00:57
|
相似题推荐
计算题
|
较易
(0.85)
名校
解题方法
【推荐1】(1)正常人的血液中葡萄糖(简称血糖,化学式为C6H12O6)的浓度在3.61-6.11 m mol / L之间,今测得某病人1mL血液中含葡萄糖0.60 mg,相当于_____________ mmol / L,他的血糖属正常、偏高还是偏低?________________ ;
(2)标准状况下11.2L,由CO和H2组成的混合气体的质量为7.2g,则混合气体的平均摩尔质量为___ ,如果此混合气体完全燃烧消耗氧气的物质的量为___ mol。
(2)标准状况下11.2L,由CO和H2组成的混合气体的质量为7.2g,则混合气体的平均摩尔质量为
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐2】某实验小组以 溶液为原料制备
溶液为原料制备 ,并用重量法测定产品中
,并用重量法测定产品中 的含量。设计了如下实验方案:
的含量。设计了如下实验方案:
步骤2,产品中 的含量测定
的含量测定
①称取产品 ,用
,用 水溶解,酸化,加热至近沸;
水溶解,酸化,加热至近沸;
②在不断搅拌下,向①所得溶液逐滴加入热的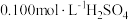 溶液,
溶液,
③沉淀完全后, 水浴40分钟,经过滤、洗涤、烘干等步骤,称量白色固体,质量为
水浴40分钟,经过滤、洗涤、烘干等步骤,称量白色固体,质量为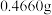 。
。
产品中 的质量分数为
的质量分数为_______ (保留三位有效数字)。
 溶液为原料制备
溶液为原料制备 ,并用重量法测定产品中
,并用重量法测定产品中 的含量。设计了如下实验方案:
的含量。设计了如下实验方案:步骤2,产品中
 的含量测定
的含量测定①称取产品
 ,用
,用 水溶解,酸化,加热至近沸;
水溶解,酸化,加热至近沸;②在不断搅拌下,向①所得溶液逐滴加入热的
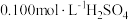 溶液,
溶液,③沉淀完全后,
 水浴40分钟,经过滤、洗涤、烘干等步骤,称量白色固体,质量为
水浴40分钟,经过滤、洗涤、烘干等步骤,称量白色固体,质量为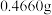 。
。产品中
 的质量分数为
的质量分数为
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐1】计算并填空
(1)5.75g Na与水反应,得到200mL溶液。在标准状况下,生成的氢气的体积为__________ ;得到溶液的物质的量浓度为__________ 。
(2)已知,11.6g CO和 的混合物的总物质的量为0.3mol。
的混合物的总物质的量为0.3mol。
①计算混合气体的平均摩尔质量为__________ (小数点后保留一位有效数字);
②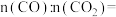
__________ 。
③将此混合气体通入 溶液中,若恰好得到
溶液中,若恰好得到 溶液,需要的NaOH溶液体积为
溶液,需要的NaOH溶液体积为__________ L。
(1)5.75g Na与水反应,得到200mL溶液。在标准状况下,生成的氢气的体积为
(2)已知,11.6g CO和
 的混合物的总物质的量为0.3mol。
的混合物的总物质的量为0.3mol。①计算混合气体的平均摩尔质量为
②
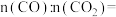
③将此混合气体通入
 溶液中,若恰好得到
溶液中,若恰好得到 溶液,需要的NaOH溶液体积为
溶液,需要的NaOH溶液体积为
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐2】取4.6克的钠投入水中,完全反应后问:
(1)生成的气体体积在标准状态下为多少升____________ ?
(2)生成的溶质的质量是多少____________ ?
(1)生成的气体体积在标准状态下为多少升
(2)生成的溶质的质量是多少
您最近一年使用:0次



