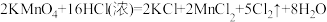完成下列有关物质的量的相关计算
(1)等质量的NH3和CH4,分子个数比为___________ ,同温同压下,等体积的CO2和O2密度比为___________ 。
(2)S燃烧时有SO2生成,其原理为:S+O2 SO2,若转移2.408×1024个电子,则生成的SO2的物质的量是
SO2,若转移2.408×1024个电子,则生成的SO2的物质的量是___________ 。
(3)在标准状况下,224mL CO2恰好与20mL NaOH溶液反应生成NaHCO3,则此NaOH溶液中n(NaOH)为___________ 。
(4)氢气是一种清洁能源,甲烷制氢的化学方程式为CH4+O2=CO2+2H2.在标准状况下,CH4与一定量的O2中恰好完全反应,反应后测得生成物的体积是672mL,则生成H2___________ mol,消耗的O2的体积是___________ 。
(1)等质量的NH3和CH4,分子个数比为
(2)S燃烧时有SO2生成,其原理为:S+O2
 SO2,若转移2.408×1024个电子,则生成的SO2的物质的量是
SO2,若转移2.408×1024个电子,则生成的SO2的物质的量是(3)在标准状况下,224mL CO2恰好与20mL NaOH溶液反应生成NaHCO3,则此NaOH溶液中n(NaOH)为
(4)氢气是一种清洁能源,甲烷制氢的化学方程式为CH4+O2=CO2+2H2.在标准状况下,CH4与一定量的O2中恰好完全反应,反应后测得生成物的体积是672mL,则生成H2
更新时间:2023-10-22 13:26:38
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】(1)同温同压下,同体积的甲烷( )和氨气(
)和氨气( )物质的量之比为
)物质的量之比为______ ,原子总数之比为________ ,密度之比为________ 。
(2)在标准状况下,CO和 的混合气体共39.2L,质量为59.5g,则CO和
的混合气体共39.2L,质量为59.5g,则CO和 的物质的量之比为
的物质的量之比为________ ,其中 体积分数为
体积分数为________ ,混合气体的摩尔质量为________ 。
(3)将 固体溶于水配成250mL溶液,取出10mL溶液加水稀释到100nL,稀释后溶液中NaOH的物质的量浓度为
固体溶于水配成250mL溶液,取出10mL溶液加水稀释到100nL,稀释后溶液中NaOH的物质的量浓度为________ mol/L;向稀释后的溶液中加入100ml 0.01mol/L 溶液(假设混合后溶液体积等于两溶液体积之和),混合后
溶液(假设混合后溶液体积等于两溶液体积之和),混合后 的物质的量浓度为
的物质的量浓度为________ mo/L。
 )和氨气(
)和氨气( )物质的量之比为
)物质的量之比为(2)在标准状况下,CO和
 的混合气体共39.2L,质量为59.5g,则CO和
的混合气体共39.2L,质量为59.5g,则CO和 的物质的量之比为
的物质的量之比为 体积分数为
体积分数为(3)将
 固体溶于水配成250mL溶液,取出10mL溶液加水稀释到100nL,稀释后溶液中NaOH的物质的量浓度为
固体溶于水配成250mL溶液,取出10mL溶液加水稀释到100nL,稀释后溶液中NaOH的物质的量浓度为 溶液(假设混合后溶液体积等于两溶液体积之和),混合后
溶液(假设混合后溶液体积等于两溶液体积之和),混合后 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】三硝酸甘油酯[C3H5(ONO2)3]是一种炸药,可因撞击而爆炸,同时产生高温。爆炸按下式进行:4C3H5(ONO2)3→wN2+xCO2+yH2O+zO2(式中w,x,y,z为化学计量数)。科学实验证明:相同条件(温度、压力)下相同体积的不同气体所含分子数相等。当三硝酸甘油酯爆炸并恢复到常温时,所得气体的体积比为____ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】(1)当CO、CO2的分子个数之比为1∶1时,原子总数之比为________ ,质量之比为________ 。
(2)中和含0.2 mol HCl的稀盐酸,需NaOH的质量为________ g。
(3)将5 mol·L-1的Mg(NO3)2溶液a mL稀释至b mL,稀释后溶液中NO3-的物质的量浓度是______ mol·L-1。
(4)同温同压下,同体积的氨气和H2S气体的质量之比为________ ;同质量的氨气和硫化氢气体的体积之比为________ ;若二者氢原子数相等,则它们的体积之比为________ 。
(2)中和含0.2 mol HCl的稀盐酸,需NaOH的质量为
(3)将5 mol·L-1的Mg(NO3)2溶液a mL稀释至b mL,稀释后溶液中NO3-的物质的量浓度是
(4)同温同压下,同体积的氨气和H2S气体的质量之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】CaCO3加热分解时的失重百分比为___________ ; 1mol 过氧化钠与水充分反应生成过氧化氢的质量是___________ ; 超氧化钠NaO2与CO2的反应可以类比于过氧化钠与CO2的反应。1molNaO2与CO2充分反应后放出的气体的体积是___________ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】将一定质量的镁铝混合物投入200mL硫酸中,固体全部溶解后,向所得溶液中加入5mol/L的NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如图所示。

(1)写出bc段发生的化学反应方程式___ ;
(2)镁和铝的总质量为___ g;
(3)b点溶液中的溶质为___ ,硫酸的物质的量浓度为___ mol/L;
(4)生成的氢气在标准状况下的体积为___ L;
(5)c点溶液中通入足量的CO2的反应化学方程式为___ 。

(1)写出bc段发生的化学反应方程式
(2)镁和铝的总质量为
(3)b点溶液中的溶质为
(4)生成的氢气在标准状况下的体积为
(5)c点溶液中通入足量的CO2的反应化学方程式为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】将1.00mol/L 硫酸铜溶液和2.00 mol/L 硫酸铁溶液按体积比1:2混合得到1L混合液(假设混合溶液的体积等于混合前两种溶液的体积之和),再向其中加入足量的铁粉,经过足够长的时间后,铁粉有剩余。请计算(计算结果保留两位小数):
(1)混合后溶液中铜离子的物质的量浓度为_______ mol/L。
(2)溶解的铁粉的质量为_______ g。
(3)最后硫酸亚铁的物质的量浓度为_______ mol/L。
(1)混合后溶液中铜离子的物质的量浓度为
(2)溶解的铁粉的质量为
(3)最后硫酸亚铁的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】请写出简单的计算过程。
(1)在空气中煅烧CoC2O4生成钴氧化物和CO2,测得充分煅烧后固体质量为2.41 g,CO2 体积为1.344 L(标准状况),则钴氧化物的化学式为_____________ 。
(2)将一定量Fe、FeO 和 Fe2O3 的混合物放入25 mL 2 mol·L-1 的HNO3溶液中,反应完全后,无固体剩余,生成 224 mL NO 气体(标准状况),再向反应后的溶液中加入1mol·L-1 的 NaOH 溶液,要使铁元素全部沉淀下来,所加 NaOH 溶液的体积最少是__________________ 。
(3)取Ce(OH)4产品5.000g,加酸溶解后,向其中加入含0.03300molFeSO4的FeSO4溶液使Ce4+全部被还原成Ce3+,再用0.1000mol·L-1的酸性KMnO4标准溶液滴定至终点时,消耗20.00mL标准溶液。则该产品中Ce(OH)4的质量分数为________________ 。(已知氧化性:Ce4+>KMnO4;Ce(OH)4的相对分子质量为208)。
(1)在空气中煅烧CoC2O4生成钴氧化物和CO2,测得充分煅烧后固体质量为2.41 g,CO2 体积为1.344 L(标准状况),则钴氧化物的化学式为
(2)将一定量Fe、FeO 和 Fe2O3 的混合物放入25 mL 2 mol·L-1 的HNO3溶液中,反应完全后,无固体剩余,生成 224 mL NO 气体(标准状况),再向反应后的溶液中加入1mol·L-1 的 NaOH 溶液,要使铁元素全部沉淀下来,所加 NaOH 溶液的体积最少是
(3)取Ce(OH)4产品5.000g,加酸溶解后,向其中加入含0.03300molFeSO4的FeSO4溶液使Ce4+全部被还原成Ce3+,再用0.1000mol·L-1的酸性KMnO4标准溶液滴定至终点时,消耗20.00mL标准溶液。则该产品中Ce(OH)4的质量分数为
您最近一年使用:0次