随原子序数的递增,八种短周期元素(用英文小写字母表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。
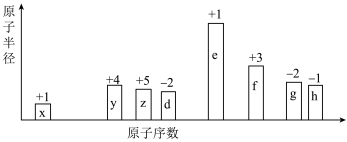
根据判断出的元素回答问题:
(1)g在元素周期表的位置是_______ 。
(2)比较d、f简单离子的半径大小(用化学式表示,下同)_______ ,比较g、h最高价氧化物对应水化物酸性_______ 。
(3)d的氢化物沸点高于y的氢化物沸点的原因_______ 。
(4)写出f的最高价氧化物对应的水化物与h的最高价氧化物对应的水化物反应的离子方程式_______ 。
(5)由元素f、h形成的物质X与由元素x、z形成的化合物Y可发生以下反应:
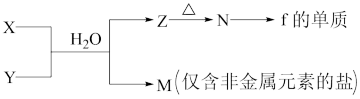
①写出M的电子式_______ 。
②写出X溶液与Y溶液反应的离子方程式_______ 。

根据判断出的元素回答问题:
(1)g在元素周期表的位置是
(2)比较d、f简单离子的半径大小(用化学式表示,下同)
(3)d的氢化物沸点高于y的氢化物沸点的原因
(4)写出f的最高价氧化物对应的水化物与h的最高价氧化物对应的水化物反应的离子方程式
(5)由元素f、h形成的物质X与由元素x、z形成的化合物Y可发生以下反应:

①写出M的电子式
②写出X溶液与Y溶液反应的离子方程式
更新时间:2023-09-27 20:50:28
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】根据①~⑩号元素所在周期表中的位置,回答下列问题:

(1)⑨形成的简单离子结构示意图为___________ 。
(2)用电子式表示⑤和⑩形成原子数目比为1:2的化合物的形成过程___________ 。
(3)②③④三种元素分别形成简单离子的离子半径由大到小的顺序是_________ (填离子符号)。
(4)①和⑧构成的化合物能和水剧烈反应产生氢气,该反应的化学方程式为___________ 。
(5)⑥的单质与④的最高价氧化物对应水化物反应的离子方程式为___________ 。
(6)②和⑦相比非金属性较强的是___________ (填元素符号),下列能证明这一事实的有___________ (填序号)。
A.⑦的简单氢化物稳定性强于②的简单氢化物
B.⑦的简单氢化物酸性强于②的简单氢化物
C.⑦单质与氢气反应比②单质与氢气反应更加剧烈
D.⑦单质的熔点比②单质的低
(7)运用元素周期律推测陌生元素的性质,下列推断错误的是___________(填序号)

(1)⑨形成的简单离子结构示意图为
(2)用电子式表示⑤和⑩形成原子数目比为1:2的化合物的形成过程
(3)②③④三种元素分别形成简单离子的离子半径由大到小的顺序是
(4)①和⑧构成的化合物能和水剧烈反应产生氢气,该反应的化学方程式为
(5)⑥的单质与④的最高价氧化物对应水化物反应的离子方程式为
(6)②和⑦相比非金属性较强的是
A.⑦的简单氢化物稳定性强于②的简单氢化物
B.⑦的简单氢化物酸性强于②的简单氢化物
C.⑦单质与氢气反应比②单质与氢气反应更加剧烈
D.⑦单质的熔点比②单质的低
(7)运用元素周期律推测陌生元素的性质,下列推断错误的是___________(填序号)
| A.铊(Tl)单质既能与盐酸作用产生氢气,又能与NaOH溶液反应放出氢气 |
| B.砹(At)单质为有色固体,HAt不稳定,AgAt不溶于水也不溶于稀硝酸 |
C.锂(Li)单质在氧气中剧烈燃烧,产物是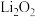 |
D.硫酸锶( )是难溶于水的白色固体 )是难溶于水的白色固体 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】有 、
、 、
、 、
、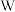 四种元素,它们的核电荷数依次增大。已知:
四种元素,它们的核电荷数依次增大。已知:
① 原子最外层电子数是次外层电子数的2倍。
原子最外层电子数是次外层电子数的2倍。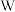 原子
原子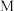 层上的电子比
层上的电子比 层多5个。
层多5个。
② 的负离子与氖原子的电子层结构相同。标准状况时
的负离子与氖原子的电子层结构相同。标准状况时 可形成
可形成 气体,经测定
气体,经测定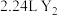 气体为
气体为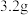 。
。
③ 与
与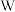 可形成化合物
可形成化合物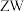 ,
, 该化合物中含质子数
该化合物中含质子数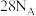 。请回答:
。请回答:
(1)写出 各元素的名称:
各元素的名称:
_______ 、
_______ 、
_______ 、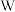
_______ 。
(2)写出下列微粒的结构示意图或电子式。
① 的原子的结构示意图
的原子的结构示意图_______
② 的负离子结构示意图
的负离子结构示意图_______
③ 的正离子电子式
的正离子电子式_______
④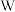 的负离子的电子式
的负离子的电子式_______
 、
、 、
、 、
、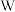 四种元素,它们的核电荷数依次增大。已知:
四种元素,它们的核电荷数依次增大。已知:①
 原子最外层电子数是次外层电子数的2倍。
原子最外层电子数是次外层电子数的2倍。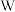 原子
原子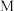 层上的电子比
层上的电子比 层多5个。
层多5个。②
 的负离子与氖原子的电子层结构相同。标准状况时
的负离子与氖原子的电子层结构相同。标准状况时 可形成
可形成 气体,经测定
气体,经测定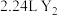 气体为
气体为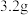 。
。③
 与
与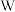 可形成化合物
可形成化合物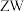 ,
, 该化合物中含质子数
该化合物中含质子数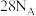 。请回答:
。请回答:(1)写出
 各元素的名称:
各元素的名称:


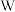
(2)写出下列微粒的结构示意图或电子式。
①
 的原子的结构示意图
的原子的结构示意图②
 的负离子结构示意图
的负离子结构示意图③
 的正离子电子式
的正离子电子式④
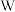 的负离子的电子式
的负离子的电子式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】X、Y、Z、W是元素周期表前四周期中的常见元素,其相关信息如下表:
(1)W位于元素周期表第_____ 周期第______ 族,其原子最外层有____ 个电子。
(2)X的活泼性比Y的_____ (填“强”或“弱”);X和Y的气态氢化物中,较稳定的是____ (写化学式)。
(3)写出Z2Y2的电子式________________ ,XY2的结构式__________________ 。
(4)在X原子与氢原子形成的多种分子中,有些分子的核磁共振氢谱显示有两种氢,写出其中一种分子的名称______________ 。氢元素、X、Y的原子也可共同形成多种分子和某种常见无机阴离子,写出其中一种分子与该无机阴离子反应的离子方程式________________ 。
元素 | 相关信息 |
X | X原子的L层电子数是K层电子数的2倍 |
Y | Y原子的最外层电子排布式为:nsnnpn+2 |
Z | Z存在质量数为23,中子数为12的原子核 |
W | W有多种化合价,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色 |
(2)X的活泼性比Y的
(3)写出Z2Y2的电子式
(4)在X原子与氢原子形成的多种分子中,有些分子的核磁共振氢谱显示有两种氢,写出其中一种分子的名称
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
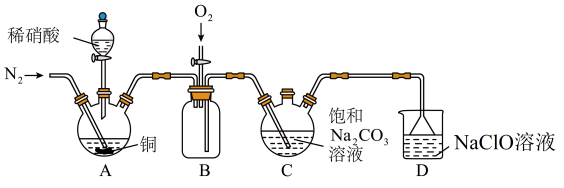
【推荐1】亚硝酸钠NaNO2主要用于医药、染料和漂白等行业,也常用于食品保鲜剂。某小组拟利用氮氧化物制备产品NaNO2。
已知: ,
,
回答下列问题:
(1)实验室制取N2有多种方法,请根据元素化合物知识和氧化还原反应相关理论,结合下列供选试剂和如图装置(净化装置略去),选出一种可行的方法,写出化学方程式___________ 。
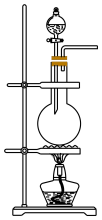
【可供选择的试剂:CuO(s)、NH3(g)、Cl2(g)、O2(g)、饱和NaNO2(aq)、饱和NH4Cl(aq)】
实验时装置B中应间断性通入适量的O2,其目的是___________ 。
(2)装置A中盛装稀硝酸的仪器的名称是___________ ;NO不能单独被纯碱溶液吸收,若要使氮的氧化物完全被纯碱溶液吸收且产品纯度最高,则n(NO):n(NO2)=___________ 。
(3)装置D中倒置漏斗的作用是___________ ,NaClO将NO氧化成NO ,写出该反应的离子方程式
,写出该反应的离子方程式___________ 。工业上也用NaClO溶液吸收硝酸尾气,其他条件相同,加入稀盐酸调节NaClO溶液pH会促进NO转化为NO ,原因是
,原因是___________ 。
(4)设计实验探究NaNO2的性质。实验完毕后,从装置C中分离出NaNO2固体粗产品,取少量上述产品配制成溶液,分成2份分别进行甲、乙两组实验,实验操作及现象、结论如表。
①上述实验___________ (填标号)的结论不可靠,理由是___________ 。
②经实验测得实验乙反应后的溶液中氮元素仅以NO 的形式存在,酸性KMnO4溶液与NO
的形式存在,酸性KMnO4溶液与NO 反应的离子方程式为
反应的离子方程式为___________ 。

已知:
 ,
,
回答下列问题:
(1)实验室制取N2有多种方法,请根据元素化合物知识和氧化还原反应相关理论,结合下列供选试剂和如图装置(净化装置略去),选出一种可行的方法,写出化学方程式

【可供选择的试剂:CuO(s)、NH3(g)、Cl2(g)、O2(g)、饱和NaNO2(aq)、饱和NH4Cl(aq)】
实验时装置B中应间断性通入适量的O2,其目的是
(2)装置A中盛装稀硝酸的仪器的名称是
(3)装置D中倒置漏斗的作用是
 ,写出该反应的离子方程式
,写出该反应的离子方程式 ,原因是
,原因是(4)设计实验探究NaNO2的性质。实验完毕后,从装置C中分离出NaNO2固体粗产品,取少量上述产品配制成溶液,分成2份分别进行甲、乙两组实验,实验操作及现象、结论如表。
| 实验操作及现象 | 结论 | |
| 甲 | 滴加少量酸性KI-淀粉溶液,振荡,溶液变蓝 | 酸性条件下NO 具有氧化性 具有氧化性 |
| 乙 | 滴加少量酸性KMnO4溶液,振荡,紫色褪去 | 酸性条件下NO 具有还原性 具有还原性 |
②经实验测得实验乙反应后的溶液中氮元素仅以NO
 的形式存在,酸性KMnO4溶液与NO
的形式存在,酸性KMnO4溶液与NO 反应的离子方程式为
反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】碳酸锰(MnCO3)是制造电信器材的软磁铁氧体,也用作脱硫的催化剂,瓷釉、涂料和清漆的颜料。工业上利用软锰矿(主要成分是 ,还含有
,还含有 、
、 、CuO等杂质)制取碳酸锰的流程如下图所示:
、CuO等杂质)制取碳酸锰的流程如下图所示:

已知:①还原焙烧的主反应为
②氧化能力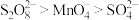
可能用到的数据如下:
根据要求回答下列问题:
(1)基态锰原子的价层电子排布式为_______ , 中存在过氧键(—O—O—),请问
中存在过氧键(—O—O—),请问 中S的化合价为
中S的化合价为_______ 。
(2)在实验室进行步骤A操作时,可能用到的主要仪器为_______ 。
A.坩埚 B.蒸发皿 C.烧杯
(3)步骤E中调节 ,其目的是
,其目的是_______ 。
(4)步骤G发生的离子方程式为_______ ,若 恰好沉淀完全时测得溶液中
恰好沉淀完全时测得溶液中 的浓度为
的浓度为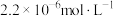 ,则
,则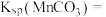
_______ 。
(5)实验室可以用 溶液来检验
溶液来检验 是否完全发生反应,请写出对应的离子方程式
是否完全发生反应,请写出对应的离子方程式_______ 。
 ,还含有
,还含有 、
、 、CuO等杂质)制取碳酸锰的流程如下图所示:
、CuO等杂质)制取碳酸锰的流程如下图所示:
已知:①还原焙烧的主反应为

②氧化能力
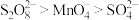
可能用到的数据如下:
| 氢氧化物 |  |  |  |  |
| 开始沉淀pH | 1.5 | 6.5 | 4.2 | 8.3 |
| 沉淀完全pH | 3.7 | 9.7 | 7.4 | 9.8 |
(1)基态锰原子的价层电子排布式为
 中存在过氧键(—O—O—),请问
中存在过氧键(—O—O—),请问 中S的化合价为
中S的化合价为(2)在实验室进行步骤A操作时,可能用到的主要仪器为
A.坩埚 B.蒸发皿 C.烧杯
(3)步骤E中调节
 ,其目的是
,其目的是(4)步骤G发生的离子方程式为
 恰好沉淀完全时测得溶液中
恰好沉淀完全时测得溶液中 的浓度为
的浓度为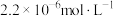 ,则
,则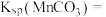
(5)实验室可以用
 溶液来检验
溶液来检验 是否完全发生反应,请写出对应的离子方程式
是否完全发生反应,请写出对应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域,且温度不同, 和碱的反应产物也不同。实验室中利用如图装置(部分装置省略)制备
和碱的反应产物也不同。实验室中利用如图装置(部分装置省略)制备 和
和 ,探究其氧化还原性质。
,探究其氧化还原性质。

回答下列问题:
(1)实验前必须进行的操作是___________ 。
(2)盛放浓盐酸的仪器名称是___________ ,a中的试剂为___________ 。
(3)该实验中制备 的化学方程式为:
的化学方程式为:___________ ,c中化学反应的离子方程式是___________ 。
(4)d中可选用试剂___________(填标号)。
(5)取少量 和
和 溶液分别置于1号和2号试管中,滴加淀粉
溶液分别置于1号和2号试管中,滴加淀粉 溶液。1号试管溶液颜色不变,2号试管溶液变为蓝色,可知该条件下
溶液。1号试管溶液颜色不变,2号试管溶液变为蓝色,可知该条件下 的氧化能力
的氧化能力___________ (填“大于”或“小于”) 。
。
(6)若反应结束后,取出b中试管,经冷却结晶、过滤、少量冷水洗涤、干燥,得到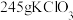 晶体,标况下b试管中消耗
晶体,标况下b试管中消耗 的体积为
的体积为___________ 。
 和碱的反应产物也不同。实验室中利用如图装置(部分装置省略)制备
和碱的反应产物也不同。实验室中利用如图装置(部分装置省略)制备 和
和 ,探究其氧化还原性质。
,探究其氧化还原性质。
回答下列问题:
(1)实验前必须进行的操作是
(2)盛放浓盐酸的仪器名称是
(3)该实验中制备
 的化学方程式为:
的化学方程式为:(4)d中可选用试剂___________(填标号)。
A. 溶液 溶液 | B. 溶液 溶液 | C. 溶液 溶液 | D.稀 |
(5)取少量
 和
和 溶液分别置于1号和2号试管中,滴加淀粉
溶液分别置于1号和2号试管中,滴加淀粉 溶液。1号试管溶液颜色不变,2号试管溶液变为蓝色,可知该条件下
溶液。1号试管溶液颜色不变,2号试管溶液变为蓝色,可知该条件下 的氧化能力
的氧化能力 。
。(6)若反应结束后,取出b中试管,经冷却结晶、过滤、少量冷水洗涤、干燥,得到
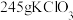 晶体,标况下b试管中消耗
晶体,标况下b试管中消耗 的体积为
的体积为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】题目
(1)A、B、C、D、E六种短周期元素的原子序数依次增大。已知A、C、E三原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水,D元素原子的次外层电子数比最外层电子数多3个。试回答:
①写出下列元素的符号A___________ ,C___________ ;
②用电子式表示B、E形成的化合物___________ ;
③D的一种单质D4难溶于水,易溶于CS2,请解释原因__________________ 。
(2)X、Y、Z、W四种前四周期元素的原子序数依次递增。X元素属于非金属,且X原子核外各能级上的电子数相等;Y原子核外的p电子数比X原子核外的p电子数多2个,Z原子核外最外层的p电子是最外层的s电子的2倍,W元素的基态原子在前四周期中未成对电子数最多。试回答:
①写出W元素的名称_______ ,X、Y两元素形成的非极性分子的结构式___________ 。
②X、Z元素的最高价氧化物对应水化物的酸性强弱为____ <_____ (用化学式表示)。
③X、Y、Z这三种元素原子半径的大小为_____ >______ >______ (填元素符号)。
(1)A、B、C、D、E六种短周期元素的原子序数依次增大。已知A、C、E三原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水,D元素原子的次外层电子数比最外层电子数多3个。试回答:
①写出下列元素的符号A
②用电子式表示B、E形成的化合物
③D的一种单质D4难溶于水,易溶于CS2,请解释原因
(2)X、Y、Z、W四种前四周期元素的原子序数依次递增。X元素属于非金属,且X原子核外各能级上的电子数相等;Y原子核外的p电子数比X原子核外的p电子数多2个,Z原子核外最外层的p电子是最外层的s电子的2倍,W元素的基态原子在前四周期中未成对电子数最多。试回答:
①写出W元素的名称
②X、Z元素的最高价氧化物对应水化物的酸性强弱为
③X、Y、Z这三种元素原子半径的大小为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】表中列出了①~⑦七种元素在周期表中的位置。请按要求回答:
(1)七种元素中,原子半径最大的是_______ (填元素符号)。
(2)③与⑦的简单氢化物中,稳定性好的是(填化学式,下同)_______ ,沸点高的是_______ ,沸点高的原因是_______ 。
(3)元素②形成的一种氢化物常用作火箭燃料,则该物质的电子式为_______ 。
(4)元素④的最高价氧化物对应的水化物与元素⑤的最高价氧化物对应的水化物发生反应的离子方程式为_______ 。
(5)由①、②、③三种元素组成的离子化合物是_______ ,检验该化合物中阳离子的方法是_______ 。
(6)含有上述元素的物质间存在如图转化。

 所含的化学键类型是
所含的化学键类型是_______ ,实验室检验 是否为离子化合物的方法
是否为离子化合物的方法_______ 。
族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ |
(2)③与⑦的简单氢化物中,稳定性好的是(填化学式,下同)
(3)元素②形成的一种氢化物常用作火箭燃料,则该物质的电子式为
(4)元素④的最高价氧化物对应的水化物与元素⑤的最高价氧化物对应的水化物发生反应的离子方程式为
(5)由①、②、③三种元素组成的离子化合物是
(6)含有上述元素的物质间存在如图转化。

 所含的化学键类型是
所含的化学键类型是 是否为离子化合物的方法
是否为离子化合物的方法
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下图为元素周期表的一部分,请用相关化学用语回答下列问题。
(1)④、⑤、⑥的原子半径由大到小的顺序是_______ 。
(2)②、③、⑧的最高价氧化物对应水化物酸性最强的分子式是_______ 。
(3)⑥的离子结构示意图为_______ 。
(4)⑤、⑥最高价氧化物对应水合物反应的离子方程式为_______ 。
(5)写出下列物质的电子式或结构式:
①④⑤组成化合物电子式:_______ ;②最高价氧化物电子式:_______ ;③单质结构式:_______ 。
| 族 周期 | IA | 0 | |||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | ||
| 2 | …… | ② | ③ | ④ | |||||
| 3 | ⑤ | …… | ⑥ | ⑦ | ⑧ | ||||
(2)②、③、⑧的最高价氧化物对应水化物酸性最强的分子式是
(3)⑥的离子结构示意图为
(4)⑤、⑥最高价氧化物对应水合物反应的离子方程式为
(5)写出下列物质的电子式或结构式:
①④⑤组成化合物电子式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E五种短周期元素,原子序数依次增大,A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y,A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物。回答下列问题:
(1)常温下,X、Y的水溶液的pH均为5。则两种水溶液中由水电离出的H+浓度之比是_______ 。
(2)A、B、D、E四种元素组成的某无机化合物,受热易分解。写出少量该化合物溶液与足量的Ba(OH)2溶液反应的离子方程式_______ 。
(3)将BA4,D2分别通入插在酸溶液中的两个电极形成燃料电池,则通BA4的一极的电极反应式为_______ 。
(4)化学反应3A2(g)+C2(g)⇌2CA3(g)。当反应达到平衡时不断改变条件(不改变A2、C2和CA3的量),如图表示反应速率与反应过程的关系,其中表示平衡混合物中CA3的含量最高的一段时间是_______ 。温度为T℃时,将4amolA2和2a molC2放入1L密闭容器中,充分反应后测得C2的转化率为50%,则平衡混合气中C2的体积分数为_______ ,平衡时压强为起始压强的_______ 倍。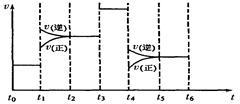
(1)常温下,X、Y的水溶液的pH均为5。则两种水溶液中由水电离出的H+浓度之比是
(2)A、B、D、E四种元素组成的某无机化合物,受热易分解。写出少量该化合物溶液与足量的Ba(OH)2溶液反应的离子方程式
(3)将BA4,D2分别通入插在酸溶液中的两个电极形成燃料电池,则通BA4的一极的电极反应式为
(4)化学反应3A2(g)+C2(g)⇌2CA3(g)。当反应达到平衡时不断改变条件(不改变A2、C2和CA3的量),如图表示反应速率与反应过程的关系,其中表示平衡混合物中CA3的含量最高的一段时间是

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】A、B、C、D、E五种短周期元素,原子序数依次增大,其中只有C为金属元素。A、C原子序数之和等于E的原子序数,D与B同主族且D原子序数是B原子序数的2倍。AB2和DB2溶于水得到酸性溶液,C2D溶于水得到碱性溶液。
(1)E元素在周期表中的位置为_______________ ;工业上制取C 单质的化学方程式为______ 。
(2)A的最低负价氢化物的空间构型为___ ;C、D、E 的简单离子的离子半径由大到小的顺序是__ (用离子符号表示)。
(3)化合物C2D3中,该化合物的水溶液在空气中久置后变质,生成一种单质,所得溶液呈强碱性,用化学方程式表示这一变化过程____________________ 。
(1)E元素在周期表中的位置为
(2)A的最低负价氢化物的空间构型为
(3)化合物C2D3中,该化合物的水溶液在空气中久置后变质,生成一种单质,所得溶液呈强碱性,用化学方程式表示这一变化过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】X、Y、Z、W均为短周期主族元素,X、Y、Z原子的最外层电子数之和为10。X与Z同族,Y最外层电子数等于X次外层电子数,且Y原子半径大于Z。W的最外层电子数等于X的核外电子总数,且W单质常温下为固体。请回答下列问题:
(1)Z在周期表中的位置为______________ 。
(2)Y元素形成的离子的结构示意图为____________ 。
(3)X、Y、Z三种元素对应的原子半径大小关系为____________ (填元素符号)。
(4)X和Z形成的简单氢化物,热稳定性较好的是______________ (填化学式)。
(5)下列说法正确的是_______ 。
A.X的氢化物在常温常压下均为气体
B.最高价氧化物对应的水化物的酸性W>Z
C.由于Z的氧化物ZO2既可与酸反应,又能与碱反应,所以ZO2为两性氧化物
D.W的氧化物WO2,具有还原性,能使酸性KMnO4溶液褪色
(1)Z在周期表中的位置为
(2)Y元素形成的离子的结构示意图为
(3)X、Y、Z三种元素对应的原子半径大小关系为
(4)X和Z形成的简单氢化物,热稳定性较好的是
(5)下列说法正确的是
A.X的氢化物在常温常压下均为气体
B.最高价氧化物对应的水化物的酸性W>Z
C.由于Z的氧化物ZO2既可与酸反应,又能与碱反应,所以ZO2为两性氧化物
D.W的氧化物WO2,具有还原性,能使酸性KMnO4溶液褪色
您最近一年使用:0次




