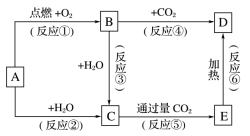
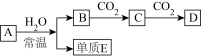
已知A、B、C、D是单质及其化合物,其焰色试验均为黄色,存在如图转化(部分反应物或生成物已略去)。
回答问题:
(1)若A为金属钠则A与水反应的离子方程式为______ 。
(2)若A为过氧化钠质量为7.8g,与足量水反应,转移电子的物质的量为______ mol。
(3) 中氧元素的化合价为
中氧元素的化合价为______ , 中阴、阳离子个数比是
中阴、阳离子个数比是______ 。
(4)C是______ (填化学式)溶液、向C溶液中逐滴滴入稀盐酸,现象是______ 。
(5)若D溶液中混有少量C,除去C的最佳方法是______ 。
(6)碳酸氢钠受热分解化学方程式______ 。

回答问题:
(1)若A为金属钠则A与水反应的离子方程式为
(2)若A为过氧化钠质量为7.8g,与足量水反应,转移电子的物质的量为
(3)
 中氧元素的化合价为
中氧元素的化合价为 中阴、阳离子个数比是
中阴、阳离子个数比是(4)C是
(5)若D溶液中混有少量C,除去C的最佳方法是
(6)碳酸氢钠受热分解化学方程式
更新时间:2023-11-07 13:47:13
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】现有X、Y、M、N四种化合物,已知它们的阳离子含有 、
、 、
、 、
、 ,阴离子含有
,阴离子含有 、
、 、
、 、
、 。现将它们分别配成
。现将它们分别配成 的溶液,常温下进行如下实验:
的溶液,常温下进行如下实验:
①溶液X、Y的焰色试验为黄色,溶液M的 ;
;
②盐溶液X和溶液Y混合,有气体生成;
③向溶液N中滴加溶液M,先出现白色沉淀,继续滴加,沉淀完全溶解;
④溶液Y和溶液N混合,既有气体生成,又有沉淀生成。
根据上述实验现象,回答下列问题:
(1)溶液Y显___________ (“酸”、“碱”或“中”)性。
(2)写出下列物质的化学式:X___________ 、M___________ 。
(3)实验②中,反应的离子方程式为___________ 。
(4)溶液X和溶液M混合,溶液显中性时,反应的离子方程式为___________ 。
(5)实验④中,反应的离子方程式为___________ 。
(6)设计实验方案检验溶液X中的阴离子___________ 。
 、
、 、
、 、
、 ,阴离子含有
,阴离子含有 、
、 、
、 、
、 。现将它们分别配成
。现将它们分别配成 的溶液,常温下进行如下实验:
的溶液,常温下进行如下实验:①溶液X、Y的焰色试验为黄色,溶液M的
 ;
;②盐溶液X和溶液Y混合,有气体生成;
③向溶液N中滴加溶液M,先出现白色沉淀,继续滴加,沉淀完全溶解;
④溶液Y和溶液N混合,既有气体生成,又有沉淀生成。
根据上述实验现象,回答下列问题:
(1)溶液Y显
(2)写出下列物质的化学式:X
(3)实验②中,反应的离子方程式为
(4)溶液X和溶液M混合,溶液显中性时,反应的离子方程式为
(5)实验④中,反应的离子方程式为
(6)设计实验方案检验溶液X中的阴离子
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
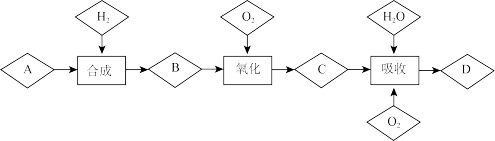
【推荐2】已知A是空气中含量最高的一种气体,D是一种重要的无机化工原料,由A到D的转化过程如下图所示。
回答下列问题:
(1)物质A的电子式为_______ ,物质D的分子式为_______ 。
(2)“合成”需要在高温、高压和催化剂的条件下进行,其发生反应的化学方程式_______ 。
(3)“吸收”中通入过量O2的目的是_______ 。
(4)工业上贮存物质D的浓溶液可选择的罐体材料为(填标号)_______ 。
a.银 b.铜 c.铝 d.锌

回答下列问题:
(1)物质A的电子式为
(2)“合成”需要在高温、高压和催化剂的条件下进行,其发生反应的化学方程式
(3)“吸收”中通入过量O2的目的是
(4)工业上贮存物质D的浓溶液可选择的罐体材料为(填标号)
a.银 b.铜 c.铝 d.锌
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】A—E五种物质都含有同一种元素,它们之间的转化关系如图所示,其中A为淡黄色固体化合物,B为单质,C是常见的碱。

(1)固体D的化学式为___________ ,常见用途有___________ (任写一条)。
(2)写出下列反应的离子方程式:
①单质B投入水中___________ ;
②D的饱和溶液中通CO2___________ 。
(3)下列说法不正确的是___________ (不定项选择)
A.物质E是工业生产物质D的一种原料
B.1molCl2与物质C充分反应,转移2mol电子
C.氯碱工业的产品包括Cl2和物质C
D.A→D的反应是氧化还原反应
E.检验D物质所含的金属元素,可用玻璃棒蘸取少量D,在酒精灯外焰上灼烧

(1)固体D的化学式为
(2)写出下列反应的
①单质B投入水中
②D的饱和溶液中通CO2
(3)下列说法不正确的是
A.物质E是工业生产物质D的一种原料
B.1molCl2与物质C充分反应,转移2mol电子
C.氯碱工业的产品包括Cl2和物质C
D.A→D的反应是氧化还原反应
E.检验D物质所含的金属元素,可用玻璃棒蘸取少量D,在酒精灯外焰上灼烧
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
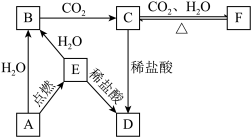
【推荐1】如图所示,下列各项变化的未知物焰色反应均呈黄色,E为淡黄色粉末。
回答下列问题。
(1)写出A→B的化学方程式,_____________________ 。
(2)写出C→D的离子方程式,_____________ 。
(3)当C溶液中含有杂质F,如何除杂:____________________ ,反应涉及的离子方程式_____________ 。
(4)E与CO2反应气体体积减小了11.2L(标准状况下),反应中转移电子的数目是___________ 。
(5)在一密闭容器中有CO、H2、O2共16.5 g和足量的E,用电火花引燃,使其完全反应,固体增重7.5 g,则原混合气体中O2的质量是__________ g。

回答下列问题。
(1)写出A→B的化学方程式,
(2)写出C→D的离子方程式,
(3)当C溶液中含有杂质F,如何除杂:
(4)E与CO2反应气体体积减小了11.2L(标准状况下),反应中转移电子的数目是
(5)在一密闭容器中有CO、H2、O2共16.5 g和足量的E,用电火花引燃,使其完全反应,固体增重7.5 g,则原混合气体中O2的质量是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验仪器,用下图中的实验装置进行实验,证明过氧化钠可作供氧剂。
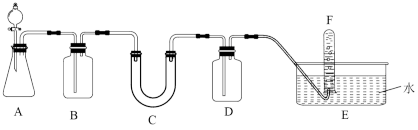
(1)A是制取 的装置,写出A中发生反应的化学方程式
的装置,写出A中发生反应的化学方程式___________ 。
(2)填写表中空格:
(3)写出过氧化钠与二氧化碳反应的化学方程式___________ 。
(4)用___________ 检验F中收集到的气体,现象是___________ 。
(5)将单质钠放到饱和Ca(OH)2溶液中会发生___________ ,用方程式解释___________

(1)A是制取
 的装置,写出A中发生反应的化学方程式
的装置,写出A中发生反应的化学方程式(2)填写表中空格:
| 仪器 | 加入试剂 | 加入该试剂的目的 |
| B | 饱和 溶液 溶液 | |
| C | 与 和水反应产生 和水反应产生 | |
| D | NaOH溶液 |
(4)用
(5)将单质钠放到饱和Ca(OH)2溶液中会发生
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】如图,A是金属钠,根据关系图回答下列问题。

(1)写出下列符号所代表的物质的化学式:B:___________ ;D:___________ 。
(2)写出下列物质转化的化学方程式。
①A→C:___________ 。
②C→D:___________ 。
(3)钠是一种很活泼的金属,下列保存金属钠的方法正确的是___________ (填字母)。
A.放在细沙中 B.放在水中 C.放在煤油中
(4)钠投入硫酸铜溶液中可观察到生成___________ 色沉淀
(5)在潜水艇和消防员的呼吸面具中,B所发生反应的化学方程式为___________ ,从氧化剂和还原剂的角度分析,在这个反应中B的作用是__________ 。

(1)写出下列符号所代表的物质的化学式:B:
(2)写出下列物质转化的化学方程式。
①A→C:
②C→D:
(3)钠是一种很活泼的金属,下列保存金属钠的方法正确的是
A.放在细沙中 B.放在水中 C.放在煤油中
(4)钠投入硫酸铜溶液中可观察到生成
(5)在潜水艇和消防员的呼吸面具中,B所发生反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】有A、B、C、D、E五种物质,在一定条件下的相互转化关系如图所示。已知:常温下E为无色液体,C、D为无色气体单质,A为金属单质,B为淡黄色固体,请回答下列问题:

(1)B的名称是___________ 。
(2)在一定条件下,D+C→E,该反应属于___________ 。
①化合反应 ②置换反应 ③复合分解反应 ④非氧化还原反应
(3)写出下列反应的化学方程式:
①A与C作用生成B:___________ ;
②B与H2O反应___________ 。

(1)B的名称是
(2)在一定条件下,D+C→E,该反应属于
①化合反应 ②置换反应 ③复合分解反应 ④非氧化还原反应
(3)写出下列反应的化学方程式:
①A与C作用生成B:
②B与H2O反应
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】在生活中亚硝酸钠(NaNO2)应用十分广泛,它是一种白色固体,外观与NaCl极其相似;少量可做食品的护色剂,可防止肉毒杆菌在肉类食品中生长,还可用于治疗氰化物中毒等。某化学兴趣小组查阅资料得知2NO+Na2O2=2NaNO2,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)。

已知:①NO能被高锰酸钾氧化,但不能被浓硫酸氧化。
②酸性高锰酸钾溶液可将 氧化成
氧化成 。
。
回答下列问题:
Ⅰ.NaNO2的制备:
(1)盛装浓硝酸的仪器名称为_____ ,仪器按气流方向连接顺序为b→g_____ (装置可重复使用)。
(2)反应开始前打开止水夹a,通入过量氮气的目的是排除装置中的空气,若不排除装置中的空气,可能产生的后果是_____ ;反应结束后打开止水夹a,通入过量氮气的目的是_____ 。
(3)盛水的洗气瓶的作用是_____ 。
(4)判断Na2O2已被NO反应完全的现象是_____ 。
Ⅱ.测定NaNO2的纯度:
准确称取反应后的固体3.000g于烧杯中,加入煮沸并冷却的蒸馏水溶解,配成250mL的溶液;取出25.00mL的溶液于锥形瓶中,用0.1 mol∙L−1的酸性KMnO4溶液滴定至刚好完全反应,用去16.00mL的酸性KMnO4溶液。
(5)滴定过程中的离子反应方程式为_____ 。
(6)所得固体中NaNO2的纯度为______ %。

已知:①NO能被高锰酸钾氧化,但不能被浓硫酸氧化。
②酸性高锰酸钾溶液可将
 氧化成
氧化成 。
。回答下列问题:
Ⅰ.NaNO2的制备:
(1)盛装浓硝酸的仪器名称为
(2)反应开始前打开止水夹a,通入过量氮气的目的是排除装置中的空气,若不排除装置中的空气,可能产生的后果是
(3)盛水的洗气瓶的作用是
(4)判断Na2O2已被NO反应完全的现象是
Ⅱ.测定NaNO2的纯度:
准确称取反应后的固体3.000g于烧杯中,加入煮沸并冷却的蒸馏水溶解,配成250mL的溶液;取出25.00mL的溶液于锥形瓶中,用0.1 mol∙L−1的酸性KMnO4溶液滴定至刚好完全反应,用去16.00mL的酸性KMnO4溶液。
(5)滴定过程中的离子反应方程式为
(6)所得固体中NaNO2的纯度为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】A~H为中学化学中常见的物质,其转化关系如图,其中“O”代表化合物,“□”代表单质,A为治疗胃酸过多的一种药剂的主要成分,G为淡黄色固体,C在通常状况下为无色液体,F为金属单质。请回答:
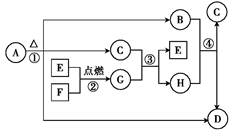
(1)G的化学式为______________ 。
(2)反应①②③④中属于氧化还原反应的_________ 。
(3)写出A→B+C+D的化学方程式_______________ 。写出F与C反应的离子万程式_______________ 。

(1)G的化学式为
(2)反应①②③④中属于氧化还原反应的
(3)写出A→B+C+D的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】A、B、C、D、E、F六种物质有如下变化关系,E是淡黄色粉末,
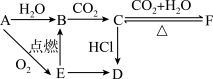
写出A、B、C、D、E、F的化学式: A.____ ,B.____ ,C._____ ,D._____ ,E._____ ,F.______

写出A、B、C、D、E、F的化学式: A.
您最近一年使用:0次