填空。
(1)常温常压条件下,相同体积的NH3和H2S所含N、S质量之比为___________ 。
(2)40.5 g某金属氯化物MCl2中含有0.6 molC1-,则M的相对原子质量为___________ 。
(3)a mLAl2(SO4)3溶液中含 b g,则溶液中A13+的物质的量浓度
b g,则溶液中A13+的物质的量浓度___________ 。
(4)用化学方法测量一个容器A的体积:把47.5 g MgC12放入500 mL烧杯中,加入150 mL蒸馏水;待MgCl2完全溶解后,将溶液全部转移到容器A中,用蒸馏水稀释至完全充满容器A;从中取出溶液50 mL,该溶液恰好与20 mL0.20 mol·L-1AgNO3溶液完全反应。通过计算可知该容器A的体积为___________ L。
(5)把V L含有MgSO4与K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为Mg(OH)2;另一份加入含b mol BaCl2的溶液,恰好使 完全沉淀为BaSO4,则原混合溶液中钾离子的物质的量浓度为
完全沉淀为BaSO4,则原混合溶液中钾离子的物质的量浓度为___________ 。
(1)常温常压条件下,相同体积的NH3和H2S所含N、S质量之比为
(2)40.5 g某金属氯化物MCl2中含有0.6 molC1-,则M的相对原子质量为
(3)a mLAl2(SO4)3溶液中含
 b g,则溶液中A13+的物质的量浓度
b g,则溶液中A13+的物质的量浓度(4)用化学方法测量一个容器A的体积:把47.5 g MgC12放入500 mL烧杯中,加入150 mL蒸馏水;待MgCl2完全溶解后,将溶液全部转移到容器A中,用蒸馏水稀释至完全充满容器A;从中取出溶液50 mL,该溶液恰好与20 mL0.20 mol·L-1AgNO3溶液完全反应。通过计算可知该容器A的体积为
(5)把V L含有MgSO4与K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为Mg(OH)2;另一份加入含b mol BaCl2的溶液,恰好使
 完全沉淀为BaSO4,则原混合溶液中钾离子的物质的量浓度为
完全沉淀为BaSO4,则原混合溶液中钾离子的物质的量浓度为
更新时间:2023-11-08 18:29:24
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】现有由硝酸钾、硝酸铵、硝酸镁组成的无土栽培液0.2 L,部分离子的浓度如下表所示:
(1)该混合溶液中硝酸镁的物质的量浓度为_______ ,将该混合溶液加水稀释至体积为1 L,稀释后溶液中NO 的物质的量浓度为
的物质的量浓度为_______ 。
(2)混合液中硝酸铵的物质的量为_______ ,硝酸钾的质量为_______ 。
(3)向该溶液中加入_______ mol NaOH可以使Mg2+完全沉淀,写出该反应的化学方程式_______
| 离子种类 | NH | Mg2+ | NO |
| 离子的物质的量浓度( mol·L-1) | 0.2 | 0.1 | 0.6 |
(1)该混合溶液中硝酸镁的物质的量浓度为
 的物质的量浓度为
的物质的量浓度为(2)混合液中硝酸铵的物质的量为
(3)向该溶液中加入
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】无机化合物可根据其组成和性质进行分类:
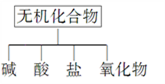
(1)上图所示的物质分类方法名称是________ 。
(2)以H、O、N、S中两种或三种 元素组成合适的物质,分别填在下表②③⑥处。
(3)过量⑦通入④中反应的离子方程式:______________________________ 。
(4)设阿伏伽德罗常数的值为NA。15.9g ⑤溶于水配制成250mL溶液,CO32-的粒子数为__________ ,Na+的物质的量浓度为_______________ 。
(5)上述八种物质中有两种可发生离子反应:NH4++OH- NH3·H2O,其对应的化学反应方程式为
NH3·H2O,其对应的化学反应方程式为____________________________________________________ 。

(1)上图所示的物质分类方法名称是
(2)以H、O、N、S中
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 |
| 化学式 | ①HCl ② | ③ ④Ba(OH)2 | ⑤Na2CO3 ⑥ | ⑦CO2 ⑧Na2O2 |
(3)过量⑦通入④中反应的离子方程式:
(4)设阿伏伽德罗常数的值为NA。15.9g ⑤溶于水配制成250mL溶液,CO32-的粒子数为
(5)上述八种物质中有两种可发生离子反应:NH4++OH-
 NH3·H2O,其对应的化学反应方程式为
NH3·H2O,其对应的化学反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
(1)该浓盐酸中HCl的物质的量浓度为__________ mol•L-1。
(2)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.200mol•L-1的稀盐酸。可供选用的仪器有:A胶头滴管;B量筒;C烧杯;D天平;E玻璃棒。
①配制稀盐酸时,上述仪器中不需要使用的有 (选填字母),还缺少的仪器有__________ 。
②该学生需要用__________ mL量筒量取__________ mL上述浓盐酸进行配制。
③配制稀盐酸时,在洗涤操作中,将洗涤液全部移入容量瓶,其目的是__________ 。
④配制稀盐酸时,在定容操作中,应在距刻度线__________ 处,改用胶头滴管滴加蒸馏水至液面与__________ 。
⑤若出现如下情况,对所配溶液浓度将有何影响?(填“偏高”、“偏低”或“无影响”)定容时俯视刻度线__________ ;定容后经振荡、摇匀、静置,发现液面下降,再加适合的蒸馏水__________ 。
| 盐酸 分子式:HCl 相对分子质量:36.5 密度:1.19g/cm3 质量分数:36.5% |
(1)该浓盐酸中HCl的物质的量浓度为
(2)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.200mol•L-1的稀盐酸。可供选用的仪器有:A胶头滴管;B量筒;C烧杯;D天平;E玻璃棒。
①配制稀盐酸时,上述仪器中不需要使用的有 (选填字母),还缺少的仪器有
②该学生需要用
③配制稀盐酸时,在洗涤操作中,将洗涤液全部移入容量瓶,其目的是
④配制稀盐酸时,在定容操作中,应在距刻度线
⑤若出现如下情况,对所配溶液浓度将有何影响?(填“偏高”、“偏低”或“无影响”)定容时俯视刻度线
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】化学与生产、生活及科研密切相关。回答下列问题:
(1)《淮南子·说山训》云:慈石能引铁(慈,旧作磁)。“慈石”的主要成分是_______ (填化学式)。
(2)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,11.2L“人造空气”的质量是4.8g,其中氧气和氦气的分子数之比为_______ 。
(3)厨房中常用小苏打作面包和糕点的发泡剂,写出小苏打受热分解的化学方程式_______ 。
(4)科学家经过研究发现中国霾呈中性,其主要原因如图所示:

请判断A的符号是_______ 。
(5)火药是古代道士配出的“药”,燃放烟花爆竹“产生大量烟雾”,这种烟雾的成分是二氧化硫,与空气中的水分最终形成了稀硫酸气溶胶。下列说法正确的是_______ (填字母)。
A.二氧化硫与空气中的水通过化合反应直接形成稀硫酸
B.稀硫酸具有强氧化性,可用于杀菌消毒
C.烟花爆竹燃烧产生的 和可吸入颗粒物均属于大气污染物
和可吸入颗粒物均属于大气污染物
(6)据文献报道,难溶于水的 可在
可在 溶液中“溶解”,“溶解”后硫元素都以
溶液中“溶解”,“溶解”后硫元素都以 的形式存在。若要检验“溶解”后溶液中
的形式存在。若要检验“溶解”后溶液中 是否有剩余,简要写出相关的实验操作
是否有剩余,简要写出相关的实验操作_______ 。
(1)《淮南子·说山训》云:慈石能引铁(慈,旧作磁)。“慈石”的主要成分是
(2)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,11.2L“人造空气”的质量是4.8g,其中氧气和氦气的分子数之比为
(3)厨房中常用小苏打作面包和糕点的发泡剂,写出小苏打受热分解的化学方程式
(4)科学家经过研究发现中国霾呈中性,其主要原因如图所示:

请判断A的符号是
(5)火药是古代道士配出的“药”,燃放烟花爆竹“产生大量烟雾”,这种烟雾的成分是二氧化硫,与空气中的水分最终形成了稀硫酸气溶胶。下列说法正确的是
A.二氧化硫与空气中的水通过化合反应直接形成稀硫酸
B.稀硫酸具有强氧化性,可用于杀菌消毒
C.烟花爆竹燃烧产生的
 和可吸入颗粒物均属于大气污染物
和可吸入颗粒物均属于大气污染物(6)据文献报道,难溶于水的
 可在
可在 溶液中“溶解”,“溶解”后硫元素都以
溶液中“溶解”,“溶解”后硫元素都以 的形式存在。若要检验“溶解”后溶液中
的形式存在。若要检验“溶解”后溶液中 是否有剩余,简要写出相关的实验操作
是否有剩余,简要写出相关的实验操作
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】由于地球的二氧化碳剧增,由此产生的“温室效应”使自然灾害频繁发生,2004年底印度洋发生的大地震及海啸造成的惨剧使世人记忆犹新。消除“温室效应”的有效措施是广泛植树造林。已知180 g葡萄糖(C6H12O6)完全燃烧时放热2804 kJ。太阳每分钟对地球表面辐射能量为2.1 J/cm2;植物通过光合作用生成葡萄糖和氧气。设光合作用时太阳能量利用率10%,每片树叶面积以10 cm2计算,这样的树叶100片要合成1.8 g葡萄糖。
(1)需光照多长时间__________ ?
(2)若空气中含CO2质量分数为0.3%,需要标准状况下空气多少升__________ ?(标准状况下空气密度为1.29 g/L)
(1)需光照多长时间
(2)若空气中含CO2质量分数为0.3%,需要标准状况下空气多少升
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】在一定温度下,某饱和氢氧化钠溶液体积为V mL,溶液密度为d g·cm-3,质量分数为w,物质的量浓度为c mol·L-1,溶液中含氢氧化钠的质量为m g,该温度下NaOH的溶解度为S。
(1)用w来表示该温度下氢氧化钠的溶解度(S)为_________________ 。
(2)用m、V表示溶液中溶质的物质的量浓度(c)为__________________ 。
(3)用w、d表示溶液中溶质的物质的量浓度(c)为__________________ 。
(4)用c、d表示溶液中溶质的质量分数(w)为______________________ 。
(5)用S、d表示溶液中溶质的物质的量浓度(c)为___________________ 。
(1)用w来表示该温度下氢氧化钠的溶解度(S)为
(2)用m、V表示溶液中溶质的物质的量浓度(c)为
(3)用w、d表示溶液中溶质的物质的量浓度(c)为
(4)用c、d表示溶液中溶质的质量分数(w)为
(5)用S、d表示溶液中溶质的物质的量浓度(c)为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)标准状况下,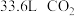 的物质的量为
的物质的量为_______  ,质量为
,质量为_______  。
。
(2)小明一次可以喝一瓶水,求一瓶纯净水(按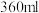 计)中含有
计)中含有_______ 个水分子。
(3)某小组同学欲用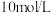 的盐酸配制
的盐酸配制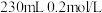 盐酸溶液,需用量筒取用
盐酸溶液,需用量筒取用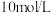 盐酸
盐酸_______  。
。
(4)写电子式:
_______ 
_______ 
_______
(5)用电子式表示下列物质形成过程:

_______ ;

_______ 。
(1)标准状况下,
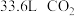 的物质的量为
的物质的量为 ,质量为
,质量为 。
。(2)小明一次可以喝一瓶水,求一瓶纯净水(按
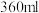 计)中含有
计)中含有(3)某小组同学欲用
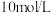 的盐酸配制
的盐酸配制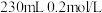 盐酸溶液,需用量筒取用
盐酸溶液,需用量筒取用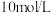 盐酸
盐酸 。
。(4)写电子式:



(5)用电子式表示下列物质形成过程:


您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)1mol/L的CaCl2溶液0.5L,Cl-离子的物质的量浓度___________ mol/L。
(2)标准状况下,33.6L的NH3所具有的物质的量为___________ mol,将其溶解于水配成1L的溶液,则溶液的物质的量浓度为___________ mol/L,在Cl2+2NaOH=NaCl+NaClO+H2O的反应中,写出反应的离子方程式___________ 。氧化产物是___________ ,还原产物是___________ ;氧化剂与还原剂的物质的量的比是___________ 。
(3)用双线桥表示出电子转移的方向和数目___________ 。
Cl2+2NaOH=NaCl+NaClO+H2O
(1)1mol/L的CaCl2溶液0.5L,Cl-离子的物质的量浓度
(2)标准状况下,33.6L的NH3所具有的物质的量为
(3)用双线桥表示出电子转移的方向和数目
Cl2+2NaOH=NaCl+NaClO+H2O
您最近一年使用:0次



