随着化石能源的减少,新能源的开发利用日益迫切。
(1)Bunsen热化学循环制氢工艺由下列三个反应组成:
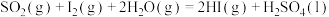
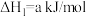
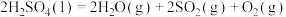
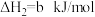
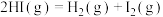
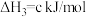
则: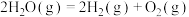

___________ kJ/mol。
(2)硅光电池作为电源已广泛应用于人造卫星、灯塔和无人气象站等,工业制备纯硅的反应为
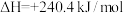 ,若将生成的HCl通入100mL1mol/L的NaOH溶液中恰好完全反应,则此制备纯硅反应过程
,若将生成的HCl通入100mL1mol/L的NaOH溶液中恰好完全反应,则此制备纯硅反应过程___________ (填“吸收”或“放出”)的热量是___________ kJ。
(3)甲醇是一种新型的汽车动力燃料。
①以 和
和 为原料合成甲醇,反应的能量变化如下图所示,则图中A处应填写的内容为
为原料合成甲醇,反应的能量变化如下图所示,则图中A处应填写的内容为___________ 。

②工业上利用CO和 来制备甲醇气体。已知某些化学键的键能数据如下表:
来制备甲醇气体。已知某些化学键的键能数据如下表:
设CO以 键构成,则工业制备甲醇的热化学方程式为
键构成,则工业制备甲醇的热化学方程式为___________ 。
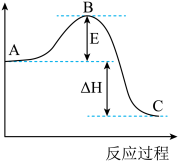
(4)恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图所示:
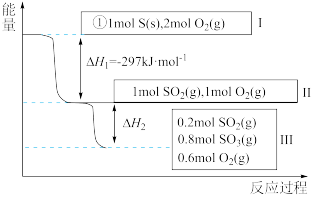
已知: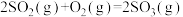

①表示硫的燃烧热的热化学方程式为___________ 。
②图中
___________ kJ/mol。
(1)Bunsen热化学循环制氢工艺由下列三个反应组成:
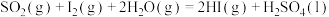
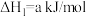
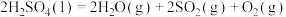
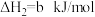
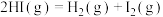
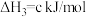
则:
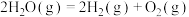

(2)硅光电池作为电源已广泛应用于人造卫星、灯塔和无人气象站等,工业制备纯硅的反应为

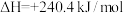 ,若将生成的HCl通入100mL1mol/L的NaOH溶液中恰好完全反应,则此制备纯硅反应过程
,若将生成的HCl通入100mL1mol/L的NaOH溶液中恰好完全反应,则此制备纯硅反应过程(3)甲醇是一种新型的汽车动力燃料。
①以
 和
和 为原料合成甲醇,反应的能量变化如下图所示,则图中A处应填写的内容为
为原料合成甲醇,反应的能量变化如下图所示,则图中A处应填写的内容为
②工业上利用CO和
 来制备甲醇气体。已知某些化学键的键能数据如下表:
来制备甲醇气体。已知某些化学键的键能数据如下表:| 化学键 |  |  |  |  |  |  |
键能/ | 348 | 413 | 436 | 358 | 1072 | 463 |
 键构成,则工业制备甲醇的热化学方程式为
键构成,则工业制备甲醇的热化学方程式为(4)恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图所示:

已知:
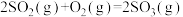

①表示硫的燃烧热的热化学方程式为
②图中

更新时间:2023-11-17 06:03:01
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)NH4Cl溶液显酸性的原因是___ (用离子方程式表示)。
(2)有pH均为3的CH3COOH、HNO3、H2SO4三种物质的溶液,物质的量浓度由大到小的顺序为___ 。
(3)二氧化碳加氢制甲醇的反应一般可通过如下步骤来实现:
①CO2(g)+H2(g)=CO(g)+H2O(g) △H1=+41kJ·mol-1
②CO(g)+2H2(g)=CH3OH(g) △H2=-90kJ·mol-1
二氧化碳加氢制甲醇的热化学方程式___ 。
(4)如图所示装置中,A、B、C、D均为铂电极。断开K1,闭合K2、K3一段时间后,A、B中气体的量之间的关系如图所示:
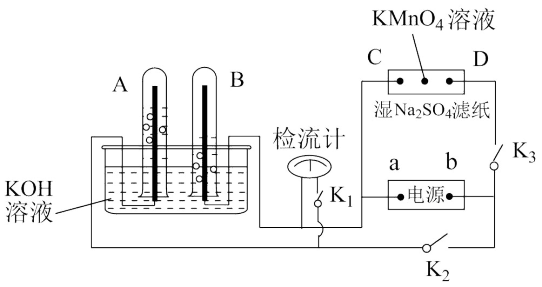
①写出A电极反应式___ 。
②在湿的Na2SO4溶液滤纸条中心的KMnO4液滴发生的现象为___ 。
③若电解一段时间后,A、B中均有气体包围电极。此时切断K2、K3,闭合K1,则电流表的指针发生移动,其理由是___ 。
(1)NH4Cl溶液显酸性的原因是
(2)有pH均为3的CH3COOH、HNO3、H2SO4三种物质的溶液,物质的量浓度由大到小的顺序为
(3)二氧化碳加氢制甲醇的反应一般可通过如下步骤来实现:
①CO2(g)+H2(g)=CO(g)+H2O(g) △H1=+41kJ·mol-1
②CO(g)+2H2(g)=CH3OH(g) △H2=-90kJ·mol-1
二氧化碳加氢制甲醇的热化学方程式
(4)如图所示装置中,A、B、C、D均为铂电极。断开K1,闭合K2、K3一段时间后,A、B中气体的量之间的关系如图所示:

①写出A电极反应式
②在湿的Na2SO4溶液滤纸条中心的KMnO4液滴发生的现象为
③若电解一段时间后,A、B中均有气体包围电极。此时切断K2、K3,闭合K1,则电流表的指针发生移动,其理由是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】请回答下列问题:
(1)已知2mol氢气燃烧生成液态水时放出572kJ的热量,反应方程式是2H2(g)+O2(g)=2H2O(l)。
①该反应的生成物能量总和__ (填“大于”、“小于”或“等于”)反应物能量总和。
②若2mol氢气完全燃烧生成水蒸气,则放出的热量___ (填“大于”、“小于”或“等于”)572 kJ。
(2)2.3g有机物C2H6O和一定量的氧气混合点燃,恰好完全燃烧,生成CO2和液态水,并放出68.35kJ热量,则该反应的热化学方程式是___ 。
(3)FeS2焙烧产生的SO2可用于制硫酸。已知25℃、101kPa时:
2SO2(g)+O2(g) 2SO3(g) ΔH1=-197 kJ·mol-1
2SO3(g) ΔH1=-197 kJ·mol-1
H2O(g)=H2O(l) ΔH2=-44kJ·mol-1
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) ΔH3=-545kJ·mol-1
则SO3(g)与H2O(l)反应生成H2SO4(l)的热化学方程式是___ 。
(4)2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示。该反应通常用V2O5作催化剂,加V2O5会使图中B点
2SO3(g)反应过程的能量变化如图所示。该反应通常用V2O5作催化剂,加V2O5会使图中B点___ (填“升高”还是“降低”),△H___ (填“变大”、“变小”或“不变”)。
(5)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、___ 、量筒。量取反应物时,取50 mL 0.50 mol·L-1的盐酸,还需加入的试剂是___ (填序号)。
A.50 mL0.50mol·L-1NaOH溶液
B.50 mL0.55mol·L-1NaOH溶液
C.1.0gNaOH固体
(1)已知2mol氢气燃烧生成液态水时放出572kJ的热量,反应方程式是2H2(g)+O2(g)=2H2O(l)。
①该反应的生成物能量总和
②若2mol氢气完全燃烧生成水蒸气,则放出的热量
(2)2.3g有机物C2H6O和一定量的氧气混合点燃,恰好完全燃烧,生成CO2和液态水,并放出68.35kJ热量,则该反应的热化学方程式是
(3)FeS2焙烧产生的SO2可用于制硫酸。已知25℃、101kPa时:
2SO2(g)+O2(g)
 2SO3(g) ΔH1=-197 kJ·mol-1
2SO3(g) ΔH1=-197 kJ·mol-1H2O(g)=H2O(l) ΔH2=-44kJ·mol-1
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) ΔH3=-545kJ·mol-1
则SO3(g)与H2O(l)反应生成H2SO4(l)的热化学方程式是
(4)2SO2(g)+O2(g)
 2SO3(g)反应过程的能量变化如图所示。该反应通常用V2O5作催化剂,加V2O5会使图中B点
2SO3(g)反应过程的能量变化如图所示。该反应通常用V2O5作催化剂,加V2O5会使图中B点
(5)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、
A.50 mL0.50mol·L-1NaOH溶液
B.50 mL0.55mol·L-1NaOH溶液
C.1.0gNaOH固体
您最近一年使用:0次
【推荐3】回答下列问题
(1)①写出小苏打的化学式___________ ;
②写出Fe2+的价电子排布式___________ 。
(2)实验室用软锰矿和浓盐酸制氯气,写出该反应的化学方程式___________ 。
(3)在常温下,0.1mol/LCH3COONa溶液的pH=9,则溶液中由水电离出来的c(OH-)=___________
(4)火箭发射可以用肼(N2H4,液态)作燃料,NO2作氧化剂,两者反应生成N2和水蒸气。
已知:N2(g)+2O2(g)=2NO2(g) ΔH1=+66.4kJ/mol
N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ/mol
请写出N2H4(l)与NO2反应的热化学方程式___________
(5)下表列出了某短周期元素R的各级电离能数据(用I1、I2……表示)。
关于元素R的下列推断中,正确的是___________ (用相应的编号填写)
①R元素基态原子的电子排布式为1s22s2
②R元素位于元素周期表中第ⅡA族
③R元素的最高正化合价为+2价
④R元素的第一电离能高于同周期相邻元素的第一电离能
(1)①写出小苏打的化学式
②写出Fe2+的价电子排布式
(2)实验室用软锰矿和浓盐酸制氯气,写出该反应的化学方程式
(3)在常温下,0.1mol/LCH3COONa溶液的pH=9,则溶液中由水电离出来的c(OH-)=
(4)火箭发射可以用肼(N2H4,液态)作燃料,NO2作氧化剂,两者反应生成N2和水蒸气。
已知:N2(g)+2O2(g)=2NO2(g) ΔH1=+66.4kJ/mol
N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ/mol
请写出N2H4(l)与NO2反应的热化学方程式
(5)下表列出了某短周期元素R的各级电离能数据(用I1、I2……表示)。
| 元素 | 电离能/(kJ·mol-1) | |||||
| I1 | I2 | I3 | I4 | I5 | …… | |
| R | 740 | 1500 | 7700 | 10500 | 13630 | …… |
①R元素基态原子的电子排布式为1s22s2
②R元素位于元素周期表中第ⅡA族
③R元素的最高正化合价为+2价
④R元素的第一电离能高于同周期相邻元素的第一电离能
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】甲醇是一种重要的化工原料,又是一种可再生能源,具有开发和应用的广阔前景。
(1)已知:CH3OH(g)===HCHO(g)+H2(g) ΔH=+84 kJ·mol-1
2H2(g)+O2(g)===2H2O(g) ΔH=-484 kJ·mol-1
①工业上常以甲醇为原料制取甲醛,请写出CH3OH(g)与O2(g)反应生成HCHO(g)和H2O(g)的热化学方程式:______________________________________________ 。
②在上述制备甲醛时,常向反应器中通入适当过量的氧气,其目的_________________ 。
(2)工业上可用如下方法合成甲醇,化学方程式为CO(g)+2H2(g)==CH3OH(g),已知某些化学键的键能数据如下表:
请回答下列问题:
①图1中曲线a到曲线b的措施是_________ 。

②已知CO中的C与O之间为叁键,其键能为x kJ/mol,则x=________ 。
(3)由甲醇、氧气和NaOH溶液构成的新型手机电池,可使手机连续使用一个月才充一次电。
①该电池负极的电极反应式为______________________________________ 。
②若以该电池为电源,用石墨作电极电解200 mL含有如下离子的溶液。
电解一段时间后,当两极收集到相同体积(相同条件下)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象)阳极上收集到氧气的质量为________ 。
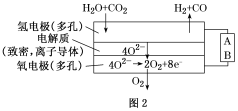
(4)电解水蒸气和CO2产生合成气(H2+CO)。较高温度下(700~1 000 ℃),在SOEC两侧电极上施加一定的直流电压,H2O和CO2在氢电极发生还原反应产生O2-,O2-穿过致密的固体氧化物电解质层到达氧电极,在氧电极发生氧化反应得到纯O2。由图2可知A为直流电源的________ (填“正极”或“负极”),请写出以H2O为原料生成H2的电极反应式:____________________ 。
(1)已知:CH3OH(g)===HCHO(g)+H2(g) ΔH=+84 kJ·mol-1
2H2(g)+O2(g)===2H2O(g) ΔH=-484 kJ·mol-1
①工业上常以甲醇为原料制取甲醛,请写出CH3OH(g)与O2(g)反应生成HCHO(g)和H2O(g)的热化学方程式:
②在上述制备甲醛时,常向反应器中通入适当过量的氧气,其目的
(2)工业上可用如下方法合成甲醇,化学方程式为CO(g)+2H2(g)==CH3OH(g),已知某些化学键的键能数据如下表:
| 化学键 | C—C | C—H | H—H | C—O | C≡O | O—H |
| 键能/(kJ·mol-1) | 348 | 413 | 436 | 358 | x | 463 |
请回答下列问题:
①图1中曲线a到曲线b的措施是

②已知CO中的C与O之间为叁键,其键能为x kJ/mol,则x=
(3)由甲醇、氧气和NaOH溶液构成的新型手机电池,可使手机连续使用一个月才充一次电。
①该电池负极的电极反应式为
②若以该电池为电源,用石墨作电极电解200 mL含有如下离子的溶液。
| 离子 | Cu2+ | H+ | Cl- | SO42- |
| c/(mol·L-1) | 0.5 | 2 | 2 | 0.5 |
电解一段时间后,当两极收集到相同体积(相同条件下)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象)阳极上收集到氧气的质量为
(4)电解水蒸气和CO2产生合成气(H2+CO)。较高温度下(700~1 000 ℃),在SOEC两侧电极上施加一定的直流电压,H2O和CO2在氢电极发生还原反应产生O2-,O2-穿过致密的固体氧化物电解质层到达氧电极,在氧电极发生氧化反应得到纯O2。由图2可知A为直流电源的

您最近一年使用:0次
填空题
|
适中
(0.65)
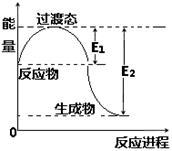
【推荐2】Ⅰ.(1)下图为1molNO2(g)和1molCO(g)反应生成NO(g)和CO2(g)过程中的能量变化示意图。已知E1=134KJ/mol,E2=368KJ/mol( E1、 E2为反应的活化能)。若在反应体系中加入催化剂,反应速率增大,则E1、△H的变化分别是 、 (填“增大”、“减小”或“不变”)。写出该 反应的热化学方程式 。
(2)若反应SO2(g)+I2(g)+2H2O(g)=H2SO4(l)+2HI(g)在150℃下能自发进行,则△H___0。
A.大于 B.小于 C.等于 D.大于或小于都可
Ⅱ.以CO2为碳源制取低碳有机物成为国际研究焦点,下面为CO2加氢制取乙醇的反应:
2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g) △H=QkJ/mol (Q>0)
CH3CH2OH(g)+3H2O(g) △H=QkJ/mol (Q>0)
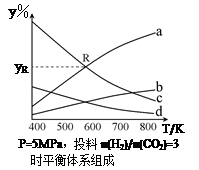
在密闭容器中,按CO2与H2的物质的量之比为1:3进行投料,在5MPa下测得不同温度下平衡体系中各种物质的体积分数(y%)如下图所示。完成下列填空:
(1)表示CH3CH2OH体积分数曲线的是____(选填序号)。
(2)在一定温度下反应达到平衡的标志是 。
A.平衡常数K不再增大 B.CO2的转化率不再增大
C.混合气体的平均相对分子质量不再改变 D.反应物不再转化为生成物
(3)其他条件恒定,达到平衡后,能提高H2转化率的措施是_______(选填编号)。
A.升高温度 B.充入更多的H2C.移去乙醇 D.增大容器体积
(4)图中曲线a和c的交点R对应物质的体积分数yR=_______。
(2)若反应SO2(g)+I2(g)+2H2O(g)=H2SO4(l)+2HI(g)在150℃下能自发进行,则△H___0。
A.大于 B.小于 C.等于 D.大于或小于都可


Ⅱ.以CO2为碳源制取低碳有机物成为国际研究焦点,下面为CO2加氢制取乙醇的反应:
2CO2(g)+6H2(g)
 CH3CH2OH(g)+3H2O(g) △H=QkJ/mol (Q>0)
CH3CH2OH(g)+3H2O(g) △H=QkJ/mol (Q>0)在密闭容器中,按CO2与H2的物质的量之比为1:3进行投料,在5MPa下测得不同温度下平衡体系中各种物质的体积分数(y%)如下图所示。完成下列填空:
(1)表示CH3CH2OH体积分数曲线的是____(选填序号)。
(2)在一定温度下反应达到平衡的标志是 。
A.平衡常数K不再增大 B.CO2的转化率不再增大
C.混合气体的平均相对分子质量不再改变 D.反应物不再转化为生成物
(3)其他条件恒定,达到平衡后,能提高H2转化率的措施是_______(选填编号)。
A.升高温度 B.充入更多的H2C.移去乙醇 D.增大容器体积
(4)图中曲线a和c的交点R对应物质的体积分数yR=_______。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.已知下列热化学方程式:
①2H2(g)+O2(g)=2H2O(l) △H=-570kJ/mol
②2H2O(g)=2H2(g)+O2(g) △H=+483.6kJ/mol
回答下列问题:
(1)上述反应中属于放热反应的是_______ (填写序号)。
(2)燃烧10gH2生成液态水,放出的热量为_______ 。
(3)已知:1L1mol/LH2SO4溶液与2L1mol/LNaOH溶液完全反应,放出114.6kJ的热量,由此推知H2SO4与NaOH发生中和反应,写出该中和热的热化学方程式为_______ 。
Ⅱ.已知:工业上制二甲醚是在一定温度(230~280℃)、压强(2.0~10.0MPa)和催化剂作用下进行的,反应器中发生了下列反应:
CO(g)+2H2(g)=CH3OH(g) ΔH1=-90.7kJ·mol-1 ①
2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH2=-23.5kJ·mol-1 ②
CO(g)+H2O(g)=CO2(g)+H2(g) ΔH3=-41.2kJ·mol-1 ③
(4)反应器中的总反应可表示为3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g),计算该反应的ΔH=_______ 。
①2H2(g)+O2(g)=2H2O(l) △H=-570kJ/mol
②2H2O(g)=2H2(g)+O2(g) △H=+483.6kJ/mol
回答下列问题:
(1)上述反应中属于放热反应的是
(2)燃烧10gH2生成液态水,放出的热量为
(3)已知:1L1mol/LH2SO4溶液与2L1mol/LNaOH溶液完全反应,放出114.6kJ的热量,由此推知H2SO4与NaOH发生中和反应,写出该中和热的热化学方程式为
Ⅱ.已知:工业上制二甲醚是在一定温度(230~280℃)、压强(2.0~10.0MPa)和催化剂作用下进行的,反应器中发生了下列反应:
CO(g)+2H2(g)=CH3OH(g) ΔH1=-90.7kJ·mol-1 ①
2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH2=-23.5kJ·mol-1 ②
CO(g)+H2O(g)=CO2(g)+H2(g) ΔH3=-41.2kJ·mol-1 ③
(4)反应器中的总反应可表示为3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g),计算该反应的ΔH=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
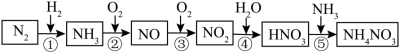
【推荐1】氮元素及其化合物的转化关系如图所示。___________ 。
(2)氮元素在元素周期表中的位置是___________ 。
(3)已知1molNH3发生反应②,完全反应生成NO和水蒸气时放出226 kJ的热,该反应的热化学方程式是___________ 。
(4)汽车尾气净化装置中,气体在催化剂表面吸附与解吸作用的过程如图所示。___________ 。
②催化转化过程中,理论上每生成1mol 时,转移的电子为
时,转移的电子为___________ mol。
(2)氮元素在元素周期表中的位置是
(3)已知1molNH3发生反应②,完全反应生成NO和水蒸气时放出226 kJ的热,该反应的热化学方程式是
(4)汽车尾气净化装置中,气体在催化剂表面吸附与解吸作用的过程如图所示。
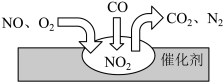
②催化转化过程中,理论上每生成1mol
 时,转移的电子为
时,转移的电子为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
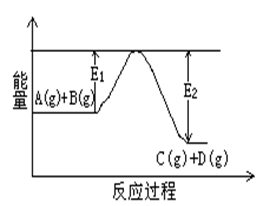
(1)反应A(g)+B(g) C(g)+D(g)过程中的能量变化如图 所示,判断该反应△H
C(g)+D(g)过程中的能量变化如图 所示,判断该反应△H___________ 0 (填“>”、“<”、“无法确定”)。
(2)在Al2O3、Ni催化下气态甲酸发生下列反应:
甲酸(g)= CO (g)+ H2O (g) △H1= + 34.0 kJ/mol
甲酸(g)= CO2 (g)+ H2(g) △H2= —7.0 kJ/mol
则甲酸的分子式为____________ ,在该条件下,气态CO2 和气态H2 生成气态CO和气态H2O的热化学方程式为 __________________________________________________________________ 。
(3)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水(H2O2)。当把0.4mol液态肼和0.8mol 液态H2O2混合反应,生成氮气和水蒸气,放出256.7kJ的热量(相当于25℃、101 kPa下测得的热量)。反应的热化学方程式为:____________________________________________________________________________ 。
(1)反应A(g)+B(g)
 C(g)+D(g)过程中的能量变化如图 所示,判断该反应△H
C(g)+D(g)过程中的能量变化如图 所示,判断该反应△H
(2)在Al2O3、Ni催化下气态甲酸发生下列反应:
甲酸(g)= CO (g)+ H2O (g) △H1= + 34.0 kJ/mol
甲酸(g)= CO2 (g)+ H2(g) △H2= —7.0 kJ/mol
则甲酸的分子式为
(3)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水(H2O2)。当把0.4mol液态肼和0.8mol 液态H2O2混合反应,生成氮气和水蒸气,放出256.7kJ的热量(相当于25℃、101 kPa下测得的热量)。反应的热化学方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
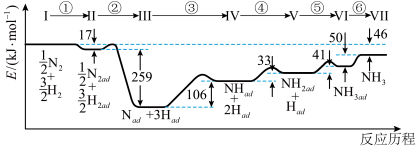
【推荐1】肼 又称联氨,在航空航天方面应用广泛,可用作火箭燃料。已知
又称联氨,在航空航天方面应用广泛,可用作火箭燃料。已知 键、
键、 键键能分别为
键键能分别为 ,
, 与
与 反应的能量变化如图所示:
反应的能量变化如图所示:

(1) 中
中 键的键能为
键的键能为________  。
。
(2)一定条件下, 与
与 反应的热化学方程式为:
反应的热化学方程式为:________________ 。
 又称联氨,在航空航天方面应用广泛,可用作火箭燃料。已知
又称联氨,在航空航天方面应用广泛,可用作火箭燃料。已知 键、
键、 键键能分别为
键键能分别为 ,
, 与
与 反应的能量变化如图所示:
反应的能量变化如图所示:
(1)
 中
中 键的键能为
键的键能为 。
。(2)一定条件下,
 与
与 反应的热化学方程式为:
反应的热化学方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表中的数据是破坏1 mol物质中的化学键所消耗的能量(kJ):
根据上述数据回答(1)~(5)题。
(1)下列物质本身具有的能量最低的是____ 。
A.H2 B.Cl2 C.Br2 D.I2
(2)下列氢化物中,最稳定的是____ 。
A.HCl B.HBr C.HI
(3)X2+H2 2HX(X代表Cl、Br、I )的反应是吸热反应还是放热反应?答:
2HX(X代表Cl、Br、I )的反应是吸热反应还是放热反应?答:___________ 。
(4)相同条件下,X2(X代表Cl、Br、I)分别与氢气反应,当消耗等物质的量的氢气时,放出或吸收的热量最多的是_____ 。
(5)若无上表中的数据,你能正确回答出问题(4)吗?
答:_____ ,你的根据是____________ 。
| 物质 | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| 能量/kJ | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
根据上述数据回答(1)~(5)题。
(1)下列物质本身具有的能量最低的是
A.H2 B.Cl2 C.Br2 D.I2
(2)下列氢化物中,最稳定的是
A.HCl B.HBr C.HI
(3)X2+H2
 2HX(X代表Cl、Br、I )的反应是吸热反应还是放热反应?答:
2HX(X代表Cl、Br、I )的反应是吸热反应还是放热反应?答:(4)相同条件下,X2(X代表Cl、Br、I)分别与氢气反应,当消耗等物质的量的氢气时,放出或吸收的热量最多的是
(5)若无上表中的数据,你能正确回答出问题(4)吗?
答:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】在 25℃、101kPa 下,依据事实写出下列反应的热化学方程式。
(1)1g 乙醇燃烧生成CO2和液态水时放热 29.7kJ。则表示乙醇燃烧热的热化学方程式为_____ ;
(2)已知拆开 1mol H﹣H 键,1molN﹣H 键,1molN≡N 键分别需要的能量是 436kJ、391kJ、946kJ,则 N2 与H2 反应生成 NH3 的热化学方程式为________________ ;若适量的 N2 和O2 完全反应,每生成 23 克 NO2 需要吸收 16.95kJ 热量。则其热化学方程式为:_____ ;已知 AX3 的熔点和沸点分别为-93.6 ℃和 76℃,AX5 的熔点为 167 ℃。室温时 AX3与气体 X2 反应生成 1 mol AX5,放出热量 123.8 kJ。该反应的热化学方程式为:__________
(1)1g 乙醇燃烧生成CO2和液态水时放热 29.7kJ。则表示乙醇燃烧热的热化学方程式为
(2)已知拆开 1mol H﹣H 键,1molN﹣H 键,1molN≡N 键分别需要的能量是 436kJ、391kJ、946kJ,则 N2 与H2 反应生成 NH3 的热化学方程式为
您最近一年使用:0次

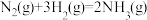 △H=
△H=

