下列关于判断化学反应方向的说法正确的是
| A.通过改变温度的办法可使非自发反应转变为自发反应 |
| B.所有自发进行的化学反应都是放热反应 |
| C.熵值减小的反应不可能是自发反应 |
| D.相同物质的量同一物质固、液、气三种状态的熵值依次减小 |
更新时间:2023-10-05 09:11:01
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列实验操作对应的现象与结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向两支分别盛有0.1mol/L醋酸和饱和硅酸的试管中滴加等浓度的Na2CO3溶液 | 两支试管都都有气泡产生 | 醋酸和硅酸的酸性比碳酸强 |
| B | 室温下向物质的量浓度均为0.1mol/L的NaCl和NaI混合溶液中滴加AgNO3溶液 | 先出现黄色沉淀 | Ksp(AgCl)<Ksp(AgI) |
| C | 室温下将Ba(OH)2·8H2O晶体与NH4Cl晶体在小烧杯中混合 | 烧杯壁感觉变凉 | Ba(OH)2·8H2O与NH4Cl的反应是吸热反应 |
| D | 将0.1mol/L的氨水稀释成0.01mol/L,测量稀释前后溶液pH | pH减小 | 稀释后NH3·H2O电离程度减小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】分类是学习和研究化学的一种常用的科学方法。下列分类合理的是
①根据酸分子中含有的H原子个数将酸分为一元酸、二元酸等
②根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应
③根据电解质在水溶液或熔融状态下能否完全电离将电解质分为强电解质和弱电解质
④根据元素原子最外层电子数的多少将元素分为金属和非金属
⑤根据反应的热效应将化学反应分为放热反应和吸热反应
①根据酸分子中含有的H原子个数将酸分为一元酸、二元酸等
②根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应
③根据电解质在水溶液或熔融状态下能否完全电离将电解质分为强电解质和弱电解质
④根据元素原子最外层电子数的多少将元素分为金属和非金属
⑤根据反应的热效应将化学反应分为放热反应和吸热反应
| A.②③⑤ | B.①②⑤ | C.①②③ | D.②③④⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】对于反应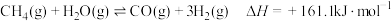 ,下列说法正确的是
,下列说法正确的是
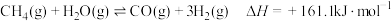 ,下列说法正确的是
,下列说法正确的是| A.该反应在任何温度下都能自发进行 |
B. 和 和 充分反应时,吸收的热量为322.2kJ 充分反应时,吸收的热量为322.2kJ |
C.反应的平衡常数可表示为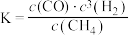 |
D.其他条件相同,增大 ,CH4的转化率下降 ,CH4的转化率下降 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
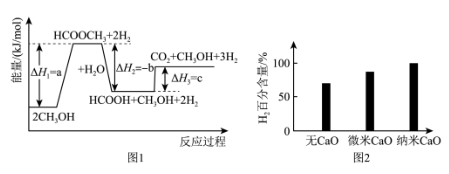
【推荐2】甲醇水蒸气催化重整是获取H2的重要方法,反应CH3OH(g)+H2O(g) CO2(g)+3H2(g) ΔH>0能量变化如图1所示。830°C时,相同时间内向反应体系中投入一定量CaO做对比实验,结果如图2所示,下列说法中正确的是
CO2(g)+3H2(g) ΔH>0能量变化如图1所示。830°C时,相同时间内向反应体系中投入一定量CaO做对比实验,结果如图2所示,下列说法中正确的是
 CO2(g)+3H2(g) ΔH>0能量变化如图1所示。830°C时,相同时间内向反应体系中投入一定量CaO做对比实验,结果如图2所示,下列说法中正确的是
CO2(g)+3H2(g) ΔH>0能量变化如图1所示。830°C时,相同时间内向反应体系中投入一定量CaO做对比实验,结果如图2所示,下列说法中正确的是
| A.该反应的ΔH=(a-b-c)kJ·mol-1 |
| B.CaO表面积越大,吸收CO2效果越好 |
| C.该反应在低温下能自发进行 |
| D.选择适当催化剂降低ΔH3可显著提高催化重整反应速率 |
您最近一年使用:0次

 是一种强温室气体,消除大气中的
是一种强温室气体,消除大气中的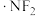 和
和 有两种反应历程如图所示。下列说法
有两种反应历程如图所示。下列说法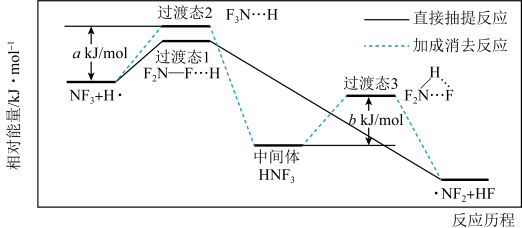

 ,下列说法不正确的是
,下列说法不正确的是

