通过计算填写下列内容:
(1)在标准状况下,6.72L CO的物质的量为_______ mol,质量为_______ g。
(2)23g C2H5OH的氢原子数目为_______ 。
(3)100mLNa2SO4溶液中, SO 的物质的量浓度为1mol/L,则Na+的物质的量浓度为
的物质的量浓度为1mol/L,则Na+的物质的量浓度为_______ ,加水稀释至1L后,Na2SO4的物质的量浓度为 _______
(4)常用的干燥剂有:①生石灰;②氢氧化钠固体;③变色硅胶(主要成分是二氧化硅,在其中掺入少量的无水氯化钴作指示剂);④五氧化二磷;⑤无水氯化钙;⑥浓硫酸。
①上述物质中,属于非电解质的是_______ (填字母,下同)。
A. ④ B. ③④ C.③④⑤ D. ③④⑤⑥
②上述干燥剂中①,其主要化学成分所属的类别为_______ 。
A.酸 B.碱 C.盐 D.酸性氧化物 E.碱性氧化物
③硅胶中无水氯化钴(CoCl2)呈蓝色,吸水后变为粉红色的CoCl2·6H2O,该变化过程属于_______ (填“物理变化”或“化学变化”)。
(1)在标准状况下,6.72L CO的物质的量为
(2)23g C2H5OH的氢原子数目为
(3)100mLNa2SO4溶液中, SO
 的物质的量浓度为1mol/L,则Na+的物质的量浓度为
的物质的量浓度为1mol/L,则Na+的物质的量浓度为(4)常用的干燥剂有:①生石灰;②氢氧化钠固体;③变色硅胶(主要成分是二氧化硅,在其中掺入少量的无水氯化钴作指示剂);④五氧化二磷;⑤无水氯化钙;⑥浓硫酸。
①上述物质中,属于非电解质的是
A. ④ B. ③④ C.③④⑤ D. ③④⑤⑥
②上述干燥剂中①,其主要化学成分所属的类别为
A.酸 B.碱 C.盐 D.酸性氧化物 E.碱性氧化物
③硅胶中无水氯化钴(CoCl2)呈蓝色,吸水后变为粉红色的CoCl2·6H2O,该变化过程属于
更新时间:2023-10-05 10:29:34
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】按要求填写下列空格:
(1)49g 的物质的量是
的物质的量是___________ 。
(2)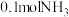 中所含质子数与
中所含质子数与___________ 克 中所含电子数相等。
中所含电子数相等。
(3)已知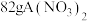 中含有
中含有 个
个 ,则该A的摩尔质量为
,则该A的摩尔质量为___________ 。
(4)39gNa2O2中的Na+数目为___________ NA,将其投入水中充分反应后产生标准状况下气体体积为___________ 。
(5)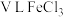 溶液中含
溶液中含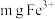 ,则溶液中
,则溶液中 的物质的量浓度为
的物质的量浓度为___________  。
。
(1)49g
 的物质的量是
的物质的量是(2)
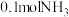 中所含质子数与
中所含质子数与 中所含电子数相等。
中所含电子数相等。(3)已知
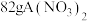 中含有
中含有 个
个 ,则该A的摩尔质量为
,则该A的摩尔质量为(4)39gNa2O2中的Na+数目为
(5)
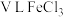 溶液中含
溶液中含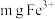 ,则溶液中
,则溶液中 的物质的量浓度为
的物质的量浓度为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】甲烷(CH4)是一种高效清洁能源,见天然气的主要成分。2017年我国在南海海域首次发现裸露的可燃冰,可燃冰是天然气水合物晶体,假设可燃冰的水笼里装的都是甲烷,理想的甲烷水合物的化学式为CH4·8H2O。请回答下列问题:
(1)甲烷水合物(CH4·8H2O)的摩尔质量为___________ ,其中质量分数最大的元素为___________ (填元素符号)。
(2)含有4.214×1024个氢原子的CH4的物质的量为___________ mol,质量为___________ g
(3)含0.2NA个氢原子的CH4,在标准状况下的体积约为___________ L
(4)常温常压下,等质量的CH4和H2的体积之比V(CH4):V(H2)=___________ ,前者所含氢原子个数与后者所含氢原子个数之比为___________
(1)甲烷水合物(CH4·8H2O)的摩尔质量为
(2)含有4.214×1024个氢原子的CH4的物质的量为
(3)含0.2NA个氢原子的CH4,在标准状况下的体积约为
(4)常温常压下,等质量的CH4和H2的体积之比V(CH4):V(H2)=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】CO和CO2是碳的重要氧化物
(1)在标准状况下,5.6升CO的物质的量是
(2)11克CO2的体积是
(3)等物质的量的CO和
 ,二者的质量之比
,二者的质量之比
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)在标准状况下①3.36L NH3②1.204×1023个CH4③18gH2O④0.4 mol HCl
a.体积由小到大的顺序_____________________________________ (填序号,下同);
b.氢原子个数由小到大的顺序____________________________________ 。
(2)18.6 g Na2X含有0.6 mol Na+,Na2X的摩尔质量为________ 。
(3)若a g某气体中含有的分子数为b,则c g该气体在标准状况下的体积是(设NA为阿伏伽德罗常数的值)________ L。
a.体积由小到大的顺序
b.氢原子个数由小到大的顺序
(2)18.6 g Na2X含有0.6 mol Na+,Na2X的摩尔质量为
(3)若a g某气体中含有的分子数为b,则c g该气体在标准状况下的体积是(设NA为阿伏伽德罗常数的值)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有以下物质:①H2SO4;②氯水;③KOH固体;④熔融KHSO4;⑤漂白粉;⑥生铁;⑦SO2;⑧Al2O3;⑨蔗糖。请回答下列问题:
(1)以上物质中能导电的是_______ (填序号),以上物质中属于电解质的是_______ (填序号)。以上物质中属于非电解质的是_______ (填序号)。
(2)某物质A加热时按化学方程式 分解,产物均为全体,测得相同条件下由生成物组成的混合气体对
分解,产物均为全体,测得相同条件下由生成物组成的混合气体对 的相对密度为50,则反应物A的摩尔质量为
的相对密度为50,则反应物A的摩尔质量为_______ 。
(3)标准状况下,将V L的氨气溶于1 L的水中,所得溶液的密度为 ,此氨水的物质的量浓度是
,此氨水的物质的量浓度是_______ mol/L:已知8 mol/L的氨水的密度为 ,2 mol/L的氨水的密度为
,2 mol/L的氨水的密度为 ,
, ,若将上述两种溶液等质量混合(忽略混合时体积变化),所得氨水的浓度
,若将上述两种溶液等质量混合(忽略混合时体积变化),所得氨水的浓度_______ 5 mol/L(填>、<或=)。
(1)以上物质中能导电的是
(2)某物质A加热时按化学方程式
 分解,产物均为全体,测得相同条件下由生成物组成的混合气体对
分解,产物均为全体,测得相同条件下由生成物组成的混合气体对 的相对密度为50,则反应物A的摩尔质量为
的相对密度为50,则反应物A的摩尔质量为(3)标准状况下,将V L的氨气溶于1 L的水中,所得溶液的密度为
 ,此氨水的物质的量浓度是
,此氨水的物质的量浓度是 ,2 mol/L的氨水的密度为
,2 mol/L的氨水的密度为 ,
, ,若将上述两种溶液等质量混合(忽略混合时体积变化),所得氨水的浓度
,若将上述两种溶液等质量混合(忽略混合时体积变化),所得氨水的浓度
您最近一年使用:0次
【推荐3】把铁、氧化铁、氧化铜的混合物粉末放入110mL4mol/L盐酸中,充分反应后产生896mLH2(标准状况),残留固体1.28g.过滤,滤液中无Cu2+,将滤液加水稀释到200mL,测得其中c(H+)=0.4mol/L。
请回答下列问题(请写出必要的解题过程):
(1)残留固体1.28g为___________ (填化学式)。
(2)原混合物粉末中,m(CuO)=___________ g。
(3)滤液稀释到200mL后,c(Fe2+)=___________ mol/L。
(4)稀释后,加入足量的硝酸银,产生沉淀的物质的量n(AgCl)=___________ mol。
(5)原混合物总质量为m(总)=___________ g。
请回答下列问题(请写出必要的解题过程):
(1)残留固体1.28g为
(2)原混合物粉末中,m(CuO)=
(3)滤液稀释到200mL后,c(Fe2+)=
(4)稀释后,加入足量的硝酸银,产生沉淀的物质的量n(AgCl)=
(5)原混合物总质量为m(总)=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】有如下物质:①铜;②NaOH溶液;③ 固体;④
固体;④ ;⑤酒精;⑥蒸馏水;⑦
;⑤酒精;⑥蒸馏水;⑦ 溶液;⑧
溶液;⑧ 晶体
晶体
(1)以上物质中,属于电解质的是_____ (填序号,下同),属于非电解质的是_____ 。
(2)已知蒸馏水有非常微弱的导电性,上述物质除⑥外,能导电的是_____ 。
(3)写出③溶于水的电离方程式_____ 。
(4)将②与⑦进行混合,该过程中发生的离子反应方程式是_____ 。
(5)向氢氧化钡溶液中加入物质③的溶液至恰好沉淀完全,其离子方程式为_____ 。
 固体;④
固体;④ ;⑤酒精;⑥蒸馏水;⑦
;⑤酒精;⑥蒸馏水;⑦ 溶液;⑧
溶液;⑧ 晶体
晶体(1)以上物质中,属于电解质的是
(2)已知蒸馏水有非常微弱的导电性,上述物质除⑥外,能导电的是
(3)写出③溶于水的电离方程式
(4)将②与⑦进行混合,该过程中发生的离子反应方程式是
(5)向氢氧化钡溶液中加入物质③的溶液至恰好沉淀完全,其离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.现有下列八种物质: ①铝 ②蔗糖 ③SiO2 ④H2SO4 ⑤NaOH ⑥FeSO4溶液 ⑦Ba(OH)2 ⑧氢氧化铁胶体。
(1)上述物质属于电解质的有____________ (填序号,下同),能导电的有__________ 。
(2)上述物质中有两种物质在水溶液中反应的离子方程式为H++OH−===H2O,则该反应的化学方程式为____________ 。
(3)实验室制备⑧的离子方程式为__________________ 。若在⑧中缓慢加入④的溶液,产生的现象是________________________ 。
(4)③是玻璃的主要成分之一,③与⑤溶液反应的化学方程式为_______________ ,工艺师常用_______ (填物质名称)来雕刻玻璃。
Ⅱ.下列各组物质的分离或提纯,应选用下述方法的哪一种? (填选项字母)
A.分液 B.过滤 C.萃取 D.蒸馏 E.蒸发结晶 F.高温分解
(5)分离CCl4和H2O:___________ 。
(6)除去澄清石灰水中悬浮的CaCO3:___________ 。
(7)分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物:__________ 。
(1)上述物质属于电解质的有
(2)上述物质中有两种物质在水溶液中反应的离子方程式为H++OH−===H2O,则该反应的化学方程式为
(3)实验室制备⑧的离子方程式为
(4)③是玻璃的主要成分之一,③与⑤溶液反应的化学方程式为
Ⅱ.下列各组物质的分离或提纯,应选用下述方法的哪一种? (填选项字母)
A.分液 B.过滤 C.萃取 D.蒸馏 E.蒸发结晶 F.高温分解
(5)分离CCl4和H2O:
(6)除去澄清石灰水中悬浮的CaCO3:
(7)分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】有下列物质:①NaCl固体 ②盐酸 ③ 溶液 ④铜 ⑤二氧化碳气体 ⑥硫酸氢钾固体 ⑦乙醇(
溶液 ④铜 ⑤二氧化碳气体 ⑥硫酸氢钾固体 ⑦乙醇( ) ⑧液态硫酸 ⑨熔融态
) ⑧液态硫酸 ⑨熔融态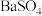 ⑩液态
⑩液态 。请回答下列问题(用序号):
。请回答下列问题(用序号):
(1)属于电解质的是_______ ;属于非电解质的是_______ 。
(2)上述状态下可导电的物质是_______ ;
(3) 是一种酸式盐,可用作清洁剂、防腐剂等。
是一种酸式盐,可用作清洁剂、防腐剂等。
① 溶于水时的电离方程式
溶于水时的电离方程式_______ 。
②少量 与
与 溶液混合,该反应的离子方程式为
溶液混合,该反应的离子方程式为_______ 。
③写出澄清石灰水与过量二氧化碳反应的离子方程式:_______ 。
 溶液 ④铜 ⑤二氧化碳气体 ⑥硫酸氢钾固体 ⑦乙醇(
溶液 ④铜 ⑤二氧化碳气体 ⑥硫酸氢钾固体 ⑦乙醇( ) ⑧液态硫酸 ⑨熔融态
) ⑧液态硫酸 ⑨熔融态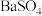 ⑩液态
⑩液态 。请回答下列问题(用序号):
。请回答下列问题(用序号):(1)属于电解质的是
(2)上述状态下可导电的物质是
(3)
 是一种酸式盐,可用作清洁剂、防腐剂等。
是一种酸式盐,可用作清洁剂、防腐剂等。①
 溶于水时的电离方程式
溶于水时的电离方程式②少量
 与
与 溶液混合,该反应的离子方程式为
溶液混合,该反应的离子方程式为③写出澄清石灰水与过量二氧化碳反应的离子方程式:
您最近一年使用:0次



