按要求填写下列空格:
(1)49g 的物质的量是
的物质的量是___________ 。
(2)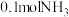 中所含质子数与
中所含质子数与___________ 克 中所含电子数相等。
中所含电子数相等。
(3)已知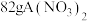 中含有
中含有 个
个 ,则该A的摩尔质量为
,则该A的摩尔质量为___________ 。
(4)39gNa2O2中的Na+数目为___________ NA,将其投入水中充分反应后产生标准状况下气体体积为___________ 。
(5)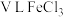 溶液中含
溶液中含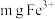 ,则溶液中
,则溶液中 的物质的量浓度为
的物质的量浓度为___________  。
。
(1)49g
 的物质的量是
的物质的量是(2)
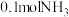 中所含质子数与
中所含质子数与 中所含电子数相等。
中所含电子数相等。(3)已知
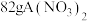 中含有
中含有 个
个 ,则该A的摩尔质量为
,则该A的摩尔质量为(4)39gNa2O2中的Na+数目为
(5)
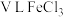 溶液中含
溶液中含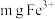 ,则溶液中
,则溶液中 的物质的量浓度为
的物质的量浓度为 。
。
更新时间:2024-01-06 09:50:02
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】按要求完成下列填空:
(1)某金属氯化物 的摩尔质量为
的摩尔质量为 ,取该金属氯化物
,取该金属氯化物 配成水溶液,与足量
配成水溶液,与足量 溶液完全反应,生成
溶液完全反应,生成 白色沉淀。则金属M的摩尔质量为
白色沉淀。则金属M的摩尔质量为___________ g/mol
(2)一定量的液态化合物 ,在一定量
,在一定量 中恰好完全反应:
中恰好完全反应: (注:l表示液态,g表示气态),冷却后在标准状况下,测得生成物的体积为
(注:l表示液态,g表示气态),冷却后在标准状况下,测得生成物的体积为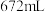 ,则反应前
,则反应前 的体积是
的体积是___________ mL,反应结束后,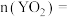
___________ mol
(3) 某物质的量浓度的
某物质的量浓度的 溶液中缓慢通入一定量的
溶液中缓慢通入一定量的 充分反应,再向上述所得溶液中逐滴滴加
充分反应,再向上述所得溶液中逐滴滴加 的盐酸,(忽略液体混合带来的体积变化)所得气体的体积与所加盐酸的体积关系如图所示:
的盐酸,(忽略液体混合带来的体积变化)所得气体的体积与所加盐酸的体积关系如图所示:
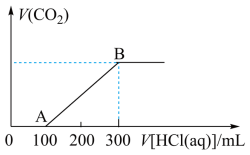
①OA段、AB段发生反应的化学方程式___________ 、___________ 。
②B点时,反应所得溶液中溶质的物质的量浓度是___________ mol/L
(1)某金属氯化物
 的摩尔质量为
的摩尔质量为 ,取该金属氯化物
,取该金属氯化物 配成水溶液,与足量
配成水溶液,与足量 溶液完全反应,生成
溶液完全反应,生成 白色沉淀。则金属M的摩尔质量为
白色沉淀。则金属M的摩尔质量为(2)一定量的液态化合物
 ,在一定量
,在一定量 中恰好完全反应:
中恰好完全反应: (注:l表示液态,g表示气态),冷却后在标准状况下,测得生成物的体积为
(注:l表示液态,g表示气态),冷却后在标准状况下,测得生成物的体积为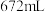 ,则反应前
,则反应前 的体积是
的体积是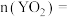
(3)
 某物质的量浓度的
某物质的量浓度的 溶液中缓慢通入一定量的
溶液中缓慢通入一定量的 充分反应,再向上述所得溶液中逐滴滴加
充分反应,再向上述所得溶液中逐滴滴加 的盐酸,(忽略液体混合带来的体积变化)所得气体的体积与所加盐酸的体积关系如图所示:
的盐酸,(忽略液体混合带来的体积变化)所得气体的体积与所加盐酸的体积关系如图所示:
①OA段、AB段发生反应的化学方程式
②B点时,反应所得溶液中溶质的物质的量浓度是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ、一密闭容器被无摩擦、可滑动的两隔板a和b分成甲、乙两室。标准状况下,在乙室中充入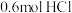 ,甲室中充入
,甲室中充入 、
、 的混合气体,静止时隔板位置如图。已知甲、乙两室中气体的质量之差为10.9g。回答下列问题:
的混合气体,静止时隔板位置如图。已知甲、乙两室中气体的质量之差为10.9g。回答下列问题:
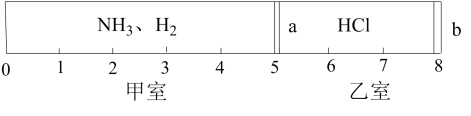
(1)甲室中气体的物质的量为___________ mol。
(2)甲室中气体的质量为___________ g。
(3)甲室中 、
、 的平均相对分子质量为
的平均相对分子质量为___________ 。
(4)经过查资料知道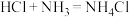 (
( 常温下是固体),如果将隔板a去掉,当
常温下是固体),如果将隔板a去掉,当 与
与 完全反应后,隔板b将静置于刻度“
完全反应后,隔板b将静置于刻度“___________ ”处(填数字)。
Ⅱ、现有下列基本粒子: 、
、 、
、 、
、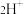 、
、 、
、 、
、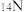 、
、 ,回答下列问题:
,回答下列问题:
(5)有___________ 种不同的核素。互为同素异形体的粒子为___________ 。
(6)中子数相等的是___________ 和___________ 。
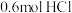 ,甲室中充入
,甲室中充入 、
、 的混合气体,静止时隔板位置如图。已知甲、乙两室中气体的质量之差为10.9g。回答下列问题:
的混合气体,静止时隔板位置如图。已知甲、乙两室中气体的质量之差为10.9g。回答下列问题:
(1)甲室中气体的物质的量为
(2)甲室中气体的质量为
(3)甲室中
 、
、 的平均相对分子质量为
的平均相对分子质量为(4)经过查资料知道
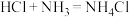 (
( 常温下是固体),如果将隔板a去掉,当
常温下是固体),如果将隔板a去掉,当 与
与 完全反应后,隔板b将静置于刻度“
完全反应后,隔板b将静置于刻度“Ⅱ、现有下列基本粒子:
 、
、 、
、 、
、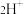 、
、 、
、 、
、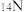 、
、 ,回答下列问题:
,回答下列问题:(5)有
(6)中子数相等的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】利用相关知识填空。
(1)标准状况下11.2LNH3中含___________ 个氨分子,含___________ mol氢原子。
(2)等质量的SO2和SO3物质的量之比是___________ :所含的氧原子个数之比是___________ 。
(3)4.8gCH4中所含氢原子数与___________ g水所含氢原子数相等。
(4)已知A是一种金属,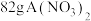 中含有
中含有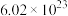 个硝酸根离子,则该硝酸盐的摩尔质量为
个硝酸根离子,则该硝酸盐的摩尔质量为___________ 。
(5)标况下,一定量的N2与22.4LCO所含电子的物质的量相等,则N2的质量是___________ 。
(6)在一定温度和压强下,0.4mol某气体的体积为9.8L,则该条件下的气体摩尔体积为___________ 。若此时压强为101kPa,则温度___________ 0℃ (填“高于”“低于”或“等于”)。
(7)有一种由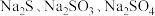 组成的混合物,经测定含硫25.6%,则混合物中含氧的质量分数为
组成的混合物,经测定含硫25.6%,则混合物中含氧的质量分数为___________ 。
(1)标准状况下11.2LNH3中含
(2)等质量的SO2和SO3物质的量之比是
(3)4.8gCH4中所含氢原子数与
(4)已知A是一种金属,
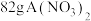 中含有
中含有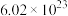 个硝酸根离子,则该硝酸盐的摩尔质量为
个硝酸根离子,则该硝酸盐的摩尔质量为(5)标况下,一定量的N2与22.4LCO所含电子的物质的量相等,则N2的质量是
(6)在一定温度和压强下,0.4mol某气体的体积为9.8L,则该条件下的气体摩尔体积为
(7)有一种由
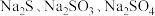 组成的混合物,经测定含硫25.6%,则混合物中含氧的质量分数为
组成的混合物,经测定含硫25.6%,则混合物中含氧的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题
(1)0.5mol水中含有___________ 个水分子;9g水与___________ g硫酸所含的分子数相等。
(2)100mL0.2mol/LNa2SO4溶液中Na+的物质的量浓度为___________ 。
(3)标准状况下,和2molNH3含有相同氢原子数的CH4的体积为___________ 。
(4)从1LAl2(SO4)3溶液中取出100mL,向其中加入200mL0.9mol·L-1的BaCl2溶液恰好使SO 完全沉淀,则原溶液中Al3+的物质的量浓度为
完全沉淀,则原溶液中Al3+的物质的量浓度为___________ 。
(5)12.4gNa2R含0.4molNa+,则Na2R的摩尔质量为___________ ,R的相对原子质量为___________ 。
(6)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,11.2L“人造空气”的质量是4.8g,其中氧气和氦气的分子数之比是___________ 。
(1)0.5mol水中含有
(2)100mL0.2mol/LNa2SO4溶液中Na+的物质的量浓度为
(3)标准状况下,和2molNH3含有相同氢原子数的CH4的体积为
(4)从1LAl2(SO4)3溶液中取出100mL,向其中加入200mL0.9mol·L-1的BaCl2溶液恰好使SO
 完全沉淀,则原溶液中Al3+的物质的量浓度为
完全沉淀,则原溶液中Al3+的物质的量浓度为(5)12.4gNa2R含0.4molNa+,则Na2R的摩尔质量为
(6)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,11.2L“人造空气”的质量是4.8g,其中氧气和氦气的分子数之比是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题。
(1)1molHNO3的质量是___________ ,1mol HNO3约含有___________ 个氮原子。
(2)标准状况下11.2LHCl气体的物质的量是___________ 。将此HCl气体 溶于水中配成1L溶液,所得盐酸溶液的物质的量浓度是 ___________ 。
(3)2molOH-含有___________ mol电子。
(1)1molHNO3的质量是
(2)标准状况下11.2LHCl气体的物质的量是
(3)2molOH-含有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】I.x、y、z三种气体的相对分子质量的关系为M(x)<M(y)=0.5M(z),则
(1)同温同压下,三种气体中密度最小的是__________ 。
(2)分子数目和等的三种气体,质量最大的是__________ 。
(3)20℃时,若2moly与1molz的体积相等,则y与z气体的压强比为__________ 。
II.丹砂炼汞的反应原理包括以下两个反应:
反应I:HgS+O2=Hg+SO2
反应II:HgS+CaO→Hg+CaS+CaSO4(未配平)
(4)反应I中,还原产物是__________ ,反应中每生成1molSO2,转移的电子数为__________ 。
(5)配平反应II,并用双线桥法标出反应中电子转移的方向和数目__________ 。
(1)同温同压下,三种气体中密度最小的是
(2)分子数目和等的三种气体,质量最大的是
(3)20℃时,若2moly与1molz的体积相等,则y与z气体的压强比为
II.丹砂炼汞的反应原理包括以下两个反应:
反应I:HgS+O2=Hg+SO2
反应II:HgS+CaO→Hg+CaS+CaSO4(未配平)
(4)反应I中,还原产物是
(5)配平反应II,并用双线桥法标出反应中电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】 是阿伏加德罗常数,完成下列问题。
是阿伏加德罗常数,完成下列问题。
(1)① ②
② ③
③ ④NaClO溶液⑤硫酸⑥乙醇⑦
④NaClO溶液⑤硫酸⑥乙醇⑦ ⑧
⑧ 溶液,上述物质属于强电解质的是
溶液,上述物质属于强电解质的是_______ ;14.9 g NaClO溶解在水中,要使 数与水分子数之比为1∶100,则需要水的个数为
数与水分子数之比为1∶100,则需要水的个数为_______ 。
(2) 可以通过下列反应制备:
可以通过下列反应制备: 。
。 是
是_______ (填“氧化产物”、“还原产物”或“氧化产物和还原产物”)。每生成1分子氧气,转移电子的数目为_______ 。
(3)砒霜低温下微溶于水,溶解的砒霜与水反应生成亚砷酸(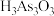 ),亚砷酸为三元弱酸。可用石灰水检验澄清溶液中是否含有砒霜,现象是有白色沉淀
),亚砷酸为三元弱酸。可用石灰水检验澄清溶液中是否含有砒霜,现象是有白色沉淀 生成,则石灰水与亚砷酸在溶液中反应的离子方程式为
生成,则石灰水与亚砷酸在溶液中反应的离子方程式为_______ 。
(4)次磷酸钙[ ,P是+1价]可用作食品添加剂和动物营养剂,以氢氧化钙为原料制备次磷酸钙的反应为:_______
,P是+1价]可用作食品添加剂和动物营养剂,以氢氧化钙为原料制备次磷酸钙的反应为:_______ _______
_______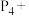 _______
_______ _______
_______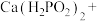 _______
_______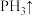 。配平该反应的化学方程式
。配平该反应的化学方程式_______ 。
 是阿伏加德罗常数,完成下列问题。
是阿伏加德罗常数,完成下列问题。(1)①
 ②
② ③
③ ④NaClO溶液⑤硫酸⑥乙醇⑦
④NaClO溶液⑤硫酸⑥乙醇⑦ ⑧
⑧ 溶液,上述物质属于强电解质的是
溶液,上述物质属于强电解质的是 数与水分子数之比为1∶100,则需要水的个数为
数与水分子数之比为1∶100,则需要水的个数为(2)
 可以通过下列反应制备:
可以通过下列反应制备: 。
。 是
是(3)砒霜低温下微溶于水,溶解的砒霜与水反应生成亚砷酸(
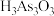 ),亚砷酸为三元弱酸。可用石灰水检验澄清溶液中是否含有砒霜,现象是有白色沉淀
),亚砷酸为三元弱酸。可用石灰水检验澄清溶液中是否含有砒霜,现象是有白色沉淀 生成,则石灰水与亚砷酸在溶液中反应的离子方程式为
生成,则石灰水与亚砷酸在溶液中反应的离子方程式为(4)次磷酸钙[
 ,P是+1价]可用作食品添加剂和动物营养剂,以氢氧化钙为原料制备次磷酸钙的反应为:_______
,P是+1价]可用作食品添加剂和动物营养剂,以氢氧化钙为原料制备次磷酸钙的反应为:_______ _______
_______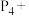 _______
_______ _______
_______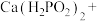 _______
_______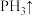 。配平该反应的化学方程式
。配平该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据要求回答下列问题:
(1)药物法匹拉韦的主要成分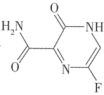 中氮原子的杂化轨道类型为
中氮原子的杂化轨道类型为_______ 。
(2)磷酸根离子的空间构型为_______ ,其中P的杂化轨道类型为_______ ;与 互为等电子体的阴离子有
互为等电子体的阴离子有_______ (写出一种离子符号)。
(3)在500~600℃的气相中,氯化铍以二聚体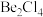 的形式存在,在该二聚体中
的形式存在,在该二聚体中 的杂化方式是
的杂化方式是_______ ,
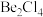 中含有配位键的数目为
中含有配位键的数目为_______ (用含 的代数式表示,设
的代数式表示,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(1)药物法匹拉韦的主要成分
 中氮原子的杂化轨道类型为
中氮原子的杂化轨道类型为(2)磷酸根离子的空间构型为
 互为等电子体的阴离子有
互为等电子体的阴离子有(3)在500~600℃的气相中,氯化铍以二聚体
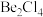 的形式存在,在该二聚体中
的形式存在,在该二聚体中 的杂化方式是
的杂化方式是
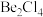 中含有配位键的数目为
中含有配位键的数目为 的代数式表示,设
的代数式表示,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】物质的量有关计算:
(1)a gNa2S中含有b个Na+,则阿伏加德罗常数为___________ 。(用含有a、b的代数式表示)
(2)若12.4 g Na2X中含有0.4 mol钠离子,Na2X的摩尔质量是___________ 。
(3)在相同的温度和压强下,A容器中CH4气体和B容器中NH3气体所含有的氢原子总数相等,则两个容器的体积比为___________ 。
(4)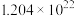 个CO2分子,含O的质量为
个CO2分子,含O的质量为___________ 。1mol 中含有
中含有___________ 个质子。
(5)同温同压下, 和
和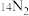 两种气体的密度之比为
两种气体的密度之比为___________ 。
(6)在标准状况下,由CO和CO2组成的混合气体13.44 L,质量为20 g,该混合气体中,碳与氧两种原子的数目之比为___________ 。
(7)固体A在一定温度下分解生成气体B、C、D,反应方程式为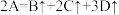 。若测得生成物气体对氢气的密度是15,则固体A的摩尔质量是
。若测得生成物气体对氢气的密度是15,则固体A的摩尔质量是___________ 。
(1)a gNa2S中含有b个Na+,则阿伏加德罗常数为
(2)若12.4 g Na2X中含有0.4 mol钠离子,Na2X的摩尔质量是
(3)在相同的温度和压强下,A容器中CH4气体和B容器中NH3气体所含有的氢原子总数相等,则两个容器的体积比为
(4)
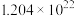 个CO2分子,含O的质量为
个CO2分子,含O的质量为 中含有
中含有(5)同温同压下,
 和
和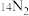 两种气体的密度之比为
两种气体的密度之比为(6)在标准状况下,由CO和CO2组成的混合气体13.44 L,质量为20 g,该混合气体中,碳与氧两种原子的数目之比为
(7)固体A在一定温度下分解生成气体B、C、D,反应方程式为
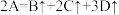 。若测得生成物气体对氢气的密度是15,则固体A的摩尔质量是
。若测得生成物气体对氢气的密度是15,则固体A的摩尔质量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】O2和O3是氧元素的两种单质,根据其分子式完成下列各题:
(1)等质量的O2和O3所含分子个数比为_______ ,原子个数比为_______ ,分子的物质的量之比为_______ 。
(2)等温等压下,等体积的O2和O3所含分子个数比为_______ ,原子个数比为_______ ,质量比为_______ 。
(3)设NA为阿伏加德罗常数的数值,如果a g氧气中含有的分子数为b,则c g氧气在标准状况下的体积约是_______ (用含NA的式子表示)。
(4)配制100 mL 1 mol/L的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84g·mL-1,质量分数为98%)的体积为_______ mL。
(5)氮化铝(AlN)广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:Al2O3+N2+3C=2AlN+3CO,请用双线桥法在化学方程式上标出该反应中电子转移的方向和数目_______ 。
(1)等质量的O2和O3所含分子个数比为
(2)等温等压下,等体积的O2和O3所含分子个数比为
(3)设NA为阿伏加德罗常数的数值,如果a g氧气中含有的分子数为b,则c g氧气在标准状况下的体积约是
(4)配制100 mL 1 mol/L的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84g·mL-1,质量分数为98%)的体积为
(5)氮化铝(AlN)广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:Al2O3+N2+3C=2AlN+3CO,请用双线桥法在化学方程式上标出该反应中电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】计算填空:
(1)同温同压下,同体积的甲烷( )和二氧化碳物质的量之比为
)和二氧化碳物质的量之比为___________ ,原子总数之比为___________ ,密度之比为___________ 。
(2)在标准状况下,①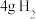 ②
② ③
③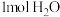 中,所含分子数最多的是
中,所含分子数最多的是___________ ,含原子数最多的是___________ ,质量最大的是___________ ,体积最小的是___________ 。(以上填序号)
(3)NO和 可发生反应:
可发生反应: ,现有
,现有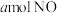 和
和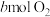 充分反应后氮原子与氧原子的个数比为
充分反应后氮原子与氧原子的个数比为___________ 。
(4)CO和 的混合气体
的混合气体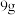 ,完全燃烧后测得
,完全燃烧后测得 体积为5.6L (标准状况),则混合气体中CO的质量是
体积为5.6L (标准状况),则混合气体中CO的质量是___________ g。
(1)同温同压下,同体积的甲烷(
 )和二氧化碳物质的量之比为
)和二氧化碳物质的量之比为(2)在标准状况下,①
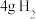 ②
② ③
③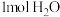 中,所含分子数最多的是
中,所含分子数最多的是(3)NO和
 可发生反应:
可发生反应: ,现有
,现有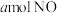 和
和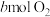 充分反应后氮原子与氧原子的个数比为
充分反应后氮原子与氧原子的个数比为(4)CO和
 的混合气体
的混合气体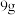 ,完全燃烧后测得
,完全燃烧后测得 体积为5.6L (标准状况),则混合气体中CO的质量是
体积为5.6L (标准状况),则混合气体中CO的质量是
您最近一年使用:0次



