锑( )冶炼过程中产生的副产物主要成分为
)冶炼过程中产生的副产物主要成分为 、
、 、
、 和
和 等,因含银量很高,是重要的银提取原料。从该副产物中提取银的工艺流程如下:
等,因含银量很高,是重要的银提取原料。从该副产物中提取银的工艺流程如下:

已知:①水合肼为 ,有很强的还原性;
,有很强的还原性;
② 在碱性条件下易转化为
在碱性条件下易转化为 ;
;
③常温下, 的溶解度为
的溶解度为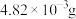 ,
, 的溶解度为0.79g。
的溶解度为0.79g。
回答下列问题:
(1) 的电子式为
的电子式为_______ 。
(2)脱氯渣的主要成分有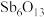 、
、 、
、 和
和_______ 。
(3)“还原脱氯”过程中会产生无色无味无毒气体,则 发生反应的化学方程式为
发生反应的化学方程式为_______ 。
(4)“氧化分银”中,不直接用硝酸的原因是_______ 。
(5)“氧化分银”中,银被氧化的离子方程式为_______ 。
(6)“沉铅过滤”中主要析出 的原因是
的原因是_______ 。
(7)“沉铅过滤”中硫酸的用量系数对铅和银的沉淀率影响如图所示。
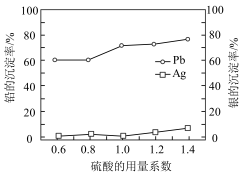
硫酸的用量系数最佳选择是_______ ,理由是_______ 。
 )冶炼过程中产生的副产物主要成分为
)冶炼过程中产生的副产物主要成分为 、
、 、
、 和
和 等,因含银量很高,是重要的银提取原料。从该副产物中提取银的工艺流程如下:
等,因含银量很高,是重要的银提取原料。从该副产物中提取银的工艺流程如下:
已知:①水合肼为
 ,有很强的还原性;
,有很强的还原性;②
 在碱性条件下易转化为
在碱性条件下易转化为 ;
;③常温下,
 的溶解度为
的溶解度为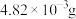 ,
, 的溶解度为0.79g。
的溶解度为0.79g。回答下列问题:
(1)
 的电子式为
的电子式为(2)脱氯渣的主要成分有
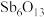 、
、 、
、 和
和(3)“还原脱氯”过程中会产生无色无味无毒气体,则
 发生反应的化学方程式为
发生反应的化学方程式为(4)“氧化分银”中,不直接用硝酸的原因是
(5)“氧化分银”中,银被氧化的离子方程式为
(6)“沉铅过滤”中主要析出
 的原因是
的原因是(7)“沉铅过滤”中硫酸的用量系数对铅和银的沉淀率影响如图所示。

硫酸的用量系数最佳选择是
更新时间:2023-11-26 11:34:53
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
名校
【推荐1】已知A、B、C、D、E五种元素为周期表前20号元素且原子序数依次增大,其中只有A、D为非金属元素。A的气态氢化物溶于水得到的溶液能使酚酞溶液变红。B、C、D的最高价氧化物对应水化物相互之间能够两两反应,且D原子最外层电子数是C原子最外层电子数的2倍。B、E元素同主族。
(1)E在元素周期表中的位置:____________ ,写出E的最高价氧化物对应水化物与C的单质反应的化学方程式:___________________________________ 。
(2)A的气态氢化物溶于水后的电离方程式为________________________________ 。
(3)B单质在空气中燃烧后的产物的电子式为____________ ,产物中存在的化学键类型有_______________ 。
(1)E在元素周期表中的位置:
(2)A的气态氢化物溶于水后的电离方程式为
(3)B单质在空气中燃烧后的产物的电子式为
您最近一年使用:0次
【推荐2】化合物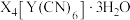 是一种摩尔质量在
是一种摩尔质量在 之间的黄色晶体(X、Y为前四周期两种元素)。取一定量的
之间的黄色晶体(X、Y为前四周期两种元素)。取一定量的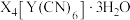 晶体完成如图转化,其中A为无色有毒气体,B、C、D是三种酸根相同的盐,B中阳离子具有较强的还原性,C溶液的焰色反应为紫色。
晶体完成如图转化,其中A为无色有毒气体,B、C、D是三种酸根相同的盐,B中阳离子具有较强的还原性,C溶液的焰色反应为紫色。
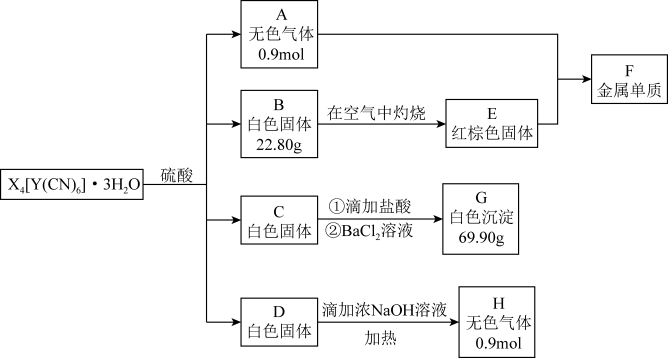
(1)写出H的电子式_______ 。
(2)A与E反应生成F的化学方程式为_______ 。
(3)单质F与过量稀硝酸反应的化学方程式为_______ 。
(4)实验室制备气体H的化学方程式是_____ 。实验室收集气体H时,验满的方法是_____ 。
(5)已知该黄色晶体受热脱水过程的热重曲线(样品质量随温度的变化曲线)如下图所示。

试确定150℃时固体物质的化学式_______ 。
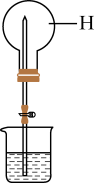
(6)当下图装置中圆底烧瓶内集满气体H后,引发喷泉的实验操作是_______ 。
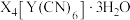 是一种摩尔质量在
是一种摩尔质量在 之间的黄色晶体(X、Y为前四周期两种元素)。取一定量的
之间的黄色晶体(X、Y为前四周期两种元素)。取一定量的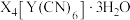 晶体完成如图转化,其中A为无色有毒气体,B、C、D是三种酸根相同的盐,B中阳离子具有较强的还原性,C溶液的焰色反应为紫色。
晶体完成如图转化,其中A为无色有毒气体,B、C、D是三种酸根相同的盐,B中阳离子具有较强的还原性,C溶液的焰色反应为紫色。
(1)写出H的电子式
(2)A与E反应生成F的化学方程式为
(3)单质F与过量稀硝酸反应的化学方程式为
(4)实验室制备气体H的化学方程式是
(5)已知该黄色晶体受热脱水过程的热重曲线(样品质量随温度的变化曲线)如下图所示。

试确定150℃时固体物质的化学式
(6)当下图装置中圆底烧瓶内集满气体H后,引发喷泉的实验操作是

您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐3】有X、Y、Z三种短周期元素,已知X的气态氢化物的分子式为H2X,该氢化物的相对分子质量与X最高价氧化物的相对分子质量之比为17∶40,X原子核内质子数与中子数相等;Y与X可形成离子化合物Y2X,Y的阳离子的电子层结构与Ne相同。Z与X处于同一周期,其气态单质是双原子分子,两原子共用一对电子。
(1)写出各元素的符号:X______ ,Y______ ,Z______ 。
(2)X的相对原子质量为____________ ,其离子的结构示意图为________ 。
(3)Y单质在空气中燃烧的化学方程式是________________________ ,该生成物与水反应的化学方程式是______________________ 。
(4)X与氢气化合的产物的电子式为________ 。
(1)写出各元素的符号:X
(2)X的相对原子质量为
(3)Y单质在空气中燃烧的化学方程式是
(4)X与氢气化合的产物的电子式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】稀土是一种重要的战略资源。氟碳铈矿的主要化学成分为 ,它是提取铈(Ce)等稀土元素的重要矿物原料。常温下,氟碳铈矿的冶炼工艺流程如下:
,它是提取铈(Ce)等稀土元素的重要矿物原料。常温下,氟碳铈矿的冶炼工艺流程如下:

已知:i.Ce元素的常见化合价为+3、+4.焙烧后Ce元素转化成 和
和 。+4价的Ce元素不易进入溶液,而+3价稀土元素易进入溶液。
。+4价的Ce元素不易进入溶液,而+3价稀土元素易进入溶液。
ii.酸浸Ⅱ中发生反应: 。
。
请回答下列问题:
(1)①焙烧氟碳铈矿的目的是___________ 。
②焙烧后产生的 是汽车尾气净化催化剂的关键成分,它能在还原气氛中供氧,在氧化气氛中耗氧。在尾气消除过程中发生反应
是汽车尾气净化催化剂的关键成分,它能在还原气氛中供氧,在氧化气氛中耗氧。在尾气消除过程中发生反应 ,写出
,写出 消除CO尾气的化学方程式:
消除CO尾气的化学方程式:___________ 。
(2)操作I的名称为___________ ,在实验室中进行操作Ⅱ时所需要的玻璃仪器有___________ 、___________ 。
(3)操作I后,向溶液中加入NaOH溶液来调节溶液的pH,以获得 沉淀,常温下加入NaOH溶液调节溶液的
沉淀,常温下加入NaOH溶液调节溶液的
___________ ,即可认为 已完全沉淀。(已知:常温下,
已完全沉淀。(已知:常温下, )
)
(4)取上述流程中得到的 产品5.000g,加酸溶解后,向其中加入含
产品5.000g,加酸溶解后,向其中加入含 的
的 溶液使
溶液使 全部被还原成
全部被还原成 ,再用
,再用 的酸性
的酸性 标准溶液滴定至终点时,消耗20.00mL标准溶液,则该产品中
标准溶液滴定至终点时,消耗20.00mL标准溶液,则该产品中 的质量分数为
的质量分数为___________ [已知氧化性: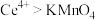 ;
; 的相对分子质量为208]。(写出计算过程)
的相对分子质量为208]。(写出计算过程)
已知:
 ,它是提取铈(Ce)等稀土元素的重要矿物原料。常温下,氟碳铈矿的冶炼工艺流程如下:
,它是提取铈(Ce)等稀土元素的重要矿物原料。常温下,氟碳铈矿的冶炼工艺流程如下:
已知:i.Ce元素的常见化合价为+3、+4.焙烧后Ce元素转化成
 和
和 。+4价的Ce元素不易进入溶液,而+3价稀土元素易进入溶液。
。+4价的Ce元素不易进入溶液,而+3价稀土元素易进入溶液。ii.酸浸Ⅱ中发生反应:
 。
。请回答下列问题:
(1)①焙烧氟碳铈矿的目的是
②焙烧后产生的
 是汽车尾气净化催化剂的关键成分,它能在还原气氛中供氧,在氧化气氛中耗氧。在尾气消除过程中发生反应
是汽车尾气净化催化剂的关键成分,它能在还原气氛中供氧,在氧化气氛中耗氧。在尾气消除过程中发生反应 ,写出
,写出 消除CO尾气的化学方程式:
消除CO尾气的化学方程式:(2)操作I的名称为
(3)操作I后,向溶液中加入NaOH溶液来调节溶液的pH,以获得
 沉淀,常温下加入NaOH溶液调节溶液的
沉淀,常温下加入NaOH溶液调节溶液的
 已完全沉淀。(已知:常温下,
已完全沉淀。(已知:常温下, )
)(4)取上述流程中得到的
 产品5.000g,加酸溶解后,向其中加入含
产品5.000g,加酸溶解后,向其中加入含 的
的 溶液使
溶液使 全部被还原成
全部被还原成 ,再用
,再用 的酸性
的酸性 标准溶液滴定至终点时,消耗20.00mL标准溶液,则该产品中
标准溶液滴定至终点时,消耗20.00mL标准溶液,则该产品中 的质量分数为
的质量分数为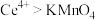 ;
; 的相对分子质量为208]。(写出计算过程)
的相对分子质量为208]。(写出计算过程)已知:

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐2】金属及其化合物在生产中用途广泛。
Ⅰ.从含铜丰富的自然资源黄铜矿(CuFeS2)冶炼铜的工艺流程如下:
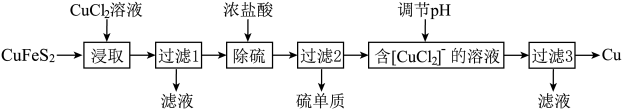
已知:CuFeS2+3CuCl2=4CuCl↓+FeCl2+2S↓
(1)浸取时,若改用FeCl3溶液,也能生成CuCl和S,该反应化学方程式为___________ 。
(2)若过滤1所得滤液中只含FeCl2,则将其在空气中加热蒸干、灼烧后,所得固体的化学式为___________ 。
(3)调节溶液的pH后,除生成Cu外,还能产生一种金属离子,此金属离子是___________ 。(填离子符号)
(4)过滤3所得滤液中可以循环使用的物质有____________ ,为保持流程持续循环,每生成1molCu,理论上需补充CuCl2的物质的量为____________ 。
Ⅱ.利用生产硼砂的废渣——硼镁泥(主要成分为MgCO3、SiO2,还含有少量Fe2O3、MnO、CaO等)为主要原料制取轻质碳酸镁[MgCO3·Mg(OH)2·2H2O]的工业流程如下:
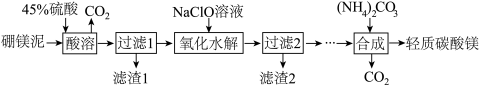
(5)写出“酸溶”一步中,MgCO3和硫酸反应的离子方程式_____________________ 。
(6)滤渣2的主要成分有MnO2和_____________ ,写出生成MnO2的离子方程式____________________ 。
(7)“合成”时需通蒸汽至80 ℃,边加热边搅拌,温度控制在80 ℃的原因是________________________ (只需写出相应的化学方程式)。
Ⅰ.从含铜丰富的自然资源黄铜矿(CuFeS2)冶炼铜的工艺流程如下:

已知:CuFeS2+3CuCl2=4CuCl↓+FeCl2+2S↓
(1)浸取时,若改用FeCl3溶液,也能生成CuCl和S,该反应化学方程式为
(2)若过滤1所得滤液中只含FeCl2,则将其在空气中加热蒸干、灼烧后,所得固体的化学式为
(3)调节溶液的pH后,除生成Cu外,还能产生一种金属离子,此金属离子是
(4)过滤3所得滤液中可以循环使用的物质有
Ⅱ.利用生产硼砂的废渣——硼镁泥(主要成分为MgCO3、SiO2,还含有少量Fe2O3、MnO、CaO等)为主要原料制取轻质碳酸镁[MgCO3·Mg(OH)2·2H2O]的工业流程如下:

(5)写出“酸溶”一步中,MgCO3和硫酸反应的离子方程式
(6)滤渣2的主要成分有MnO2和
(7)“合成”时需通蒸汽至80 ℃,边加热边搅拌,温度控制在80 ℃的原因是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】以 为载体的钯催化剂常用于石化行业加氢催化裂化过程中,工业上以失活后的废
为载体的钯催化剂常用于石化行业加氢催化裂化过程中,工业上以失活后的废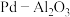 催化剂(主要含有Pd、
催化剂(主要含有Pd、 ,还有少量PdO、
,还有少量PdO、 、C)为原料制备氯化钯的流程如下:
、C)为原料制备氯化钯的流程如下:
(1)“氯化浸出”前必须“焙烧”去除废催化剂表面积碳,原因是_______ ,焙烧时间过长,“氯化浸出”率下降,可能的原因是_______ 。
(2) 中Cl原子的杂化类型是
中Cl原子的杂化类型是_______ ,“氯化浸出”时,若盐酸浓度过高,可能发生的副反应离子方程式为_______ 。
(3)滤渣1主要成分为_______ ,已知 ,若要使溶液中
,若要使溶液中 不高于
不高于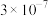 ,则应加入氨水使pH不低于
,则应加入氨水使pH不低于_______ 。
(4)工业上也可用 还原
还原 制取海绵Pd,该历程对环境友好。该反应的化学方程式为
制取海绵Pd,该历程对环境友好。该反应的化学方程式为_______ 。
(5)工业上测定Pd含量的原理为:试样用硝酸及盐酸溶解后,加过量EDTA络合钯,用锌标准溶液滴定过剩的EDTA.具体步聚如下:
I.标定锌标准溶液对钯的滴定度:
a.吸取25mLEDTA溶液置于烧杯中,滴加4~5滴盐酸,加适量水,用锌标准溶液滴定至终点,消耗锌标准溶液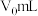 。
。
b.吸取15mL含0.0010gPd的Pd标准溶液于烧杯中,加入25mLEDTA溶液,加适量水用锌标准溶液滴定至试液由黄色变成紫红色为终点,消耗锌标准溶液 。
。
Ⅱ.滴定式样:
称取0.1000g试样置于烧杯中,加适量硝酸及盐酸充分溶解并作妥善处理,加入25mLEDT溶液,用锌标准溶液滴定至终点,消耗锌标准溶液VmL。则试样中Pd的质量分数为_______ %(用含V、 、
、 的式子表示)。
的式子表示)。
 为载体的钯催化剂常用于石化行业加氢催化裂化过程中,工业上以失活后的废
为载体的钯催化剂常用于石化行业加氢催化裂化过程中,工业上以失活后的废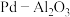 催化剂(主要含有Pd、
催化剂(主要含有Pd、 ,还有少量PdO、
,还有少量PdO、 、C)为原料制备氯化钯的流程如下:
、C)为原料制备氯化钯的流程如下: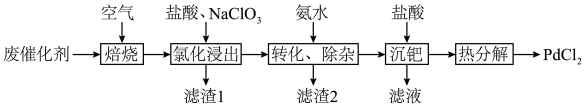
(1)“氯化浸出”前必须“焙烧”去除废催化剂表面积碳,原因是
(2)
 中Cl原子的杂化类型是
中Cl原子的杂化类型是(3)滤渣1主要成分为
 ,若要使溶液中
,若要使溶液中 不高于
不高于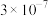 ,则应加入氨水使pH不低于
,则应加入氨水使pH不低于(4)工业上也可用
 还原
还原 制取海绵Pd,该历程对环境友好。该反应的化学方程式为
制取海绵Pd,该历程对环境友好。该反应的化学方程式为(5)工业上测定Pd含量的原理为:试样用硝酸及盐酸溶解后,加过量EDTA络合钯,用锌标准溶液滴定过剩的EDTA.具体步聚如下:
I.标定锌标准溶液对钯的滴定度:
a.吸取25mLEDTA溶液置于烧杯中,滴加4~5滴盐酸,加适量水,用锌标准溶液滴定至终点,消耗锌标准溶液
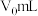 。
。b.吸取15mL含0.0010gPd的Pd标准溶液于烧杯中,加入25mLEDTA溶液,加适量水用锌标准溶液滴定至试液由黄色变成紫红色为终点,消耗锌标准溶液
 。
。Ⅱ.滴定式样:
称取0.1000g试样置于烧杯中,加适量硝酸及盐酸充分溶解并作妥善处理,加入25mLEDT溶液,用锌标准溶液滴定至终点,消耗锌标准溶液VmL。则试样中Pd的质量分数为
 、
、 的式子表示)。
的式子表示)。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】2020年6月比亚迪正式发布采用磷酸铁锂技术的刀片电池,大幅度提高了电动汽车的续航里程,可媲美特斯拉。以硫铁矿(主要成分是FeS2,含少量Al2O3、SiO2和Fe3O4)为原料制备LiFePO4的流程如下:
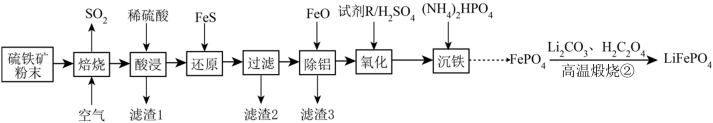
已知几种金属离子沉淀的pH如表所示:
请回答下列问题:
(1)“酸浸”需要适当加热,但温度不宜过高,其原因是___________ 。灼烧滤渣3得到固体的主要成分是___________ (写出化学式)。
(2)用FeS还原Fe3+的目的是___________ ,加入FeO的作用是___________ (用离子反应方程式表示)。
(3)试剂R宜选择___________ (填字母)。
A.高锰酸钾 B.稀硝酸 C.双氧水 D.次氯酸钠
(4)常温下,Ksp(FePO4)=1.3×10-22,“沉铁”中为了使c(Fe3+)≤1×10-5 mol·L-1,c(PO )最小为
)最小为___________ mol·L-1。
(5)写出“高温煅烧②”中由FePO4制备LiFePO4的化学方程式:___________ 。

已知几种金属离子沉淀的pH如表所示:
| 金属氢氧化物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀的pH | 2.3 | 7.5 | 4.0 |
| 完全沉淀的pH | 4.1 | 9.7 | 5.2 |
(1)“酸浸”需要适当加热,但温度不宜过高,其原因是
(2)用FeS还原Fe3+的目的是
(3)试剂R宜选择
A.高锰酸钾 B.稀硝酸 C.双氧水 D.次氯酸钠
(4)常温下,Ksp(FePO4)=1.3×10-22,“沉铁”中为了使c(Fe3+)≤1×10-5 mol·L-1,c(PO
 )最小为
)最小为(5)写出“高温煅烧②”中由FePO4制备LiFePO4的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐2】铬铁矿(FeCr2O4)中含有Al2O3、Fe2O3等杂质,以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的工艺流程示意图如下(部分操作和条件略):
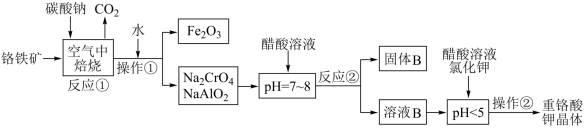
(1)铬铁矿(FeCr2O4)改写为氧化物的形式为______________________ 。
(2)反应①中发生了两个主要反应,其中一个主要反应的化学方程式为Na2CO3 + Al2O3 2NaAlO2 + CO2↑,另一个主要反应的化学方程式为
2NaAlO2 + CO2↑,另一个主要反应的化学方程式为_____________________ 。
(3)写出反应②中生成固体B的离子方程式_______________________ 。
(4)下表是相关物质的溶解度数据:
pH﹤5时,发生反应的化学方程式之一为Na2Cr2O7 + 2KCl K2Cr2O7 + 2NaCl。该反应能发生的理由是
K2Cr2O7 + 2NaCl。该反应能发生的理由是____________________________________________________________________________ 。
(5)某种酒精测试仪中,K2Cr2O7在酸性条件下将乙醇氧化为乙酸,自身被还原为三价铬离子,该反应的离子方程式为__________________________________ 。
(6)已知Ksp[Fe(OH)3] = 4.0×10-38,Ksp[Cr(OH)3] = 6.0×10-31 。含铬废渣废水的随意排放对人类生活环境有极大的危害,电解法是处理铬污染的一种方法,电解时,在阴极区有Fe(OH)3和Cr(OH)3沉淀生成,已知电解后的溶液中c(Cr3+)为3.0×10-5 mol·L-1,则溶液中c(Fe3+)为________ mol·L-1。

(1)铬铁矿(FeCr2O4)改写为氧化物的形式为
(2)反应①中发生了两个主要反应,其中一个主要反应的化学方程式为Na2CO3 + Al2O3
 2NaAlO2 + CO2↑,另一个主要反应的化学方程式为
2NaAlO2 + CO2↑,另一个主要反应的化学方程式为(3)写出反应②中生成固体B的离子方程式
(4)下表是相关物质的溶解度数据:
| 物质 | 溶解度(g/100g H2O) | 物质 | 溶解度(g/100g H2O) | ||||
| 0℃ | 40℃ | 80℃ | 0℃ | 40℃ | 80℃ | ||
| KCl | 28 | 40.1 | 51.3 | K2Cr2O7 | 4.7 | 26.3 | 73 |
| NaCl | 35.7 | 36.4 | 38 | Na2Cr2O7 | 163 | 215 | 376 |
pH﹤5时,发生反应的化学方程式之一为Na2Cr2O7 + 2KCl
 K2Cr2O7 + 2NaCl。该反应能发生的理由是
K2Cr2O7 + 2NaCl。该反应能发生的理由是(5)某种酒精测试仪中,K2Cr2O7在酸性条件下将乙醇氧化为乙酸,自身被还原为三价铬离子,该反应的离子方程式为
(6)已知Ksp[Fe(OH)3] = 4.0×10-38,Ksp[Cr(OH)3] = 6.0×10-31 。含铬废渣废水的随意排放对人类生活环境有极大的危害,电解法是处理铬污染的一种方法,电解时,在阴极区有Fe(OH)3和Cr(OH)3沉淀生成,已知电解后的溶液中c(Cr3+)为3.0×10-5 mol·L-1,则溶液中c(Fe3+)为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】以高铅硫化锌原矿[主要含有ZnS,含有少量PbS、 、
、 、FeS、
、FeS、 (氧化铟)等]为原料制备单质Zn的工艺流程如图所示:
(氧化铟)等]为原料制备单质Zn的工艺流程如图所示: 。
。
②电解液浓度过大会导致溶液黏度变大,离子迁移速率低,电解效率低。
回答下列问题:
(1)“沸腾焙烧”的目的是______ ;其中杂质FeS充分焙烧产生大量废气,废气中主要成分的空间结构为______ 。
(2)“滤渣Ⅰ”的主要成分为______ 。
(3)“除铁”时 转化为FeOOH的离子方程式为
转化为FeOOH的离子方程式为______ 。
(4)“电解”硫酸锌溶液制备Zn的化学方程式为______ ,工业所需电解液浓度为40~60 的理由是
的理由是______ ,可用______ 光谱证明阴极析出的固体为Zn。
 、
、 、FeS、
、FeS、 (氧化铟)等]为原料制备单质Zn的工艺流程如图所示:
(氧化铟)等]为原料制备单质Zn的工艺流程如图所示:
 。
。②电解液浓度过大会导致溶液黏度变大,离子迁移速率低,电解效率低。
回答下列问题:
(1)“沸腾焙烧”的目的是
(2)“滤渣Ⅰ”的主要成分为
(3)“除铁”时
 转化为FeOOH的离子方程式为
转化为FeOOH的离子方程式为(4)“电解”硫酸锌溶液制备Zn的化学方程式为
 的理由是
的理由是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
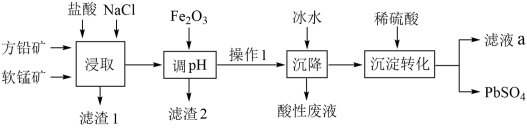
【推荐1】利用软锰矿和方铅矿(主要成分为PbS,含有 等杂质)制备
等杂质)制备 的工艺流程如图:
的工艺流程如图:
已知: ;
;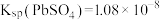 ,
,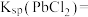
 ;
; 易溶于热水。
易溶于热水。
(1)“滤渣1”的成分是S(硫),“浸取”时被氧化的元素是_______ ,“浸取”反应的条件是_______ 。
(2)“滤渣2”的成分是_______ 。
(3)加入冰水“沉降”的离子方程式为_______ ,“酸性溶液”中的主要金属阳离子是_______ 。
(4)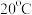 时,
时,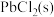 在不同浓度的盐酸中的最大溶解量(
在不同浓度的盐酸中的最大溶解量(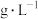 )如图所示。下列叙述正确的是
)如图所示。下列叙述正确的是_______ (填字母代号)
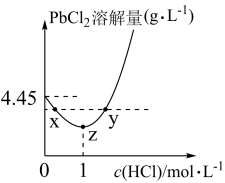
A.z→y,发生了沉淀溶解反应
B.x、y两点对应的溶液中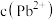 相等
相等
C.x→z, 增大使
增大使 溶解平衡逆向移动
溶解平衡逆向移动
D.盐酸浓度越小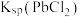 )越小
)越小
(5)“滤液a”经过处理后可以返回到_______ 工序循环使用; 经“沉淀转化”后得到
经“沉淀转化”后得到 ,当
,当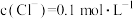 时,
时,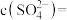
_______  。
。
 等杂质)制备
等杂质)制备 的工艺流程如图:
的工艺流程如图:
已知:
 ;
;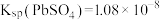 ,
,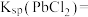
 ;
; 易溶于热水。
易溶于热水。(1)“滤渣1”的成分是S(硫),“浸取”时被氧化的元素是
(2)“滤渣2”的成分是
(3)加入冰水“沉降”的离子方程式为
(4)
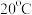 时,
时,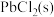 在不同浓度的盐酸中的最大溶解量(
在不同浓度的盐酸中的最大溶解量(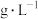 )如图所示。下列叙述正确的是
)如图所示。下列叙述正确的是
A.z→y,发生了沉淀溶解反应
B.x、y两点对应的溶液中
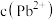 相等
相等C.x→z,
 增大使
增大使 溶解平衡逆向移动
溶解平衡逆向移动D.盐酸浓度越小
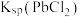 )越小
)越小(5)“滤液a”经过处理后可以返回到
 经“沉淀转化”后得到
经“沉淀转化”后得到 ,当
,当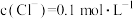 时,
时,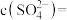
 。
。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】鞣革废水中含大量的Cr(VI)对环境有污染,工业上可以用还原法处理。
I.还原沉淀法
(1)Cr(VI)在水溶液中有 、
、 、
、 和
和 四种存在形式(
四种存在形式( 是二元弱酸),
是二元弱酸), 部分转化为
部分转化为 的离子方程式为
的离子方程式为___________ 。
(2)在pH=2的废水中,Cr(VI)主要以 和
和 的形式存在,选用还原剂FeSO4处理此废水,生成
的形式存在,选用还原剂FeSO4处理此废水,生成 沉淀,
沉淀, 还原
还原 时,两者物质的量之比为
时,两者物质的量之比为___________ 。实际投入FeSO4的量需大于上述计算值的可能原因是___________ 。
Ⅱ.还原吸附法
(3)纳米磁性Fe3O4的制备
以FeSO4和Fe2(SO4)3为原料,在氨水存在的条件下反应可生成纳米磁性Fe3O4,发生反应的化学方程式为___________ 。
(4)纳米磁性Fe3O4的修饰
某研究小组经查阅资料,发现纳米磁性Fe3O4颗粒粒径小,比表面积大,但极易发生团聚。在纳米磁性Fe3O4颗粒表面修饰SiO2(记作Fe3O4@ SiO2),可优化纳米磁性Fe3O4降解废水中 的性能,其原因是
的性能,其原因是___________ 。
(5) Fe3O4@SiO2-GO还原吸附
氧化石墨烯(记作GO)表面含有-COOH等含氧官能团,将氧化石墨烯嫁接在Fe3O4@SiO2的表面得到Fe3O4@SiO2-GO,其去除废水中Cr(VI)的过程如下:

“吸附”过程中,氧化石墨烯表面带电微粒与Cr3+之间的静电作用是实现“吸附”的重要因素,溶液中Cr3+去除率随pH变化如图所示。

①pH较小时,Cr3+去除率较低的原因是___________ 。
②实际除Cr3+时,控制pH约为6,而不选择更高pH的原因是___________ 。
I.还原沉淀法
(1)Cr(VI)在水溶液中有
 、
、 、
、 和
和 四种存在形式(
四种存在形式( 是二元弱酸),
是二元弱酸), 部分转化为
部分转化为 的离子方程式为
的离子方程式为(2)在pH=2的废水中,Cr(VI)主要以
 和
和 的形式存在,选用还原剂FeSO4处理此废水,生成
的形式存在,选用还原剂FeSO4处理此废水,生成 沉淀,
沉淀, 还原
还原 时,两者物质的量之比为
时,两者物质的量之比为Ⅱ.还原吸附法
(3)纳米磁性Fe3O4的制备
以FeSO4和Fe2(SO4)3为原料,在氨水存在的条件下反应可生成纳米磁性Fe3O4,发生反应的化学方程式为
(4)纳米磁性Fe3O4的修饰
某研究小组经查阅资料,发现纳米磁性Fe3O4颗粒粒径小,比表面积大,但极易发生团聚。在纳米磁性Fe3O4颗粒表面修饰SiO2(记作Fe3O4@ SiO2),可优化纳米磁性Fe3O4降解废水中
 的性能,其原因是
的性能,其原因是(5) Fe3O4@SiO2-GO还原吸附
氧化石墨烯(记作GO)表面含有-COOH等含氧官能团,将氧化石墨烯嫁接在Fe3O4@SiO2的表面得到Fe3O4@SiO2-GO,其去除废水中Cr(VI)的过程如下:

“吸附”过程中,氧化石墨烯表面带电微粒与Cr3+之间的静电作用是实现“吸附”的重要因素,溶液中Cr3+去除率随pH变化如图所示。

①pH较小时,Cr3+去除率较低的原因是
②实际除Cr3+时,控制pH约为6,而不选择更高pH的原因是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】利用低品位软锰矿浆(主要成分是MnO2,少量的Fe3+、Al3+等)吸收高温焙烧含硫废渣产生的SO2废气,制备硫酸锰晶体可实现资源的综合利用和环境治理。
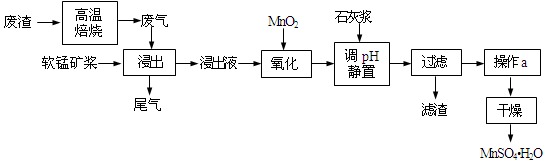
已知,浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+等其他金属离子。有关金属离子形成氢氧化物沉淀时的pH见表:
(1)写出浸出过程中主要反应的化学方程式_____________________________ 。为了提高软锰矿的浸取率,可以采取的措施除了充分搅拌外还有:_____________________ (至少答两点)。
(2)写出氧化过程中主要反应的离子方程式:_____________________________ 。
(3)①在氧化后的液体中加入石灰浆,用于调节pH,pH应调节至______ 。②若加入的石灰浆过多,会使得MnSO4•H2O晶体中含有较多杂质,其原因是_____________________________ 。
(4)下列各组试剂中,能准确测定尾气中SO2含量的是______ (选填序号)。
a.NaOH溶液、品红溶液 b.稀H2SO4酸化的KMnO4溶液 c.碘水、淀粉溶液

已知,浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+等其他金属离子。有关金属离子形成氢氧化物沉淀时的pH见表:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH | 加碱溶解的pH |
| Fe2+ | 7.6 | 9.7 | |
| Fe3+ | 2.7 | 3.7 | |
| Al3+ | 3.8 | 4.7 | >8.5 |
| Mn2+ | 8.3 | 9.8 |
(2)写出氧化过程中主要反应的离子方程式:
(3)①在氧化后的液体中加入石灰浆,用于调节pH,pH应调节至
(4)下列各组试剂中,能准确测定尾气中SO2含量的是
a.NaOH溶液、品红溶液 b.稀H2SO4酸化的KMnO4溶液 c.碘水、淀粉溶液
您最近一年使用:0次



