氯气是一种重要的化工原料。
(1)氯气和石灰乳反应可以制得漂白粉,写出反应的化学方程式___________ ,漂白粉暴露在空气中容易失效,漂白粉失效过程的化学反应方程式为___________ 。
(2)氯气与烧碱溶液反应能够制取消毒液
①写出反应的化学方程式___________ 。
②“84消毒液”能有效杀灭甲型H1N1等病毒,某同学购买了一瓶“84消毒液”,并查阅相关资料和消毒液包装说明得到如下信息:
“84消毒液”:含质量分数为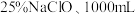 、密度
、密度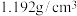 ,稀释100倍(体积比)后使用。
,稀释100倍(体积比)后使用。
请根据以上信息和相关知识回答下列问题:
该“84消毒液”的物质的量浓度为___________  。若一瓶“84消毒液”完全变质,最多能吸收
。若一瓶“84消毒液”完全变质,最多能吸收___________  空气中的
空气中的 (标准状况)。
(标准状况)。
(3)同学参阅该品牌“84消毒液”的配方,欲用 固体配制
固体配制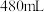 含质量分数为
含质量分数为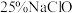 的消毒液,下列说法正确的是___________(填字母)。
的消毒液,下列说法正确的是___________(填字母)。
(4)工业上用氢气在氯气中燃烧的方法制取浓盐酸,现配制一定物质的量浓度的盐酸,下列操作导致所配制的稀盐酸的物质的量浓度偏低的是___________ (填字母)。
A.未恢复到室温就将溶液注入容量瓶并进行定容
B.用量筒量取浓盐酸时俯视凹液面最低处读数
C.容量瓶用蒸馏水洗后未干燥
D.未洗涤烧杯和玻璃棒
E.定容时俯视刻度线
(1)氯气和石灰乳反应可以制得漂白粉,写出反应的化学方程式
(2)氯气与烧碱溶液反应能够制取消毒液
①写出反应的化学方程式
②“84消毒液”能有效杀灭甲型H1N1等病毒,某同学购买了一瓶“84消毒液”,并查阅相关资料和消毒液包装说明得到如下信息:
“84消毒液”:含质量分数为
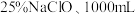 、密度
、密度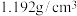 ,稀释100倍(体积比)后使用。
,稀释100倍(体积比)后使用。请根据以上信息和相关知识回答下列问题:
该“84消毒液”的物质的量浓度为
 。若一瓶“84消毒液”完全变质,最多能吸收
。若一瓶“84消毒液”完全变质,最多能吸收 空气中的
空气中的 (标准状况)。
(标准状况)。(3)同学参阅该品牌“84消毒液”的配方,欲用
 固体配制
固体配制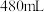 含质量分数为
含质量分数为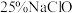 的消毒液,下列说法正确的是___________(填字母)。
的消毒液,下列说法正确的是___________(填字母)。| A.容量瓶在使用前必须要先检漏,检漏时需要倒置一次 |
| B.容量瓶用蒸馏水洗净后,应烘干才能用于溶液配制 |
C.利用购买的商品 来配制可能导致结果偏低 来配制可能导致结果偏低 |
D.需要称量的 固体质量为 固体质量为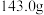 |
A.未恢复到室温就将溶液注入容量瓶并进行定容
B.用量筒量取浓盐酸时俯视凹液面最低处读数
C.容量瓶用蒸馏水洗后未干燥
D.未洗涤烧杯和玻璃棒
E.定容时俯视刻度线
23-24高一上·山东烟台·阶段练习 查看更多[2]
更新时间:2023-10-09 14:22:21
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】(I)工业上常用电解饱和食盐水的方法制备氯气,其装置如下图所示:

(1)写出电解饱和食盐水的化学方程式并在化学方程式上标出电子转移的方向和数目:_____ 。
(2)电解时,将Y极(阳极)生成的物质通入盛有NaI溶液的试管中,再加入四氯化碳充分振荡,最后观察到的现象是____________ 。
A.溶液分层,上层无色,下层橙红色
B.溶液分层,上层橙红色,下层无层
C.溶液分层,上层无色,下层紫红色
D.溶液分层,上层紫红色,下层无层
(3)用氯气制备漂白粉,请写出漂白粉长期露置在空气中失效的反应的化学方程式_______ ;____________________________ 。
(II)某同学对实验室制取氯气的装置进行改进,设计了制取无水氯化铁的实验装置图(如下),将浓盐酸滴加到盛有二氧化锰粉末的圆底烧瓶中。请回答下列问题:
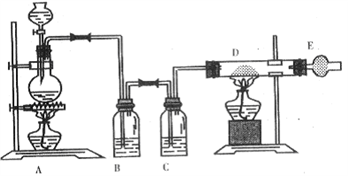
(4)烧瓶中发生反应的化学方程式____________________ ;
(5)产生的气体通过B、C装置,可以得到干燥纯净的氯气,B瓶中的试剂是_____________ ;
(6)如果将过量二氧化锰与20 mL 12 mol·L-1的盐酸混合加热,充分反应后生成的氯气明显少于0.06 mol。其主要原因为______________________________________ 。
(7)玻璃管D中反应现象是_________________ ;写出反应方程式______________________ 。
(8)干燥管E中盛有碱石灰(CaO+NaOH),其作用是__________________ 。

(1)写出电解饱和食盐水的化学方程式并在化学方程式上标出电子转移的方向和数目:
(2)电解时,将Y极(阳极)生成的物质通入盛有NaI溶液的试管中,再加入四氯化碳充分振荡,最后观察到的现象是
A.溶液分层,上层无色,下层橙红色
B.溶液分层,上层橙红色,下层无层
C.溶液分层,上层无色,下层紫红色
D.溶液分层,上层紫红色,下层无层
(3)用氯气制备漂白粉,请写出漂白粉长期露置在空气中失效的反应的化学方程式
(II)某同学对实验室制取氯气的装置进行改进,设计了制取无水氯化铁的实验装置图(如下),将浓盐酸滴加到盛有二氧化锰粉末的圆底烧瓶中。请回答下列问题:

(4)烧瓶中发生反应的化学方程式
(5)产生的气体通过B、C装置,可以得到干燥纯净的氯气,B瓶中的试剂是
(6)如果将过量二氧化锰与20 mL 12 mol·L-1的盐酸混合加热,充分反应后生成的氯气明显少于0.06 mol。其主要原因为
(7)玻璃管D中反应现象是
(8)干燥管E中盛有碱石灰(CaO+NaOH),其作用是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】Cl2、SO2、NOx都是化工生产中的重要气体,均可用氨水或NaOH溶液处理,防止污染空气。请回答下列问题:
(1)化工厂可用浓氨水来检验Cl2是否泄漏(已知3Cl2+8NH3→6NH4Cl+N2),当有少量Cl2泄漏时,可以观察到的现象是_______ ,若反应中有0.08mol的氨气被氧化,则有_______ mol电子发生转移。
(2)①若用热烧碱溶液吸收Cl2气反应后的混合溶液中,含NaCl、NaClO和NaClO3物质的量比值为n:1:1,则n=_______ 。
②SO2是形成酸雨的主要原因,取某化工区空气样本用蒸馏水处理,检测所得溶液,所含离子及其浓度如下:
根据表中数据计算,检测的溶液pH=_______ 。
(3)NO2是燃油汽车尾气中的主要污染物之一、
①在催化剂和加热条件下,NO2与NH3可反应生成无害物质,请写出反应的化学方程式:_______ 。
②实验室可用烧碱溶液吸收NO2和NO,(已知2NO2+2NaOH→NaNO2+NaNO3+H2O,NO2+NO+2NaOH→2NaNO2+H2O),当消耗100mL0.5mol⋅L-1的烧碱溶液时,共吸收混合气体_______ L(标准状态)。
(1)化工厂可用浓氨水来检验Cl2是否泄漏(已知3Cl2+8NH3→6NH4Cl+N2),当有少量Cl2泄漏时,可以观察到的现象是
(2)①若用热烧碱溶液吸收Cl2气反应后的混合溶液中,含NaCl、NaClO和NaClO3物质的量比值为n:1:1,则n=
②SO2是形成酸雨的主要原因,取某化工区空气样本用蒸馏水处理,检测所得溶液,所含离子及其浓度如下:
| 离子 | Na+ | K+ | NH | H+ | SO | NO | Cl- |
| 浓度/(mol·L-1) | 6×10-6 | 4×10-6 | 2×10-5 | a | 4×10-5 | 2×10-5 | 3×10-5 |
(3)NO2是燃油汽车尾气中的主要污染物之一、
①在催化剂和加热条件下,NO2与NH3可反应生成无害物质,请写出反应的化学方程式:
②实验室可用烧碱溶液吸收NO2和NO,(已知2NO2+2NaOH→NaNO2+NaNO3+H2O,NO2+NO+2NaOH→2NaNO2+H2O),当消耗100mL0.5mol⋅L-1的烧碱溶液时,共吸收混合气体
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】请用学过的知识分析其中的化学原理并写出化学方程式,属于离子反应的请写出离子方程式。
(1)将氯气通入熟石灰即可制的漂白粉【漂白粉的有效成分是次氯酸钙Ca(ClO)2,商品漂白粉往往含有Ca(OH)2等杂质】_________________________________ 。
(2)漂白粉之所以具有漂白作用是由于Ca(ClO)2在水溶液中发生水解反应生成具有强氧化性的物质__________________________ 。
(3)Ca(OH)2杂质的存在使溶液的碱性增强,因此漂白作用进行缓慢。要在短时间受到漂白效果,必须除去Ca(OH)2,所以工业上使用漂白粉是常加入少量弱酸如醋酸等,或加入少量的稀盐酸____________________ 、__________________ 。
(4)家庭使用漂白粉不必加酸,因为水中的CO2也起到了弱酸的作用_______________ 。
(5)不要将漂白粉与洁厕剂等强酸性物质混合使用,因为在强酸性条件下二者可以发生氧化还原反应生成一种有毒气体:_____________
(1)将氯气通入熟石灰即可制的漂白粉【漂白粉的有效成分是次氯酸钙Ca(ClO)2,商品漂白粉往往含有Ca(OH)2等杂质】
(2)漂白粉之所以具有漂白作用是由于Ca(ClO)2在水溶液中发生水解反应生成具有强氧化性的物质
(3)Ca(OH)2杂质的存在使溶液的碱性增强,因此漂白作用进行缓慢。要在短时间受到漂白效果,必须除去Ca(OH)2,所以工业上使用漂白粉是常加入少量弱酸如醋酸等,或加入少量的稀盐酸
(4)家庭使用漂白粉不必加酸,因为水中的CO2也起到了弱酸的作用
(5)不要将漂白粉与洁厕剂等强酸性物质混合使用,因为在强酸性条件下二者可以发生氧化还原反应生成一种有毒气体:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】实验室常用二氧化锰和浓盐酸共热的方法制取氯气。根据要求回答下列问题。
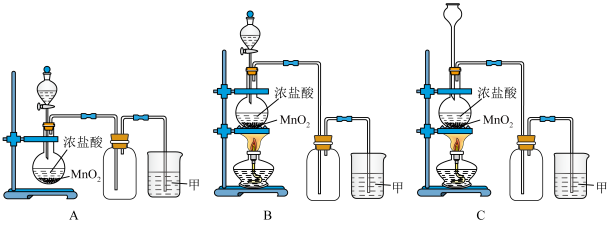
(1)A、B、C三套装置中,应选用的装置是___________ (选填“A”、“B”、“C”)。
(2)写出制取氯气的化学方程式___________ 。
(3)为了防止氯气污染环境,图中溶液甲中发生的化学反应方程式___________ 。
(4)由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,在空气中漂白粉长期存放会变质而失效的原理是___________ (用化学方程式说明)
(5)实验室也可用 固体和浓盐酸反应制取氯气,反应方程式:
固体和浓盐酸反应制取氯气,反应方程式: 。请用双线桥标出电子转移的方向和数目:
。请用双线桥标出电子转移的方向和数目:___________ 。若反应中有5mol电子转移,被氧化HCl的的物质的量为___________ 。

(1)A、B、C三套装置中,应选用的装置是
(2)写出制取氯气的化学方程式
(3)为了防止氯气污染环境,图中溶液甲中发生的化学反应方程式
(4)由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,在空气中漂白粉长期存放会变质而失效的原理是
(5)实验室也可用
 固体和浓盐酸反应制取氯气,反应方程式:
固体和浓盐酸反应制取氯气,反应方程式: 。请用双线桥标出电子转移的方向和数目:
。请用双线桥标出电子转移的方向和数目:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】用化学语言解释现象。
(1)写出实验室制取氯气的化学原理:___________ ;久置氯水酸性变强的原因:___________ ;漂粉精久置于空气中失效的原理:___________ 。
(2)配平化学方程式,并标出电子转移的方向和数目:
KMnO4+HCl=KCl+MnCl2+Cl2↑+H2O___________ 。
KClO3+HCl KCl+Cl2↑+H2O
KCl+Cl2↑+H2O___________ 。
(3)比较碳酸氢钠和碳酸在水溶液中的第一步电离:___________ ;___________ 。
(1)写出实验室制取氯气的化学原理:
(2)配平化学方程式,并标出电子转移的方向和数目:
KMnO4+HCl=KCl+MnCl2+Cl2↑+H2O
KClO3+HCl
 KCl+Cl2↑+H2O
KCl+Cl2↑+H2O(3)比较碳酸氢钠和碳酸在水溶液中的第一步电离:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室需要配制1.00mol/L的氢氧化钠溶液480mL,完成下列各题。
(1)配制步骤如下:
①应选择_______ mL容量瓶。容量瓶在使用前需要_______ 。
②用托盘天平称取_______ gNaOH固体。
③将称好的氢氧化钠固体加水溶解,待_______ 后将溶液转移至容量瓶中,转移时需用玻璃棒_______ 。
④用少量蒸馏水冲洗烧杯和玻璃棒2~3次,将洗液移入容量瓶中。
⑤向容量瓶中加水至距刻度1~2cm处,改用胶头滴管小心地加水至凹液面与刻度线平齐。
(2)分析下列操作可能会对氯化钠溶液浓度造成的影响(填“偏高”、“偏低”或“无影响”)。
①摇匀后发现液面低于刻度线再加水_______ 。
②容量瓶内有少量水_______ 。
③未洗涤或洗涤液未注入容量瓶_______ 。
④定容时俯视刻度线_______ 。
⑤溶液未经冷却,立即转移至容量瓶进行定容_______ 。
(1)配制步骤如下:
①应选择
②用托盘天平称取
③将称好的氢氧化钠固体加水溶解,待
④用少量蒸馏水冲洗烧杯和玻璃棒2~3次,将洗液移入容量瓶中。
⑤向容量瓶中加水至距刻度1~2cm处,改用胶头滴管小心地加水至凹液面与刻度线平齐。
(2)分析下列操作可能会对氯化钠溶液浓度造成的影响(填“偏高”、“偏低”或“无影响”)。
①摇匀后发现液面低于刻度线再加水
②容量瓶内有少量水
③未洗涤或洗涤液未注入容量瓶
④定容时俯视刻度线
⑤溶液未经冷却,立即转移至容量瓶进行定容
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知浓硫酸密度为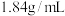 ,质量分数为98%,配制230mL1.0mol/L的稀硫酸需用量筒量取该浓硫酸
,质量分数为98%,配制230mL1.0mol/L的稀硫酸需用量筒量取该浓硫酸___________ mL。
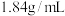 ,质量分数为98%,配制230mL1.0mol/L的稀硫酸需用量筒量取该浓硫酸
,质量分数为98%,配制230mL1.0mol/L的稀硫酸需用量筒量取该浓硫酸
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】“84消毒液”是一种以NaClO为主的高效消毒剂,在今年的新冠肺炎防治中被广泛用于宾馆、旅游、医院、家庭等的卫生消毒。某“84消毒液”瓶体部分标签如图1所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:

(1)此“84消毒液”的物质的量浓度约为_________ mol/L。(计算结果保留一位小数)
(2)该同学参阅读该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为24%的消毒液。
①如图2所示的仪器中配制溶液需要使用的是_________ (填仪器序号),还缺少的玻璃仪器是_________ 。
②下列操作中,容量瓶不具备的功能是_________ (填仪器序号)
a.配制一定体积准确浓度的标准溶液
b.贮存溶液
c.测量容量瓶规格以下的任意体积的溶液
d.准确稀释某一浓度的溶液
e.用来加热溶解固体溶质
③请计算该同学配制此溶液需用托盘天平称取称量NaClO固体的质量为_________ g。
(3)若实验遇下列情况,导致所配溶液的物质的量浓度偏高是_________ (填序号)。
A.定容时俯视刻度线B.转移前,容量瓶内有蒸馏水
C.未冷至室温就转移定容D.定容时水多用胶头滴管吸出

(1)此“84消毒液”的物质的量浓度约为
(2)该同学参阅读该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为24%的消毒液。
①如图2所示的仪器中配制溶液需要使用的是
②下列操作中,容量瓶不具备的功能是
a.配制一定体积准确浓度的标准溶液
b.贮存溶液
c.测量容量瓶规格以下的任意体积的溶液
d.准确稀释某一浓度的溶液
e.用来加热溶解固体溶质
③请计算该同学配制此溶液需用托盘天平称取称量NaClO固体的质量为
(3)若实验遇下列情况,导致所配溶液的物质的量浓度偏高是
A.定容时俯视刻度线B.转移前,容量瓶内有蒸馏水
C.未冷至室温就转移定容D.定容时水多用胶头滴管吸出
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】用Na2CO3·10H2O晶体,配置0.2mol/L的Na2CO3溶液480ml
(1)应称取Na2CO3·10H2O晶体的质量为____ 。
(2)根据下列操作对所配溶液的浓度产生的影响,完成下列要求:
①Na2CO3·10H2O晶体失去了部分结晶水;②用“左物右码”的称量方法称量晶体(使用游码);
③碳酸钠晶体不纯,其中混有氯化钠;④称量碳酸钠晶体时所用砝码生锈;
⑤容量瓶未经干燥使用;
其中引起所配溶液浓度偏高的有___ (填序号,下同),偏低的有____ ,无影响的有_____ 。
(3)为完成实验所必须要的玻璃仪器有:____ 、____ 、____ 、____ 。
(1)应称取Na2CO3·10H2O晶体的质量为
(2)根据下列操作对所配溶液的浓度产生的影响,完成下列要求:
①Na2CO3·10H2O晶体失去了部分结晶水;②用“左物右码”的称量方法称量晶体(使用游码);
③碳酸钠晶体不纯,其中混有氯化钠;④称量碳酸钠晶体时所用砝码生锈;
⑤容量瓶未经干燥使用;
其中引起所配溶液浓度偏高的有
(3)为完成实验所必须要的玻璃仪器有:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】医疗机构常用质量分数为7.45% 的次氯酸钠消毒液(密度为1.00 g·cm−3)进行消毒,回答下列问题:
(1)该消毒液的物质的量浓度为_______ mol·L−1(保留到小数点后2位)。
(2)次氯酸钠消毒液使用时需要稀释。某化学实验小组用上述消毒液配制95mL 0.7mol·L−1的溶液。
①需用量筒量取该次氯酸钠消毒液_______ mL;量取时若仰视,所配溶液的浓度将_______ (填“偏高”、“偏低”或“无影响”)。
②定容时加蒸馏水,若不慎超过刻度线,应采取的处理方法是_______ 。
(3)资料显示,次氯酸钠消毒液不能与洁厕灵(含盐酸)混合使用,对此某小组开展如下研究。

能观察到两表面皿之间出现黄绿色气体,写出该反应的离子方程式_______ ;蘸有NaOH溶液的脱脂棉吸收黄绿色气体的离子方程式是_______ 。
(1)该消毒液的物质的量浓度为
(2)次氯酸钠消毒液使用时需要稀释。某化学实验小组用上述消毒液配制95mL 0.7mol·L−1的溶液。
①需用量筒量取该次氯酸钠消毒液
②定容时加蒸馏水,若不慎超过刻度线,应采取的处理方法是
(3)资料显示,次氯酸钠消毒液不能与洁厕灵(含盐酸)混合使用,对此某小组开展如下研究。

能观察到两表面皿之间出现黄绿色气体,写出该反应的离子方程式
您最近一年使用:0次



