Cl2、SO2、NOx都是化工生产中的重要气体,均可用氨水或NaOH溶液处理,防止污染空气。请回答下列问题:
(1)化工厂可用浓氨水来检验Cl2是否泄漏(已知3Cl2+8NH3→6NH4Cl+N2),当有少量Cl2泄漏时,可以观察到的现象是_______ ,若反应中有0.08mol的氨气被氧化,则有_______ mol电子发生转移。
(2)①若用热烧碱溶液吸收Cl2气反应后的混合溶液中,含NaCl、NaClO和NaClO3物质的量比值为n:1:1,则n=_______ 。
②SO2是形成酸雨的主要原因,取某化工区空气样本用蒸馏水处理,检测所得溶液,所含离子及其浓度如下:
根据表中数据计算,检测的溶液pH=_______ 。
(3)NO2是燃油汽车尾气中的主要污染物之一、
①在催化剂和加热条件下,NO2与NH3可反应生成无害物质,请写出反应的化学方程式:_______ 。
②实验室可用烧碱溶液吸收NO2和NO,(已知2NO2+2NaOH→NaNO2+NaNO3+H2O,NO2+NO+2NaOH→2NaNO2+H2O),当消耗100mL0.5mol⋅L-1的烧碱溶液时,共吸收混合气体_______ L(标准状态)。
(1)化工厂可用浓氨水来检验Cl2是否泄漏(已知3Cl2+8NH3→6NH4Cl+N2),当有少量Cl2泄漏时,可以观察到的现象是
(2)①若用热烧碱溶液吸收Cl2气反应后的混合溶液中,含NaCl、NaClO和NaClO3物质的量比值为n:1:1,则n=
②SO2是形成酸雨的主要原因,取某化工区空气样本用蒸馏水处理,检测所得溶液,所含离子及其浓度如下:
| 离子 | Na+ | K+ | NH | H+ | SO | NO | Cl- |
| 浓度/(mol·L-1) | 6×10-6 | 4×10-6 | 2×10-5 | a | 4×10-5 | 2×10-5 | 3×10-5 |
(3)NO2是燃油汽车尾气中的主要污染物之一、
①在催化剂和加热条件下,NO2与NH3可反应生成无害物质,请写出反应的化学方程式:
②实验室可用烧碱溶液吸收NO2和NO,(已知2NO2+2NaOH→NaNO2+NaNO3+H2O,NO2+NO+2NaOH→2NaNO2+H2O),当消耗100mL0.5mol⋅L-1的烧碱溶液时,共吸收混合气体
2022高三·全国·专题练习 查看更多[1]
(已下线)第四章 非金属及其化合物(测)-2023年高考化学一轮复习讲练测(全国通用)
更新时间:2022-08-26 13:25:37
|
相似题推荐
【推荐1】化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可以减少该有害物质向环境排放。例如:

(1)完成方程式,回答相关问题。用单线桥 标出反应①的电子转移的方向和数目。
反应①为: __Na2Cr2O7 + __HCl = __NaCl + __CrCl3 + __Cl2↑+ H2O( )
反应⑥为:__ClO +__CrO
+__CrO +__
+__  =___Cl-+__CrO
=___Cl-+__CrO +__H2O
+__H2O( )
反应⑥中还原剂为___________ ,还原产物为 ____________ 。
(2)在上述转化中,需用氧化剂的步骤是____ (填编号)。

(1)完成方程式,回答相关问题。用
反应①为: __Na2Cr2O7 + __HCl = __NaCl + __CrCl3 + __Cl2↑+ H2O
反应⑥为:__ClO
 +__CrO
+__CrO +__
+__  =___Cl-+__CrO
=___Cl-+__CrO +__H2O
+__H2O反应⑥中还原剂为
(2)在上述转化中,需用氧化剂的步骤是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。回答下列问题:
(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加MnO2和H2SO4,即可得到I2, 该反应的离子方程式为__________________ 。
(2)氢氧化铁与氢碘酸反应时可生成棕色物质,该反应的离子方程式为_______________ 。
(3)从海带中提取碘的过程中,下列说法正确的是______ 。

(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加MnO2和H2SO4,即可得到I2, 该反应的离子方程式为
(2)氢氧化铁与氢碘酸反应时可生成棕色物质,该反应的离子方程式为
(3)从海带中提取碘的过程中,下列说法正确的是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】完成下列问题。
(1)2022年6月5日,长征二号F运载火箭将神舟十四号载人飞船成功发射。该运载火箭是以偏二甲肼(C2H8N2)和四氧化二氮(N2O4)作推动剂,发生反应的化学方程式为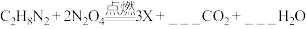 。请在横线上填写出该反应的化学计量数为
。请在横线上填写出该反应的化学计量数为___________ ,完成化学方程式的配平,X单质的化学式为___________ 。
(2)等质量的 和
和 ,分子个数比为
,分子个数比为___________ ,同温同压下,等体积的 和
和 密度比为
密度比为___________ 。
(3)在标准状况下, 恰好与
恰好与 溶液反应生成
溶液反应生成 ,则此
,则此 溶液的物质的量浓度为
溶液的物质的量浓度为___________ 。
(4)氢气是一种清洁能源,甲烷制氢的化学方程式为 。在标准状况下,
。在标准状况下, 与一定量的
与一定量的 中恰好完全反应,反应后测得生成物的体积是
中恰好完全反应,反应后测得生成物的体积是 ,则生成
,则生成
___________  ,消耗的
,消耗的 的体积是
的体积是___________ 。
(1)2022年6月5日,长征二号F运载火箭将神舟十四号载人飞船成功发射。该运载火箭是以偏二甲肼(C2H8N2)和四氧化二氮(N2O4)作推动剂,发生反应的化学方程式为
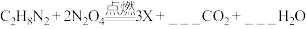 。请在横线上填写出该反应的化学计量数为
。请在横线上填写出该反应的化学计量数为(2)等质量的
 和
和 ,分子个数比为
,分子个数比为 和
和 密度比为
密度比为(3)在标准状况下,
 恰好与
恰好与 溶液反应生成
溶液反应生成 ,则此
,则此 溶液的物质的量浓度为
溶液的物质的量浓度为(4)氢气是一种清洁能源,甲烷制氢的化学方程式为
 。在标准状况下,
。在标准状况下, 与一定量的
与一定量的 中恰好完全反应,反应后测得生成物的体积是
中恰好完全反应,反应后测得生成物的体积是 ,则生成
,则生成
 ,消耗的
,消耗的 的体积是
的体积是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】已知:还原性I->Fe2+>Br-。向含有1molFeI2和2molFeBr2的溶液中通入一定量的Cl2。
(1)若通入2molCl2,此时被氧化的离子是____ ,被氧化的离子的物质的量分别是_____ 。
(2)若通入3molCl2,则被氧化的离子是____ ,对应氧化产物的物质的量分别是_____ 。
(1)若通入2molCl2,此时被氧化的离子是
(2)若通入3molCl2,则被氧化的离子是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知几种离子的还原能力强弱顺序为I->Fe2+>Br-,现有200 mL混合溶液中含FeI2、FeBr2各0.10 mol,向其中逐滴滴入氯水(假定Cl2分子只与溶质离子反应,不考虑其他反应)
(1)若氯水中有0.15 mol Cl2被还原,则所得溶液中含有的阴离子主要是________ ,剩余Fe2+的物质的量为________ 。
(2)若原溶液中Br-有一半被氧化,共消耗Cl2的物质的量为________ ,若最终所得溶液为400 mL,其中主要阳离子及其物质的量浓度为________ 。
(3)通过对上述反应的分析,试判断Cl2,I2,Fe3+,Br2四种氧化剂的氧化能力由强到弱的顺序是_________________________________________________ 。
(4)上述反应若原溶液中溶质离子全部被氧化后,再滴入足量氯水,则I2全部被Cl2氧化成HIO3(强酸)。试写出此反应的离子方程式:_________________ ;上述所有反应共消耗Cl2________ mol。
(1)若氯水中有0.15 mol Cl2被还原,则所得溶液中含有的阴离子主要是
(2)若原溶液中Br-有一半被氧化,共消耗Cl2的物质的量为
(3)通过对上述反应的分析,试判断Cl2,I2,Fe3+,Br2四种氧化剂的氧化能力由强到弱的顺序是
(4)上述反应若原溶液中溶质离子全部被氧化后,再滴入足量氯水,则I2全部被Cl2氧化成HIO3(强酸)。试写出此反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】如图是某研究性学习小组设计制取氯气并以氯气为原料进行特定反应的装置.

(1)写出A装置中发生反应的离子方程式__________ ;要将C装置接入B和D之间,正确的接法是:a→ _____ → _____ →d;
(2)实验开始先点燃A处的酒精灯,打开旋塞K,让Cl 2 充满整个装置,再点燃D处的酒精灯,Cl 2 通过C装置后进入D,D装置内盛有碳粉,发生氧化还原反应,生成CO 2 和HCl(g),发生反应的化学方程式为_________ .
(3)D处反应完毕后,关闭旋塞K,移去两个酒精灯,由于余热的作用,A处仍有少量Cl 2 产生,此时B中的现象是______________________ ,B的作用是________________________ .
(4)用量筒量取20mL E中溶液,倒入已检查完气密性良好的分液漏斗中,然后再注入10mL CCl4 ,盖好玻璃塞,振荡,静置于铁架台上(如图),等分层后取上层液和下层液,呈黄绿色的是___________________ (填“上层液”或“下层液”),能使有色布条褪色的是_________ (填“上层液”或“下层液”).
(5)在A、B、C、D、E装置中有一处需要改进,说明需要改进的理由并在方框中画出改进后的装置图_______________________ .


(1)写出A装置中发生反应的离子方程式
(2)实验开始先点燃A处的酒精灯,打开旋塞K,让Cl 2 充满整个装置,再点燃D处的酒精灯,Cl 2 通过C装置后进入D,D装置内盛有碳粉,发生氧化还原反应,生成CO 2 和HCl(g),发生反应的化学方程式为
(3)D处反应完毕后,关闭旋塞K,移去两个酒精灯,由于余热的作用,A处仍有少量Cl 2 产生,此时B中的现象是
(4)用量筒量取20mL E中溶液,倒入已检查完气密性良好的分液漏斗中,然后再注入10mL CCl4 ,盖好玻璃塞,振荡,静置于铁架台上(如图),等分层后取上层液和下层液,呈黄绿色的是
(5)在A、B、C、D、E装置中有一处需要改进,说明需要改进的理由并在方框中画出改进后的装置图

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】按要求书写方程式
(1)NaHSO4在熔融状态的电离方程式___________
(2)碳酸钙溶解在醋酸中的离子反应方程式___________
(3)将“ ”改写为对应的化学方程式
”改写为对应的化学方程式___________
(4)除去Na2CO3粉末中混有少量NaHCO3的化学方程式___________
(5)氯气与烧碱溶液反应的化学方程式为___________
(6)“84”消毒液与除垢剂(有效成分是盐酸)混合使用会产生黄绿色、有刺激性气味的气体,该反应的离子方程式是___________
(7)衣服上不小心沾到了蓝色墨水,可以先涂上酸性高锰酸钾溶液,即可除去蓝墨水中的鞣酸亚铁,再用乙二酸的稀溶液擦洗,可以迅速除去过量的 ,配平该反应的离子方程式:
,配平该反应的离子方程式:___________
_______MnO +_______H2C2O4+_______H+=_______CO2↑+_______Mn2++______H2O
+_______H2C2O4+_______H+=_______CO2↑+_______Mn2++______H2O
(1)NaHSO4在熔融状态的电离方程式
(2)碳酸钙溶解在醋酸中的离子反应方程式
(3)将“
 ”改写为对应的化学方程式
”改写为对应的化学方程式(4)除去Na2CO3粉末中混有少量NaHCO3的化学方程式
(5)氯气与烧碱溶液反应的化学方程式为
(6)“84”消毒液与除垢剂(有效成分是盐酸)混合使用会产生黄绿色、有刺激性气味的气体,该反应的离子方程式是
(7)衣服上不小心沾到了蓝色墨水,可以先涂上酸性高锰酸钾溶液,即可除去蓝墨水中的鞣酸亚铁,再用乙二酸的稀溶液擦洗,可以迅速除去过量的
 ,配平该反应的离子方程式:
,配平该反应的离子方程式:_______MnO
 +_______H2C2O4+_______H+=_______CO2↑+_______Mn2++______H2O
+_______H2C2O4+_______H+=_______CO2↑+_______Mn2++______H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】将 通入NaOH溶液制备84消毒液(有效成分为NaClO),利用氯及其化合物的“价类”二维图表示其中涉及的各物质之间的转化关系 。回答下列问题:
通入NaOH溶液制备84消毒液(有效成分为NaClO),利用氯及其化合物的“价类”二维图表示其中涉及的各物质之间的转化关系 。回答下列问题:
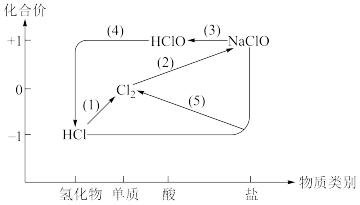
(1)实验室用二氧化锰和浓盐酸反成制备氯气,在制取Cl2的反应中,浓盐酸发生了___________ 反应
(2)制备84消毒液的化学方程式为___________ 。
(3)84消毒液中加入少量醋酸(CH3COOH)可增强效果,该反应的化学方程式为___________ 。
(4)次氯酸不稳定,光照条件下易分解。该反应的化学方程式为___________ 。
(5)84消毒液不能与洁厕剂(含盐酸)一起混合使用的原因为___________ (用离子反应方程式表示)。
 通入NaOH溶液制备84消毒液(有效成分为NaClO),利用氯及其化合物的“价类”二维图表示其中涉及的各物质之间的转化关系 。回答下列问题:
通入NaOH溶液制备84消毒液(有效成分为NaClO),利用氯及其化合物的“价类”二维图表示其中涉及的各物质之间的转化关系 。回答下列问题:
(1)实验室用二氧化锰和浓盐酸反成制备氯气,在制取Cl2的反应中,浓盐酸发生了
(2)制备84消毒液的化学方程式为
(3)84消毒液中加入少量醋酸(CH3COOH)可增强效果,该反应的化学方程式为
(4)次氯酸不稳定,光照条件下易分解。该反应的化学方程式为
(5)84消毒液不能与洁厕剂(含盐酸)一起混合使用的原因为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】NaClO广泛用作水处理剂及漂白剂。
已知:25℃时NaClO溶液中HClO、ClO-的物质的量分数随pH的分布如下图所示。
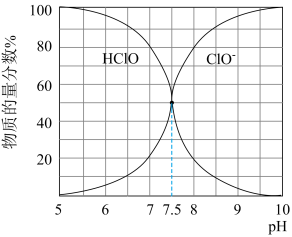
(1)工业上将Cl2通入 的NaOH溶液中制备NaClO。
的NaOH溶液中制备NaClO。
①NaClO属于______ (填“酸”、“盐”、“氧化物”),制备NaClO的离子方程式为_______ 。
②取少量pH=9时的溶液加入稀硫酸,发生离子方程式除了 外,还有
外,还有______ 。
③若反应温度过高会生成副产物NaClO3,写出该反应的离子方程式并用双线桥标明电子转移的方向和数目_______ ,该反应中氧化剂与还原剂的物质的量之比是_____ 。
(2)含NaClO消毒液与洁厕剂(含有盐酸)会产生有毒气体,写出该反应的离子方程式______ 。
已知:25℃时NaClO溶液中HClO、ClO-的物质的量分数随pH的分布如下图所示。

(1)工业上将Cl2通入
 的NaOH溶液中制备NaClO。
的NaOH溶液中制备NaClO。①NaClO属于
②取少量pH=9时的溶液加入稀硫酸,发生离子方程式除了
 外,还有
外,还有③若反应温度过高会生成副产物NaClO3,写出该反应的离子方程式并用双线桥标明电子转移的方向和数目
(2)含NaClO消毒液与洁厕剂(含有盐酸)会产生有毒气体,写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】请按要求填空。
(1)NO2是造成酸雨的污染物之一,实验室可将NO2与O2同时通入水中,使NO2完全被吸收,写出NO2完全被吸收的化学方程式_______ 。
(2)实验室用固体氢氧化钙和固体氯化铵共热制取氨气的化学方程式为:_______ 。
(1)NO2是造成酸雨的污染物之一,实验室可将NO2与O2同时通入水中,使NO2完全被吸收,写出NO2完全被吸收的化学方程式
(2)实验室用固体氢氧化钙和固体氯化铵共热制取氨气的化学方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氮、硫及其化合物是重要的化工原料,研究其性质、用途和转化具有重要意义。
(1)氮的化合物常用作制冷剂的是__________ (填名称)。
(2)燃煤排放的尾气中含有二氧化硫、氮的氧化物(主要为NO)等污染物,工业上采用.NaClO碱性溶液作为吸收剂可同时对烟气进行脱硫、脱硝。脱硫的离子方程式为__________ ,实验证明相对于SO2,NO更难脱除,其原因可能是__________ 。
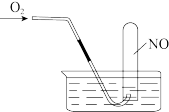
(3)将3.84 gCu和稀硝酸充分反应,生成的气体体积为__________ L(在标准状况下),用排__________ (填“水”或“空气”)法收集该气体,将收集到的气体的试管倒立于水槽中缓缓通入__________ LO2(标准状况)使NO恰好完全反应,写出观察到的现象:__________ 。
(1)氮的化合物常用作制冷剂的是
(2)燃煤排放的尾气中含有二氧化硫、氮的氧化物(主要为NO)等污染物,工业上采用.NaClO碱性溶液作为吸收剂可同时对烟气进行脱硫、脱硝。脱硫的离子方程式为
(3)将3.84 gCu和稀硝酸充分反应,生成的气体体积为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】工业上常用Na2CO3溶液吸收法处理NOx。已知:(NO不能与Na2CO3溶液反应。
NO+NO2+Na2CO3=2NaNO2+CO2 (I)
2NO2+Na2CO3=NaNO2+NaNO3+CO2 (II)
①当NOx被Na2CO3溶液完全吸收时x,x的值不可能是_______ (填字母)。
A.1.3 B.1.6 C.1.8
②将1molNOx通入Na2CO3溶液中,被完全吸收时,溶液中生成的 、
、 两种离子的物质的量随x变化关系如图所示:
两种离子的物质的量随x变化关系如图所示:

图中线段a表示__ 随x值变化的关系;若用溶质质量分数为21.2%的Na2CO3溶液吸收,则需要Na2CO3溶液至少_______ g。
③用足量的Na2CO3溶液完全吸收NOx,每产生22.4L(标准状况)CO2(全部逸出)时,吸收液质量就增加44g,则NOx中的x值为_______ 。
NO+NO2+Na2CO3=2NaNO2+CO2 (I)
2NO2+Na2CO3=NaNO2+NaNO3+CO2 (II)
①当NOx被Na2CO3溶液完全吸收时x,x的值不可能是
A.1.3 B.1.6 C.1.8
②将1molNOx通入Na2CO3溶液中,被完全吸收时,溶液中生成的
 、
、 两种离子的物质的量随x变化关系如图所示:
两种离子的物质的量随x变化关系如图所示:
图中线段a表示
③用足量的Na2CO3溶液完全吸收NOx,每产生22.4L(标准状况)CO2(全部逸出)时,吸收液质量就增加44g,则NOx中的x值为
您最近一年使用:0次



