已知:还原性I->Fe2+>Br-。向含有1molFeI2和2molFeBr2的溶液中通入一定量的Cl2。
(1)若通入2molCl2,此时被氧化的离子是____ ,被氧化的离子的物质的量分别是_____ 。
(2)若通入3molCl2,则被氧化的离子是____ ,对应氧化产物的物质的量分别是_____ 。
(1)若通入2molCl2,此时被氧化的离子是
(2)若通入3molCl2,则被氧化的离子是
2022高一·上海·专题练习 查看更多[1]
(已下线)第5章 金属及其化合物(章末复习)-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)
更新时间:2022-02-21 01:31:50
|
相似题推荐
【推荐1】ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。可以通过下列两种途径得到:
方法一:2KClO3+4HCl(浓)═2KCl+2ClO2↑+Cl2↑+2H2O
方法二(酸性条件下): ClO + H2C2O4+
+ H2C2O4+  —— ClO2↑+ CO2↑+
—— ClO2↑+ CO2↑+ 
(1)用双线桥在方法一反应方程式上标出电子转移的方向和数目______ ;请完成方法二在酸性条件下的离子方程式,并配平______ 。
(2)在方法一中浓盐酸显示出来的性质是_______ 性和________ 性
(3)方法一中产生0.1molCl2,则转移的电子的物质的量为_____ mol。
(4)方法二中被还原的元素是_____ (填元素符号)氧化产物是_____ (填化学式);
(5)比较还原性:H2C2O4_____ ClO2(填“>”、“<”或“=”)
方法一:2KClO3+4HCl(浓)═2KCl+2ClO2↑+Cl2↑+2H2O
方法二(酸性条件下): ClO
 + H2C2O4+
+ H2C2O4+  —— ClO2↑+ CO2↑+
—— ClO2↑+ CO2↑+ 
(1)用双线桥在方法一反应方程式上标出电子转移的方向和数目
(2)在方法一中浓盐酸显示出来的性质是
(3)方法一中产生0.1molCl2,则转移的电子的物质的量为
(4)方法二中被还原的元素是
(5)比较还原性:H2C2O4
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】磷化铝(AlP)和磷化氢(PH3)都是粮食储备常用的高效熏蒸杀虫剂。
(1)磷元素在元素周期表中的位置:_______ ,AlP遇水蒸气会发生反应放出PH3气体,PH3中的P原子的杂化方式为_______ 杂化,该反应的另一种产物的化学式为_______ 。
(2) 具有强还原性,能与
具有强还原性,能与 溶液反应,配平该反应的化学方程式:
溶液反应,配平该反应的化学方程式:_______ 。

(3)工业制备 的流程如图所示。
的流程如图所示。

① 次磷酸属于_______ 元酸。
② 白磷和烧碱溶液反应的化学方程式为:_______ 。
③ 若起始时有1 mol P4参加反应,则整个工业流程中共生成_______ mol  (不考虑产物损失)
(不考虑产物损失)
(1)磷元素在元素周期表中的位置:
(2)
 具有强还原性,能与
具有强还原性,能与 溶液反应,配平该反应的化学方程式:
溶液反应,配平该反应的化学方程式:
(3)工业制备
 的流程如图所示。
的流程如图所示。
① 次磷酸属于
② 白磷和烧碱溶液反应的化学方程式为:
③ 若起始时有1 mol P4参加反应,则整个工业流程中共生成
 (不考虑产物损失)
(不考虑产物损失)
您最近一年使用:0次
【推荐3】氧化还原反应在生产、生活中有广泛的用途。
Ⅰ.为防治碘缺乏病,通常在食盐中添加少量的碘酸钾(KIO3),碘酸钾和碘化钾在酸性溶液中能发生下列反应:KIO3+5KI+3H2SO4=3I2+3K2SO4+3H2O。回答下列问题:
(1)该反应中,氧化剂是_______ (填化学式,下同),还原剂是_______ ,氧化产物和还原产物的个数比是_______ 。
Ⅱ.工业废水中含有的重铬酸根离子( )有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4•7H2O)做处理剂,反应的离子方程式6Fe2+ +
)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4•7H2O)做处理剂,反应的离子方程式6Fe2+ + + 14H+ = 6Fe3+ + 2Cr3++ 7H2O
+ 14H+ = 6Fe3+ + 2Cr3++ 7H2O
(2)在该反应中,被氧化的是_______ (填离子符号,下同),还原产物是_______ ,此反应可以推断物质还原性强弱顺序是_______ 。
Ⅲ.高铁酸钠是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为:3ClO- +2Fe3+ + 10OH- = 2 +_______+ 5H2O
+_______+ 5H2O
(3)请完成该化学方程式并配平_______ 。
(4)该反应中生成2个 转移的电子数为
转移的电子数为_______ 。
Ⅰ.为防治碘缺乏病,通常在食盐中添加少量的碘酸钾(KIO3),碘酸钾和碘化钾在酸性溶液中能发生下列反应:KIO3+5KI+3H2SO4=3I2+3K2SO4+3H2O。回答下列问题:
(1)该反应中,氧化剂是
Ⅱ.工业废水中含有的重铬酸根离子(
 )有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4•7H2O)做处理剂,反应的离子方程式6Fe2+ +
)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4•7H2O)做处理剂,反应的离子方程式6Fe2+ + + 14H+ = 6Fe3+ + 2Cr3++ 7H2O
+ 14H+ = 6Fe3+ + 2Cr3++ 7H2O(2)在该反应中,被氧化的是
Ⅲ.高铁酸钠是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为:3ClO- +2Fe3+ + 10OH- = 2
 +_______+ 5H2O
+_______+ 5H2O(3)请完成该化学方程式并配平
(4)该反应中生成2个
 转移的电子数为
转移的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】亚硝酸钠被用作肉制品发色剂、防腐剂等,硝酸钠在肉制品加工中作发色剂。但亚硝酸钠是食品添加剂中急性毒性较强的物质之一,是一种剧毒药,摄取少量亚硝酸盐进入血液后,可使正常的血红蛋白变成正铁血红蛋白而失去携带氧的功能,导致组织缺氧。硝酸钠的毒性作用主要是由于它在食物中、在水中或在胃肠道内被还原成亚硝酸盐所致。亚硝酸钠生产方法是由硝酸生产过程中的氮氧化物气体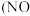 、
、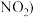 用氢氧化钠或碳酸钠溶液吸收制得。硝酸钠的生产方法是将硝酸生产中的尾气用碱液吸收后,经硝酸转化,再用碱中和、蒸发、结晶、分离制得。
用氢氧化钠或碳酸钠溶液吸收制得。硝酸钠的生产方法是将硝酸生产中的尾气用碱液吸收后,经硝酸转化,再用碱中和、蒸发、结晶、分离制得。
(1)实验室可用加热亚硝酸钠与氯化铵的浓溶液制取氮气,写出该反应的化学方程式:______ ;将亚硝酸钠溶液滴加到含淀粉的酸性KI溶液中,可观察到溶液变蓝色,写出该反应的离子方程式: ______ ;将亚硝酸钠溶液滴加到 酸性溶液中,可观察到溶液的颜色由
酸性溶液中,可观察到溶液的颜色由 ______ 色变为绿色,写出该反应的离子方程式: ______ 。
(2)写出氮氧化物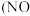 、
、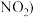 与氢氧化钠溶液反应生成亚硝酸钠溶液的离子方程式:
与氢氧化钠溶液反应生成亚硝酸钠溶液的离子方程式:______ ;若用 溶液吸收
溶液吸收 可生成
可生成 ,
, 和
和 溶液完全反应时转移电子
溶液完全反应时转移电子 ,则反应的离子方程式为
,则反应的离子方程式为 ______ 。
(3)从下列试剂中选用部分试剂鉴别亚硝酸钠、硝酸钠和氯化钠三种无色溶液,它们是______ 。
A.稀盐酸 溶液
溶液  稀硝酸
稀硝酸  氢氧化钠溶液
氢氧化钠溶液
(4)等物质的量浓度的亚硝酸钠、氯化钠、碳酸钠三种溶液中阴离子总浓度由大到小的顺序是______  填溶液中溶质的化学式
填溶液中溶质的化学式 。
。
(5)工业品硝酸钠含少量杂质 、
、 、NaCl、水不溶物
、NaCl、水不溶物 ,某同学欲测定工业品硝酸钠的纯度,进行了如下实验:
,某同学欲测定工业品硝酸钠的纯度,进行了如下实验:
 称取
称取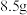 干燥工业品硝酸钠,投入盛适量蒸馏水的烧杯中,充分搅拌后加入10mL
干燥工业品硝酸钠,投入盛适量蒸馏水的烧杯中,充分搅拌后加入10mL  的A溶液
的A溶液 足量
足量 ,充分反应后过滤;
,充分反应后过滤;
 向滤液中加入足量KI溶液和适量稀硫酸,充分反应后将所得溶液配成1000mL溶液;
向滤液中加入足量KI溶液和适量稀硫酸,充分反应后将所得溶液配成1000mL溶液;
 取
取 所配溶液于锥形瓶中,加入少量B物质,再用
所配溶液于锥形瓶中,加入少量B物质,再用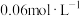 的
的 溶液滴定,用去
溶液滴定,用去 溶液
溶液 。
。
(有关反应为: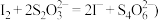
①A溶液中的溶质的化学式是______ ,加入A溶液的作用是 ______ 。
②B物质是______ ,滴定终点时的颜色变化是 ______ 。
③若该同学操作正确,但结果造成测定结果略偏高,其原因可能是 任写一点
任写一点
______ 。
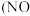 、
、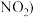 用氢氧化钠或碳酸钠溶液吸收制得。硝酸钠的生产方法是将硝酸生产中的尾气用碱液吸收后,经硝酸转化,再用碱中和、蒸发、结晶、分离制得。
用氢氧化钠或碳酸钠溶液吸收制得。硝酸钠的生产方法是将硝酸生产中的尾气用碱液吸收后,经硝酸转化,再用碱中和、蒸发、结晶、分离制得。(1)实验室可用加热亚硝酸钠与氯化铵的浓溶液制取氮气,写出该反应的化学方程式:
 酸性溶液中,可观察到溶液的颜色由
酸性溶液中,可观察到溶液的颜色由 (2)写出氮氧化物
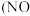 、
、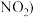 与氢氧化钠溶液反应生成亚硝酸钠溶液的离子方程式:
与氢氧化钠溶液反应生成亚硝酸钠溶液的离子方程式: 溶液吸收
溶液吸收 可生成
可生成 ,
, 和
和 溶液完全反应时转移电子
溶液完全反应时转移电子 ,则反应的离子方程式为
,则反应的离子方程式为 (3)从下列试剂中选用部分试剂鉴别亚硝酸钠、硝酸钠和氯化钠三种无色溶液,它们是
A.稀盐酸
 溶液
溶液  稀硝酸
稀硝酸  氢氧化钠溶液
氢氧化钠溶液(4)等物质的量浓度的亚硝酸钠、氯化钠、碳酸钠三种溶液中阴离子总浓度由大到小的顺序是
 填溶液中溶质的化学式
填溶液中溶质的化学式 。
。(5)工业品硝酸钠含少量杂质
 、
、 、NaCl、水不溶物
、NaCl、水不溶物 ,某同学欲测定工业品硝酸钠的纯度,进行了如下实验:
,某同学欲测定工业品硝酸钠的纯度,进行了如下实验: 称取
称取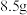 干燥工业品硝酸钠,投入盛适量蒸馏水的烧杯中,充分搅拌后加入10mL
干燥工业品硝酸钠,投入盛适量蒸馏水的烧杯中,充分搅拌后加入10mL  的A溶液
的A溶液 足量
足量 ,充分反应后过滤;
,充分反应后过滤; 向滤液中加入足量KI溶液和适量稀硫酸,充分反应后将所得溶液配成1000mL溶液;
向滤液中加入足量KI溶液和适量稀硫酸,充分反应后将所得溶液配成1000mL溶液; 取
取 所配溶液于锥形瓶中,加入少量B物质,再用
所配溶液于锥形瓶中,加入少量B物质,再用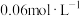 的
的 溶液滴定,用去
溶液滴定,用去 溶液
溶液 。
。(有关反应为:
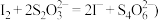
①A溶液中的溶质的化学式是
②B物质是
③若该同学操作正确,但结果造成测定结果略偏高,其原因可能是
 任写一点
任写一点
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】铁是人体含量最多的微量元素,这些铁在人体中不是以金属单质的形式存在,而是以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是_____ 。
A.Fe B.Fe2+ C.Fe3+
(2)工业盐的主要成分是NaNO2,以前有许多起因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有_____ 性。下列不能实现这种转化的物质是_____ (填字母)。
A.Cl2 B.O2 C.FeCl3 D.浓硫酸
(3)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有_____ 性。
(4)在Fe+4HNO3=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了_____ 性和_____ 性,每有1个Fe参加反应,被还原的HNO3为_____ 个,转移电子数_____ 个。用单线桥法标出该反应电子转移_____ 。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是
A.Fe B.Fe2+ C.Fe3+
(2)工业盐的主要成分是NaNO2,以前有许多起因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有
A.Cl2 B.O2 C.FeCl3 D.浓硫酸
(3)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有
(4)在Fe+4HNO3=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了
您最近一年使用:0次
【推荐3】KMnO4在实验室和工业上均有重要应用,其工业制备的部分工艺如下:
Ⅰ.将软锰矿(主要成分MnO2)粉碎后,与KOH固体混合,通入空气充分焙烧,生成暗绿色(K2MnO4)熔融态物质。
Ⅱ.冷却,将固体研细,用KOH溶液浸取,过滤,得暗绿色溶液。
Ⅲ.向暗绿色溶液中通入CO2,溶液变为紫红色,同时生成黑色固体MnO2。
Ⅳ.过滤,将紫红色溶液蒸发浓缩,冷却结晶,过滤,洗涤,干燥,得KMnO4固体。
资料:K2MnO4为暗绿色固体,在强碱性溶液中稳定,在近中性或酸性溶液中易发生歧化反应(Mn的化合价既升高又降低)。
(1)Ⅰ中,粉碎软锰矿的目的是________ 。
(2)Ⅰ中,生成K2MnO4的化学方程式是________ 。
(3)Ⅱ中,浸取时用KOH溶液的原因是________ 。
(4)Ⅲ中,CO2和K2MnO4在溶液中反应的化学方程式是________ 。
Ⅰ.将软锰矿(主要成分MnO2)粉碎后,与KOH固体混合,通入空气充分焙烧,生成暗绿色(K2MnO4)熔融态物质。
Ⅱ.冷却,将固体研细,用KOH溶液浸取,过滤,得暗绿色溶液。
Ⅲ.向暗绿色溶液中通入CO2,溶液变为紫红色,同时生成黑色固体MnO2。
Ⅳ.过滤,将紫红色溶液蒸发浓缩,冷却结晶,过滤,洗涤,干燥,得KMnO4固体。
资料:K2MnO4为暗绿色固体,在强碱性溶液中稳定,在近中性或酸性溶液中易发生歧化反应(Mn的化合价既升高又降低)。
(1)Ⅰ中,粉碎软锰矿的目的是
(2)Ⅰ中,生成K2MnO4的化学方程式是
(3)Ⅱ中,浸取时用KOH溶液的原因是
(4)Ⅲ中,CO2和K2MnO4在溶液中反应的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】常见消毒剂有:①医用酒精;②“84”消毒液(主要成分是NaClO);③漂白粉;④二氧化氯;⑤O3;⑥高铁酸钠。
(1)上述物质中,消毒原理和其他不同的是___________ (填序号,下同)。
(2)上述物质中,其有效成分属于电解质的是__________ 。
(3)HCl气体中混有Cl2,用化学方法检验Cl2的存在____________ 。
(4)高铁酸钠(Na2FeO4)是一种多功能新型水处理剂,它能消毒杀菌,原因为____________ ,它能净水,原因为________ 。
(1)上述物质中,消毒原理和其他不同的是
(2)上述物质中,其有效成分属于电解质的是
(3)HCl气体中混有Cl2,用化学方法检验Cl2的存在
(4)高铁酸钠(Na2FeO4)是一种多功能新型水处理剂,它能消毒杀菌,原因为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某溶液含有Na+还可能含有NH4+、NO3-、CO32-、SO32-、SO42-、Br-、I-一种或几种。为了鉴定其中的阴离子,分别取4份少量溶液进行以下实验:
实验①:测得混合液呈弱碱性
实验②:加入盐酸后,生成无色无味气味。该气体能使澄清石灰水变浑浊
实验③:加CCl4后,滴加少量氯水,振荡后,CCl4层未变色
实验④:加BaCl2溶液产生白色沉淀,该白色沉淀在足量盐酸中不能完全溶解
完成下列填空:
(1)实验①得到的结论:___________ ,理由_________________________________ ;
(2)实验②得到的结论:___________ ,理由_________________________________ ;
(3)实验③得到的结论:___________ ,理由_________________________________ ;
(4)实验④得到的结论:___________ ,理由_________________________________ ;
(5)上述4个实验不能确定是否存在的阴离子是_________ ;
(6)如何检验溶液中是否含有NH4+_________________________________________ 。
实验①:测得混合液呈弱碱性
实验②:加入盐酸后,生成无色无味气味。该气体能使澄清石灰水变浑浊
实验③:加CCl4后,滴加少量氯水,振荡后,CCl4层未变色
实验④:加BaCl2溶液产生白色沉淀,该白色沉淀在足量盐酸中不能完全溶解
完成下列填空:
(1)实验①得到的结论:
(2)实验②得到的结论:
(3)实验③得到的结论:
(4)实验④得到的结论:
(5)上述4个实验不能确定是否存在的阴离子是
(6)如何检验溶液中是否含有NH4+
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在某澄清溶液中,可能存在下列几种离子:H+、K+、Ba2+、SO42-、I-、CO32-。取该溶液进行下列实验:
①用pH试纸检验,该溶液呈强酸性;
②取20mL溶液加入少量氯水和少量CCl4振荡后静置,CCl4层呈紫色;
③另取部分溶液逐滴加入NaOH溶液当溶液是碱性时,再加入Na2CO3溶液,有白色沉淀生成。
(1)根据上述实验现象、推断原溶液中肯定在的离子是________ ,肯定不存在的离子是_____ ,可能存在的离子是________ 。
(2)若步骤②中消耗0.01molCl2,则溶液中与Cl2反应的离子的物质的量浓度为_________ 。
(3)写出实验③中生成白色沉淀的离子方程式_________ 。
①用pH试纸检验,该溶液呈强酸性;
②取20mL溶液加入少量氯水和少量CCl4振荡后静置,CCl4层呈紫色;
③另取部分溶液逐滴加入NaOH溶液当溶液是碱性时,再加入Na2CO3溶液,有白色沉淀生成。
(1)根据上述实验现象、推断原溶液中肯定在的离子是
(2)若步骤②中消耗0.01molCl2,则溶液中与Cl2反应的离子的物质的量浓度为
(3)写出实验③中生成白色沉淀的离子方程式
您最近一年使用:0次
【推荐1】铁是人体内含量最多的必需微量元素,缺铁性贫血患者应补充含Fe2+的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁)是一种常见的补铁药物。某兴趣小组为了检验“速力菲”药片中Fe2+的存在并测定铁元素的含量,设计如下实验(假设反应过程无铁元素损耗):

请回答下列问题:
(1)操作I的名称是____________ ,试剂1是___________________ 。
(2)证明药片中含有Fe2+的依据________________ 。
(3)加入试剂1后溶液为淡红色,说明“速力菲”中的Fe2+已部分被氧化。通常在服用“速力菲”同时服用维生素C,说明维生素C具有________________ (填“氧化性”或“还原性”)。
(4)淡红色溶液中加入氯水,发生反应的离子方程式为__________________ 。
(5)Fe(OH)2沉淀也易被O2氧化,写出该反应的化学方程式_____________________ 。
(6)“速力菲”药片中铁元素的含量为_________________ (用含有a、b的式子表示)。

请回答下列问题:
(1)操作I的名称是
(2)证明药片中含有Fe2+的依据
(3)加入试剂1后溶液为淡红色,说明“速力菲”中的Fe2+已部分被氧化。通常在服用“速力菲”同时服用维生素C,说明维生素C具有
(4)淡红色溶液中加入氯水,发生反应的离子方程式为
(5)Fe(OH)2沉淀也易被O2氧化,写出该反应的化学方程式
(6)“速力菲”药片中铁元素的含量为
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
名校
【推荐2】离子液体是一种室温熔融盐,为非水体系.由有机阳离子、Al2Cl7﹣和AlCl4﹣组成的离子液体做电解液时,可在钢制品上电镀铝.
(1)钢制品应接电源的_______ 极,已知电镀过程中不产生其他离子且有机阳离子不参与电极反应,阴极电极反应式为________________ ,若改用AlCl3水溶液作电解液,则阴极产物为_____________ .
(2)为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应转移6mol电子时,所得还原产物的物质的量为________ mol.
(3)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有__________
a、KCl b、KClO3 c、MnO2 d、Mg
取少量铝热反应所得的固体混合物,将其溶于足量稀H2SO4,滴加KSCN溶液无明显现象,_______ (填“能”或“不能”)说明固体混合物中无Fe2O3,理由是__________________ (用离子方程式说明).
(1)钢制品应接电源的
(2)为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应转移6mol电子时,所得还原产物的物质的量为
(3)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有
a、KCl b、KClO3 c、MnO2 d、Mg
取少量铝热反应所得的固体混合物,将其溶于足量稀H2SO4,滴加KSCN溶液无明显现象,
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】化学学习小组欲探究铁及其化合物的氧化性和还原性。请你协助他们完成实验报告。
实验目的:探究铁及其化合物的氧化性和还原性。
实验试剂及仪器:
试剂:氯化亚铁溶液、氯化铁溶液、氯水、 溶液、铁粉、锌片、铜片、稀硫酸。
溶液、铁粉、锌片、铜片、稀硫酸。
仪器:胶头滴管、试管、烧杯等。
(1)实验记录(仿照①实验作答,填写空白部分)。
(2)在实验②中,有部分同学在氯化亚铁溶液中滴入  溶液后,出现了红色,你认为是什么原因:
溶液后,出现了红色,你认为是什么原因:___________ ;你对实验员在配制氯化亚铁溶液时,提出的建议是___________ 。
实验目的:探究铁及其化合物的氧化性和还原性。
实验试剂及仪器:
试剂:氯化亚铁溶液、氯化铁溶液、氯水、
 溶液、铁粉、锌片、铜片、稀硫酸。
溶液、铁粉、锌片、铜片、稀硫酸。仪器:胶头滴管、试管、烧杯等。
(1)实验记录(仿照①实验作答,填写空白部分)。
| 序号 | 实验设计 | 实验现象 | 离子方程式 | 解释与结论 |
| ① | 在铁粉中滴入稀硫酸 | 铁粉溶解,溶液由无色变成浅绿色,生成无色无味气体 | 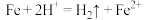 |  具有还原性 具有还原性 |
| ② |  溶液中滴入 溶液中滴入  溶液,再加氯水 溶液,再加氯水 | 滴入 溶液无明显变化,加入氯水立即变成红色 溶液无明显变化,加入氯水立即变成红色 | ||
| ③ |  溶液中加入锌片 溶液中加入锌片 |  | ||
| ④ |  |  具有氧化性 具有氧化性 |
 溶液后,出现了红色,你认为是什么原因:
溶液后,出现了红色,你认为是什么原因:
您最近一年使用:0次



