某研究性学习小组为了制取NH3,并探究NH3,铵盐相关的性质,进行了以下实验:

【制取氨气】
(1)A中发生反应的化学方程式为:_______________________ 。
(2)按图A装置制取NH3,生成的NH3,可用______ (填“浓H2SO4”或“碱石灰”)干燥,收集NH3应选择_______ (填“B”或“C”)装置。
(3)实验室制取O2、H2中,可选用A装置的气体是_________ 。
(4)若生成标准状况下22.4LNH3,至少需要NH4Cl的质量为___________ g(NH4Cl摩尔质量为53.5g·mol-1)。
【实验探究】
查阅资料可知:通常铵盐是白色晶体,易溶于水,受热易分,和碱反应能产生氨气。
(5)某同学用刚清洗过、含有较多水分的集气瓶收集氨气,__________ (填“能”或“不能”)收集到氨气。
(6)为确认某固体化肥样品中含有NH ,不必用到的试纸或试剂是
,不必用到的试纸或试剂是_____________ (只有一个正确选项)。
①NaOH溶液 ②红色石蕊试纸 ③稀H2SO4
(7)分别在两个集气瓶中滴入浓氨水和浓盐酸,盖上玻璃片,如图所示放置,然后抽去中间的玻璃片,观察到__________________ 现象。

【知识应用】
(8)为了防止碳酸氢铵肥效降低,你认为应该如何科学储存:_______________ (写出一种有效储存方法)。
(9)氨气的用途很广。如可利用氨气在催化剂存在的情况下与氧气反应来制取生产硝酸所需要的一氧化氮:4NH3+5O2 4NO+6H2O,在该反应中氨气体现
4NO+6H2O,在该反应中氨气体现 _________________ (选填“氧化性”或“还原性”)。请你列举氨气的另一种用途:______________ 。

【制取氨气】
(1)A中发生反应的化学方程式为:
(2)按图A装置制取NH3,生成的NH3,可用
(3)实验室制取O2、H2中,可选用A装置的气体是
(4)若生成标准状况下22.4LNH3,至少需要NH4Cl的质量为
【实验探究】
查阅资料可知:通常铵盐是白色晶体,易溶于水,受热易分,和碱反应能产生氨气。
(5)某同学用刚清洗过、含有较多水分的集气瓶收集氨气,
(6)为确认某固体化肥样品中含有NH
 ,不必用到的试纸或试剂是
,不必用到的试纸或试剂是①NaOH溶液 ②红色石蕊试纸 ③稀H2SO4
(7)分别在两个集气瓶中滴入浓氨水和浓盐酸,盖上玻璃片,如图所示放置,然后抽去中间的玻璃片,观察到

【知识应用】
(8)为了防止碳酸氢铵肥效降低,你认为应该如何科学储存:
(9)氨气的用途很广。如可利用氨气在催化剂存在的情况下与氧气反应来制取生产硝酸所需要的一氧化氮:4NH3+5O2
 4NO+6H2O,在该反应中氨气体现
4NO+6H2O,在该反应中氨气体现
更新时间:2023-09-20 22:27:21
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。

(1)A中装有Ca(OH)2和NH4Cl混合粉末,该反应的化学方程式是________________ 。
(2)B中加入的是碱石灰,其作用是_______________________________ 。
(3)实验时在C中观察到的现象是________________________________ 。发生反应的化学方程式是:______________________________ 。
(4)D中收集到的物质是____________ ,检验该物质的方法和现象是_______________________________ 。

(1)A中装有Ca(OH)2和NH4Cl混合粉末,该反应的化学方程式是
(2)B中加入的是碱石灰,其作用是
(3)实验时在C中观察到的现象是
(4)D中收集到的物质是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】Ⅰ、回答下列问题
(1)硅酸盐具有特殊的性质与应用,回答下列问题:硅酸盐材料是传统无机非金属材料,下列产品属于硅酸盐的是___________ (填序号)。
①玻璃 ②陶瓷 ③水晶 ④硅芯片 ⑤光导纤维 ⑥水泥 ⑦砖瓦
(2)SiO2是一种酸性氧化物。
①用化学方程式表示盛装NaOH溶液的试剂瓶不能用玻璃塞的原因:___________ 。
②熔化烧碱应选用的坩埚为___________ (填字母)。
A.铁坩埚 B.玻璃坩埚 C.石英坩埚 D.瓷坩埚
Ⅱ、某化学小组模拟工业生产制取HNO3,设计下图装置,其中a为一个可持续鼓入空气的橡皮球。

(3)装置A中主要反应的化学方程式为___________ 。
(4)F装置用浓NaOH溶液吸收NO2,生成物之一是NaNO2,请写出该反应的离子方程式:________ 。
(5)装置C中浓硫酸的主要作用是___________ 。
(6)干燥管中的碱石灰用于干燥NH3,某同学思考是否可用无水氯化钙代替碱石灰,并设计如图所示装置(仪器固定装置省略未画)进行验证,实验步骤如图:

①用烧瓶收集满干燥的氨气,立即塞如图所示的橡胶塞。
②正立烧瓶,使无水氯化钙固体滑入烧瓶底部,摇动,可以观察到的现象是___________ ,由此,该同学得出结论:不能用CaCl2代替碱石灰。
(1)硅酸盐具有特殊的性质与应用,回答下列问题:硅酸盐材料是传统无机非金属材料,下列产品属于硅酸盐的是
①玻璃 ②陶瓷 ③水晶 ④硅芯片 ⑤光导纤维 ⑥水泥 ⑦砖瓦
(2)SiO2是一种酸性氧化物。
①用化学方程式表示盛装NaOH溶液的试剂瓶不能用玻璃塞的原因:
②熔化烧碱应选用的坩埚为
A.铁坩埚 B.玻璃坩埚 C.石英坩埚 D.瓷坩埚
Ⅱ、某化学小组模拟工业生产制取HNO3,设计下图装置,其中a为一个可持续鼓入空气的橡皮球。

(3)装置A中主要反应的化学方程式为
(4)F装置用浓NaOH溶液吸收NO2,生成物之一是NaNO2,请写出该反应的离子方程式:
(5)装置C中浓硫酸的主要作用是
(6)干燥管中的碱石灰用于干燥NH3,某同学思考是否可用无水氯化钙代替碱石灰,并设计如图所示装置(仪器固定装置省略未画)进行验证,实验步骤如图:

①用烧瓶收集满干燥的氨气,立即塞如图所示的橡胶塞。
②正立烧瓶,使无水氯化钙固体滑入烧瓶底部,摇动,可以观察到的现象是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】某化学兴趣小组为了制取并探究氨气性质,按下列装置(部分夹持装置已略去)进行实验。
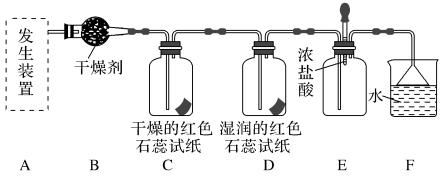
[实验探究]
(1)利用上述原理,实验室制取氨气应选用下图中___________ (填序号)发生装置进行实验。
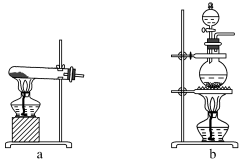
(2)B装置中的干燥剂可选用___________ (填“碱石灰”或“浓硫酸”)。
(3)用5.35 g NH4Cl固体与足量Ca(OH)2反应,最多可制得标准状况下氨气的体积为___________ L。(NH4Cl的摩尔质量为53.5 g·mol-1)
(4)气体通过C、D装置时,试纸颜色会发生变化的是___________ (填“C”或“D”)。
(5)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是___________ 。
(6)F装置中倒置漏斗的作用是___________ 。
(7)某同学用氨气和滴加酚酞的水做喷泉实验,根据烧瓶内产生红色喷泉的现象,说明氨气具有___________性质(填序号)。
(8)氨气的用途很广。如可用氨气处理二氧化氮:8NH3+6NO2=7N2+12H2O,该反应中氨气体现___________ (填“氧化性”或“还原性”)。请你列举出氨气的另一种用途:___________ 。

[实验探究]
(1)利用上述原理,实验室制取氨气应选用下图中

(2)B装置中的干燥剂可选用
(3)用5.35 g NH4Cl固体与足量Ca(OH)2反应,最多可制得标准状况下氨气的体积为
(4)气体通过C、D装置时,试纸颜色会发生变化的是
(5)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是
(6)F装置中倒置漏斗的作用是
(7)某同学用氨气和滴加酚酞的水做喷泉实验,根据烧瓶内产生红色喷泉的现象,说明氨气具有___________性质(填序号)。
| A.还原性 | B.极易溶于水 | C.与水反应生成碱性物质 |
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】如图,根据图示回答:
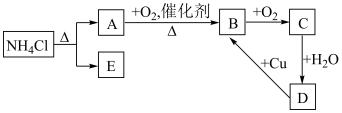
(1)A 的分子式为_____ ;B 的分子式为_____ ;C 的分子式为_____ 。
(2)将 E 溶于水,配制成 0.1 mol·L-1的溶液,滴入酚酞,显_____ 色。
(3)写出NH4Cl 溶液与NaOH 溶液共热反应的离子方程式:__________________ 。
(4)D→B 的化学方程式为:_____ 。
(5)A→B 的化学反应方程式:_____ 。

(1)A 的分子式为
(2)将 E 溶于水,配制成 0.1 mol·L-1的溶液,滴入酚酞,显
(3)写出NH4Cl 溶液与NaOH 溶液共热反应的离子方程式:
(4)D→B 的化学方程式为:
(5)A→B 的化学反应方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】某种常见的白色晶体A,与盐酸反应产生无刺激性气味的气体B:将B通入澄清石灰水中,石灰水变浑浊。若在A的水溶液中加入氢氧化钡溶液,则析出的白色沉淀C和无色气体D;D可以使湿润的红色石蕊试纸变蓝。加热固体A,可生成水、B和D,而且B和D的物质的量之比为1∶1。根据以上事实,可以判断出A是___ ,B是___ ,C是___ 。加热固体A生成水、B和D的化学方程式是___ 。
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】Ⅰ.硫和氮是人们熟悉的元素,含硫、含氮的物质与人们的生活密切相关。自然界中硫、氮的循环是维持生态平衡的重要物质基础。
(1)酸雨的pH___________ ,空气中的二氧化硫主要来自___________ 。
(2)检验溶液中 的方法是
的方法是___________ 。
(3)下列叙述中错误的是____。
(4)往蔗糖中加入浓硫酸后搅拌,有黑色物质产生,这表明浓硫酸有____。
(5)某化学兴趣小组践行绿色化学理念,通过改进后的微型实验装置(如图),用胶头滴管通过吸管向玻璃瓶中注入浓硫酸,并快速在吸管口塞上一团蘸有浓NaOH溶液的棉花团,制备并验证SO2的相关性质。

①实验中可观察到滴有紫色石蕊试液的棉签颜色变化为___________ ,蘸有溴水的棉签逐渐褪色,说明SO2具有___________ 性,蘸有品红溶液棉签逐渐褪色,说明SO2具有___________ 性。
②吸管口放置蘸有浓NaOH溶液的棉花团所起的作用是___________ 。
Ⅱ.已知氮元素及其化合物的转化关系如图所示,回答下列问题。

(6)①~④各步转化中,属于氮的固定的是___________ (填序号)。
(7)氨气的电子式为___________ ,中学化学实验室利用复分解反应来制备氨气,写出该反应的化学方程式___________ 。
(8)氨水中含有___________ 、___________ 、___________ 分子,以及含有___________ 、___________ 、___________ 离子。
(9)检验 的实验所依据的原理是____。
的实验所依据的原理是____。
①铵根离子与OH-发生反应产生氨气
②氨气极易溶于水
③NH3·H2O电离产生 和OH-
和OH-
④石蕊在碱性环境中变为蓝色
(10)除去下列物质中含有的少量杂质(括号中的物质)的方法中错误的是____。
(11)已知: ,这一反应叫做氨的催化氧化,是工业加热上制硝酸的基础,标出该反应的电子转移方向和数目:
,这一反应叫做氨的催化氧化,是工业加热上制硝酸的基础,标出该反应的电子转移方向和数目:_________ 。

(1)酸雨的pH
(2)检验溶液中
 的方法是
的方法是(3)下列叙述中错误的是____。
| A.葡萄酒中添加的SO2有抗氧化和杀菌等作用 |
| B.HCl、H2S、NH3都是电解质 |
| C.金刚石、石墨和C60是碳元素的同素异形体 |
| D.FeCl2、CuCl2都不能直接用单质通过化合反应制备 |
(4)往蔗糖中加入浓硫酸后搅拌,有黑色物质产生,这表明浓硫酸有____。
| A.吸水性 | B.脱水性 | C.强酸性 | D.强氧化性 |
(5)某化学兴趣小组践行绿色化学理念,通过改进后的微型实验装置(如图),用胶头滴管通过吸管向玻璃瓶中注入浓硫酸,并快速在吸管口塞上一团蘸有浓NaOH溶液的棉花团,制备并验证SO2的相关性质。

①实验中可观察到滴有紫色石蕊试液的棉签颜色变化为
②吸管口放置蘸有浓NaOH溶液的棉花团所起的作用是
Ⅱ.已知氮元素及其化合物的转化关系如图所示,回答下列问题。

(6)①~④各步转化中,属于氮的固定的是
(7)氨气的电子式为
(8)氨水中含有
(9)检验
 的实验所依据的原理是____。
的实验所依据的原理是____。①铵根离子与OH-发生反应产生氨气
②氨气极易溶于水
③NH3·H2O电离产生
 和OH-
和OH- ④石蕊在碱性环境中变为蓝色
| A.②④ | B.①③④ | C.①②④ | D.①②③④ |
(10)除去下列物质中含有的少量杂质(括号中的物质)的方法中错误的是____。
| A.H2(HCl):通过水洗涤 | B.NO2(NO):通入过量氧气 |
| C.NO(NH3):通过水洗涤 | D.NaCl(I2):加热 |
(11)已知:
 ,这一反应叫做氨的催化氧化,是工业加热上制硝酸的基础,标出该反应的电子转移方向和数目:
,这一反应叫做氨的催化氧化,是工业加热上制硝酸的基础,标出该反应的电子转移方向和数目:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】某溶液中可能含有NH 、Ba2+、Mg2+、Ag+、OH-、SO
、Ba2+、Mg2+、Ag+、OH-、SO 、CO
、CO 、Cl-和NO
、Cl-和NO 中的几种,且溶液中各离子的个数都相同。现用该溶液做以下实验:
中的几种,且溶液中各离子的个数都相同。现用该溶液做以下实验:
①取少量原溶液,加入足量盐酸无明显现象;
②另取少量原溶液,加入足量氢氧化钠溶液并微热,有白色沉淀产生及无色刺激性气味气体放出,该气体能使湿润的红色石蕊试纸变蓝。
请回答下列问题:
(1)实验①说明原溶液中不存在的离子为________ 。
(2)实验②说明原溶液中存在的离子为________ ,不存在的离子为________ 。
(3)②发生反应的离子方程式有________ 、________ 。
 、Ba2+、Mg2+、Ag+、OH-、SO
、Ba2+、Mg2+、Ag+、OH-、SO 、CO
、CO 、Cl-和NO
、Cl-和NO 中的几种,且溶液中各离子的个数都相同。现用该溶液做以下实验:
中的几种,且溶液中各离子的个数都相同。现用该溶液做以下实验:①取少量原溶液,加入足量盐酸无明显现象;
②另取少量原溶液,加入足量氢氧化钠溶液并微热,有白色沉淀产生及无色刺激性气味气体放出,该气体能使湿润的红色石蕊试纸变蓝。
请回答下列问题:
(1)实验①说明原溶液中不存在的离子为
(2)实验②说明原溶液中存在的离子为
(3)②发生反应的离子方程式有
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】形成酸雨的原理之一可简单表示如下:
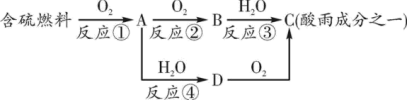
I.回答下列问题:
(1)酸雨的pH___________ (填“>”“<”或“=”)5.6.
(2)D物质的化学式为___________ 。
(3)反应②的化学方程式为___________ 。
II.已知A、B、C、D、E、F是含有同一种元素的化合物,其中F是能使湿润红色石蕊试纸变蓝的气体,它们之间能发生如下反应:①A+H2O→B+C ②C+F→D ③D+NaOH F+E+H2O
F+E+H2O
(4)写出下列物质的化学式:C___________ ,D___________ ,E___________ 。
(5)写出下列反应的离子方程式:
①___________ ;
③___________ 。

I.回答下列问题:
(1)酸雨的pH
(2)D物质的化学式为
(3)反应②的化学方程式为
II.已知A、B、C、D、E、F是含有同一种元素的化合物,其中F是能使湿润红色石蕊试纸变蓝的气体,它们之间能发生如下反应:①A+H2O→B+C ②C+F→D ③D+NaOH
 F+E+H2O
F+E+H2O(4)写出下列物质的化学式:C
(5)写出下列反应的离子方程式:
①
③
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】如图是一套制取并验证氯气部分化学性质的实验装置。
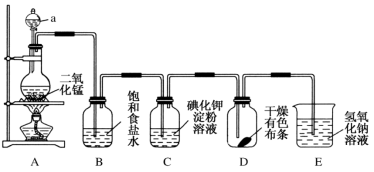
回答下列问题:
(1)装置A中,仪器a的名称___________ ,该仪器中盛放的试剂为___________ ,写出A装置发生反应的离子方程式:___________ 。
(2)当有少量Cl2通过后,观察到装置C中现象___________ 。
(3)当Cl2持续通过时,装置D中现象___________ 。
(4)若要证明Cl2无漂白性,则必须在装置___________ (用装置字母序号填写)之前增加装有浓硫酸洗气瓶的装置。
(5)装置E的作用是___________ ,该反应的离子方程式为:___________ 。

回答下列问题:
(1)装置A中,仪器a的名称
(2)当有少量Cl2通过后,观察到装置C中现象
(3)当Cl2持续通过时,装置D中现象
(4)若要证明Cl2无漂白性,则必须在装置
(5)装置E的作用是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】纯碳酸钙广泛应用于精密电子陶瓷、医药等的生产,某兴趣小组按图所示实验步骤,模拟工业流程制备高纯碳酸钙,请回答下列问题。
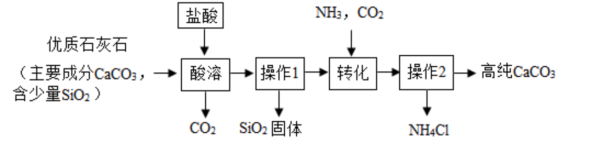
(1)“酸溶”过程中,提前将石灰石粉碎,并进行搅拌。目的是_______
(2)在“酸溶”过程中发生的化学反应方程式为_______
(3)“操作1”的名称_______
(4)实验室制取、收集干燥的NH3
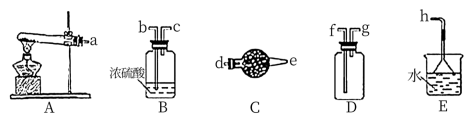
①需选用上述仪器装置的接口连接顺序是(填字母):a接_______ 、_______ 接_______ ,_______ 接h;实验室用A装置制取NH3的化学方程式为_______
②制备碳酸钙通入NH3和CO2气体时,应先通入的气体是_______ ,试写出制碳酸钙的化学方程式_______

(1)“酸溶”过程中,提前将石灰石粉碎,并进行搅拌。目的是
(2)在“酸溶”过程中发生的化学反应方程式为
(3)“操作1”的名称
(4)实验室制取、收集干燥的NH3

①需选用上述仪器装置的接口连接顺序是(填字母):a接
②制备碳酸钙通入NH3和CO2气体时,应先通入的气体是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】化学是一门以实验为基础的的自然科学,实验室常用块状大理石和稀盐酸制取 气体。
气体。
(1)写出实验室制取 的化学方程式
的化学方程式_______ 。
(2)若用如图所示装置(固定装置省略)制 。连接好装置后,需检查装置的气密性。具体操作方法是:先
。连接好装置后,需检查装置的气密性。具体操作方法是:先_______ (填字母,下同),后_______ 若导管口有气泡,放手后导管内上升一段稳定的水柱,则气密性良好。
A.用手捂住试管 B.将导管一端浸入水中

(3)实验室收集 可用的方法是
可用的方法是_______ (填字母)。
A.排水法 B.向下排空气法 C.向上排空气法
(4)若用上述发生装置在实验室还可以制取的气体是_______ 。
 气体。
气体。(1)写出实验室制取
 的化学方程式
的化学方程式(2)若用如图所示装置(固定装置省略)制
 。连接好装置后,需检查装置的气密性。具体操作方法是:先
。连接好装置后,需检查装置的气密性。具体操作方法是:先A.用手捂住试管 B.将导管一端浸入水中

(3)实验室收集
 可用的方法是
可用的方法是A.排水法 B.向下排空气法 C.向上排空气法
(4)若用上述发生装置在实验室还可以制取的气体是
您最近一年使用:0次




