 是重要的化学试剂,遇高温分解,与酸发生反应。实验室可通过如图所示装置制备
是重要的化学试剂,遇高温分解,与酸发生反应。实验室可通过如图所示装置制备 。
。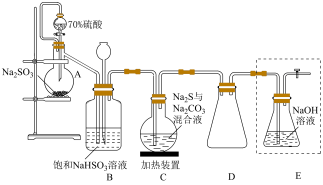
回答下列问题:
(1)仪器A的名称为
(2)下列关于装置B的作用叙述错误的是
a.通过观察气泡可控制
 气流速率
气流速率b.防止发生倒吸
c.通过长颈漏斗液面升降判断B后面装置是否堵塞
(3)C中生成产品的化学反应方程式为
(4)为保证硫代硫酸钠的产率和纯度,实验中通入的
 不能过量,原因是
不能过量,原因是(5)为测定所得产品纯度,取mg所得产品溶于蒸馏水中配制成
 溶液,取
溶液,取 置于锥形瓶中,加入2滴淀粉试剂,用
置于锥形瓶中,加入2滴淀粉试剂,用 碘的标准溶液滴定,消耗标准液
碘的标准溶液滴定,消耗标准液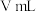 。
。已知:
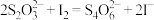
①滴定终点现象为
②产品纯度为
(6)下列装置和试剂不能代替E的是
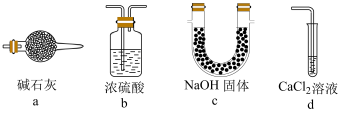
(7)硫化铜是一种难溶固体,晶胞中
 的位置如图1所示,
的位置如图1所示, 位于
位于 所构成的四面体中心,晶胞侧视图如图2所示。
所构成的四面体中心,晶胞侧视图如图2所示。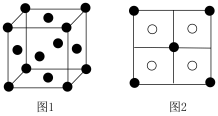
①与
 距离最近的
距离最近的 数目为
数目为②CuS的晶胞参数为apm,阿伏加德罗常数的值为
 ,则CuS晶体的密度为
,则CuS晶体的密度为 。
。
更新时间:2023-10-13 19:45:46
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
【推荐1】二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的消毒剂,是一种黄绿色的气体,其熔点为-59 ℃,沸点为11.0 ℃,易溶于水。工业上用稍潮湿的KClO3和草酸(H2C2O4)在60 ℃时反应制得。某学生拟用下图所示装置模拟工业制取并收集ClO2。
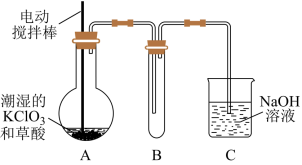
(1)A装置必须添加温度控制装置,除酒精灯外,还需要的玻璃仪器有烧杯、__________ 。
(2)B装置必须放在冰水浴中,其原因是______________________________ 。
(3)反应后在装置C中可得NaClO2溶液。已知:NaClO2饱和溶液在温度低于38℃时析出晶体是NaClO2•3H2O,高于38℃时析出晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。NaClO2的溶解度曲线如图
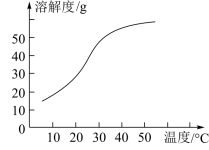
获得NaClO2晶体的操作步骤为:
①减压,55℃蒸发结晶;
②趁热过滤;
③______________________________________ ;
④在55℃干燥,得到成品。
(4)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的浓度,进行了下列实验:
步骤1:准确量取ClO2溶液10.00 mL,稀释成100.00 mL试样,量取V1 mL试样加入到锥形瓶中;
步骤2:用稀硫酸调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入指示剂,用c mol·L-1 Na2S2O3溶液滴定至终点。重复2次,测得消耗Na2S2O3溶液平均值为V2 mL(已知2Na2S2O3+I2===Na2S4O6+2NaI)。
①配制100 mL c mol·L-1 Na2S2O3标准溶液时,用到的玻璃仪器除烧杯、量筒、玻璃棒外还有:_______ 。
②若步骤2所得溶液放置时间太长,则测定结果____________ (填“偏高”、“偏低”或“不变”)
③ClO2溶液的浓度为________ g·L-1(用含字母的代数式表示)。

(1)A装置必须添加温度控制装置,除酒精灯外,还需要的玻璃仪器有烧杯、
(2)B装置必须放在冰水浴中,其原因是
(3)反应后在装置C中可得NaClO2溶液。已知:NaClO2饱和溶液在温度低于38℃时析出晶体是NaClO2•3H2O,高于38℃时析出晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。NaClO2的溶解度曲线如图

获得NaClO2晶体的操作步骤为:
①减压,55℃蒸发结晶;
②趁热过滤;
③
④在55℃干燥,得到成品。
(4)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的浓度,进行了下列实验:
步骤1:准确量取ClO2溶液10.00 mL,稀释成100.00 mL试样,量取V1 mL试样加入到锥形瓶中;
步骤2:用稀硫酸调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入指示剂,用c mol·L-1 Na2S2O3溶液滴定至终点。重复2次,测得消耗Na2S2O3溶液平均值为V2 mL(已知2Na2S2O3+I2===Na2S4O6+2NaI)。
①配制100 mL c mol·L-1 Na2S2O3标准溶液时,用到的玻璃仪器除烧杯、量筒、玻璃棒外还有:
②若步骤2所得溶液放置时间太长,则测定结果
③ClO2溶液的浓度为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】亚硝酰氯(NOCl,熔点:-64.5 ℃,沸点:-5.5 ℃)为红褐色液体或黄色气体,具有刺鼻恶臭味,遇水剧烈水解生成氮的两种氧化物与氯化氢,易溶于浓硫酸。常可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。其制备装置如图所示(其中Ⅲ、Ⅳ中均为浓硫酸):
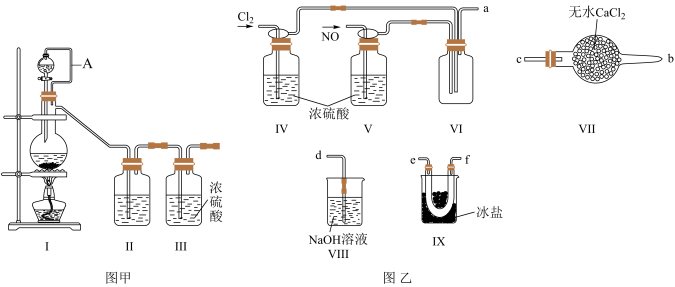
(1)用图甲中装置制备纯净干燥的原料气,补充下表中所缺少的药品。
(2)将制得的NO和Cl2通入图乙对应装置制备NOCl。
①装置连接顺序为a→_______ (按气流自左向右方向,用小写字母表示)。
②装置Ⅳ、Ⅴ除可进一步干燥NO、Cl2外,另一个作用是_______ 。
③有人认为可以将装置Ⅳ中浓硫酸合并到装置Ⅴ中,撤除装置Ⅳ,直接将NO、Cl2通入装置Ⅴ中,你同意此观点吗?你的理由是_______ 。
④实验开始的时候,先通入氯气,再通入NO,原因为_______ 。

(1)用图甲中装置制备纯净干燥的原料气,补充下表中所缺少的药品。
| 装置Ⅰ | 装置Ⅱ | ||
| 烧瓶中 | 分液漏斗中 | ||
| 制备纯净Cl2 | MnO2 | 浓盐酸 | ① |
| 制备纯净NO | Cu | 稀硝酸 | ② |
①装置连接顺序为a→
②装置Ⅳ、Ⅴ除可进一步干燥NO、Cl2外,另一个作用是
③有人认为可以将装置Ⅳ中浓硫酸合并到装置Ⅴ中,撤除装置Ⅳ,直接将NO、Cl2通入装置Ⅴ中,你同意此观点吗?你的理由是
④实验开始的时候,先通入氯气,再通入NO,原因为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】聚合硫酸铁又称聚铁,化学式为[Fe2(OH)n(SO4)3-0.5n]m,广泛用于污水处理。实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁和绿矾(FeSO4·7H2O),过程如下:

(1)验证固体W焙烧后产生的气体含有SO2的方法是:
______________________________________________________________ 。
(2)实验室制备、收集干燥的SO2,所需仪器如下。装置A产生SO2,按气流方向连接各仪器接口,顺序为a→____ →____ →____ →____ →f。
装置A中发生反应的化学方程式为_________________________________________ 。
装置D的作用是_____________ ,装置E中NaOH溶液的作用是_______________ 。

(3)制备绿矾时,向溶液X中加入过量__________ ,充分反应后,经过滤操作得到溶液Y,再经浓缩、结晶等步骤得到绿矾。过滤所需的玻璃仪器有____________________ 。
(4)欲测定溶液Y中Fe2+的浓度,需要用容量瓶配制KMnO4标准溶液,定容时视线应_____________________ ,直到_____________________ 。用KMnO4标准溶液滴定时应选用________ 滴定管(填“酸式”或“碱式”)。
(5)溶液Z的pH影响聚铁中铁的质量分数。若溶液Z的pH偏小,将导致聚铁中铁的质量分数______ (填“偏大”、“偏小”或“无影响”)。

(1)验证固体W焙烧后产生的气体含有SO2的方法是:
(2)实验室制备、收集干燥的SO2,所需仪器如下。装置A产生SO2,按气流方向连接各仪器接口,顺序为a→
装置A中发生反应的化学方程式为
装置D的作用是

(3)制备绿矾时,向溶液X中加入过量
(4)欲测定溶液Y中Fe2+的浓度,需要用容量瓶配制KMnO4标准溶液,定容时视线应
(5)溶液Z的pH影响聚铁中铁的质量分数。若溶液Z的pH偏小,将导致聚铁中铁的质量分数
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】连二亚硫酸钠( )是造纸工业中常用作漂白剂,能将有色物质还原为无色物质,提高纸浆白度。实验室利用如下流程来制备连二亚硫酸钠:
)是造纸工业中常用作漂白剂,能将有色物质还原为无色物质,提高纸浆白度。实验室利用如下流程来制备连二亚硫酸钠:
(1)第Ⅰ步需要 ,若要制取并收集干燥纯净的
,若要制取并收集干燥纯净的 ,所用装置如图所示:
,所用装置如图所示:______ ,按气流方向连接各仪器口,顺序为a______ 。
②装置D中的试剂为______ ,装置E烧杯中发生反应的离子方程式为______ 。
(2)利用下列装置制取连二亚硫酸钠: ,三颈烧瓶中发生反应的化学方程式为
,三颈烧瓶中发生反应的化学方程式为______ ,再打开活塞,加入NaOH溶液制得 。
。
下列制取 的有关说法正确的是
的有关说法正确的是______ 。
a. 的漂白原理与
的漂白原理与 相同
相同
b.单向阀的作用是只让气体进入并防倒吸
c.尾气可以用 溶液处理
溶液处理
②测定产品纯度:称取a g样品溶于水配成250mL溶液,准确量取25.00mL溶液于锥形瓶中,加入足量甲醛(HCHO)溶液,充分反应后,加入几滴淀粉溶液,滴加c mol/L碘水至反应完全,消耗碘水20.00mL。上述过程发生的反应有:


则该样品纯度为______ 。
 )是造纸工业中常用作漂白剂,能将有色物质还原为无色物质,提高纸浆白度。实验室利用如下流程来制备连二亚硫酸钠:
)是造纸工业中常用作漂白剂,能将有色物质还原为无色物质,提高纸浆白度。实验室利用如下流程来制备连二亚硫酸钠: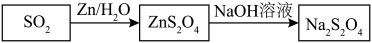
(1)第Ⅰ步需要
 ,若要制取并收集干燥纯净的
,若要制取并收集干燥纯净的 ,所用装置如图所示:
,所用装置如图所示: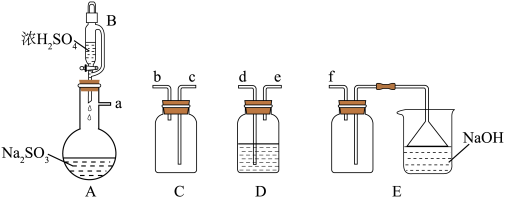
②装置D中的试剂为
(2)利用下列装置制取连二亚硫酸钠:

 ,三颈烧瓶中发生反应的化学方程式为
,三颈烧瓶中发生反应的化学方程式为 。
。下列制取
 的有关说法正确的是
的有关说法正确的是a.
 的漂白原理与
的漂白原理与 相同
相同b.单向阀的作用是只让气体进入并防倒吸
c.尾气可以用
 溶液处理
溶液处理②测定产品纯度:称取a g样品溶于水配成250mL溶液,准确量取25.00mL溶液于锥形瓶中,加入足量甲醛(HCHO)溶液,充分反应后,加入几滴淀粉溶液,滴加c mol/L碘水至反应完全,消耗碘水20.00mL。上述过程发生的反应有:


则该样品纯度为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】亚硝酰氯(NOCl,熔点:-64.5℃,沸点:-5.5℃)为红褐色液体或黄色气体,具有刺鼻恶臭味,遇水剧烈水解生成氮的两种氧化物与氯化氢,易溶于浓硫酸。常可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。其制备装置如图所示(其中Ⅲ、Ⅳ中均为浓硫酸):

(1)用图甲中装置制备纯净干燥的原料气,补充表中所缺少的药品。
(2)将制得的NO和Cl2通入图乙对应装置制备NOCl。
①装置连接顺序为a→___ (按气流自左向右方向,用小写字母表示)。
②装置Ⅳ、Ⅴ除可进一步干燥NO、Cl2外,另一个作用是___ 。
③有人认为可以将装置Ⅳ中浓硫酸合并到装置Ⅴ中,撤除装置Ⅳ,直接将NO、Cl2通入装置Ⅴ中,你同意此观点吗?你的理由是___ 。
④实验开始的时候,先通入氯气,再通入NO,原因为___ 。
(3)制得的NOCl中可能含有少量N2O4杂质,为测定产品纯度进行如下实验:称取1.6625g样品溶于50.00mLNaOH溶液中,加入几滴K2CrO4溶液作指示剂,用足量硝酸酸化的0.40mol/LAgNO3溶液滴定至产生砖红色沉淀,消耗AgNO3溶液50.00mL。
①样品的纯度(质量分数)为___ %(保留1位小数)。
②已知常温下,Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=2×10-12,若在滴定终点时测得溶液中CrO 的浓度是5.0×10-3mol/L,此时溶液中Cl-浓度是
的浓度是5.0×10-3mol/L,此时溶液中Cl-浓度是___ 。

(1)用图甲中装置制备纯净干燥的原料气,补充表中所缺少的药品。
| 装置Ⅰ | 装置Ⅱ | ||
| 烧瓶中 | 分液漏斗中 | ||
| 制备纯净Cl2 | MnO2 | 浓盐酸 | ① |
| 制备纯净NO | Cu | 稀硝酸 | ② |
①装置连接顺序为a→
②装置Ⅳ、Ⅴ除可进一步干燥NO、Cl2外,另一个作用是
③有人认为可以将装置Ⅳ中浓硫酸合并到装置Ⅴ中,撤除装置Ⅳ,直接将NO、Cl2通入装置Ⅴ中,你同意此观点吗?你的理由是
④实验开始的时候,先通入氯气,再通入NO,原因为
(3)制得的NOCl中可能含有少量N2O4杂质,为测定产品纯度进行如下实验:称取1.6625g样品溶于50.00mLNaOH溶液中,加入几滴K2CrO4溶液作指示剂,用足量硝酸酸化的0.40mol/LAgNO3溶液滴定至产生砖红色沉淀,消耗AgNO3溶液50.00mL。
①样品的纯度(质量分数)为
②已知常温下,Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=2×10-12,若在滴定终点时测得溶液中CrO
 的浓度是5.0×10-3mol/L,此时溶液中Cl-浓度是
的浓度是5.0×10-3mol/L,此时溶液中Cl-浓度是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】镁条投入盐酸时,快速溶解并产生大量气泡;投入热水时,其表面会附着微量气泡。受此启发,某兴趣小组对Mg与NaHCO3溶液的反应进行了如下探究:
I.探究反应产生的气体成分。
(1)经检验反应产生的气体有H2,实验室检验H2的方法为_______ 。
(2)小组成员认为反应产生的气体中可能有CO2,并对此进行了如下实验(图1、图2中曲线②均为对应加入镁条的数据):
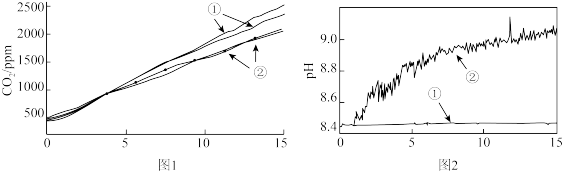
图1中曲线②对应的CO2含量逐渐增大的原因为_______ (用化学方程式表示);结合实验3解释,随着时间推移,图1中曲线②的数值低于曲线①的原因为_______ 。
II.探究Mg与NaHCO3溶液反应比与热水反应快的原因。
小组成员推测可能是溶液中的Na+或HCO 加快了该反应的发生,对比实验1设计实验如下:
加快了该反应的发生,对比实验1设计实验如下:
(3)结合实验1和4,可知溶液中的HCO 加快了反应的发生。
加快了反应的发生。
①实验4中横线处内容为_______ 。
②查阅文献可知,Mg(OH)2质地致密,MgCO3质地疏松,请结合必要的文字和化学用语解释HCO 能加快该反应的原因为
能加快该反应的原因为_______ 。
III.探究固体浑浊物的组成。
文献显示,固体浑浊物为Mg(OH)2和MgCO3的混合物。甲、乙两位同学设计不同方案,测定混合物组成。
(4)甲同学借助下图装置(可重复选用),通过测定固体热分解产物水及二氧化碳的质量,测定其组成。按照该方案,装置的连接顺序为_______ (填字母编号)。

(5)乙同学只测定了固体浑浊物在热分解前后的质量分别为3.42 g和2.00g,据此计算出固体浑浊物中n[Mg(OH)2]:n[MgCO3]=_______ 。
| 实验序号 | 实验操作 | 实验现象 |
| 1 | 向7.5 mL1mol·L-1NaHCO3溶液中加入长3cm的镁条 | 持续快速产生大量气泡,溶液略显浑浊 |
(1)经检验反应产生的气体有H2,实验室检验H2的方法为
(2)小组成员认为反应产生的气体中可能有CO2,并对此进行了如下实验(图1、图2中曲线②均为对应加入镁条的数据):
| 实验序号 | 实验操作 |
| 2 | 分别称取两份6.0 mL 1 mol·L-1NaHCO3溶液于两个相同塑料瓶中(其中一个加入0.1g镁条),塞紧CO2气体传感器,采集数据,各重复实验1次,得到图1所示曲线 |
| 3 | 分别称取两份30.0 mL 1 mol·L-1NaHCO3溶液于两个相同烧杯中(其中一个加入1.1g镁条),插入pH传感器,搅拌并采集数据,得到图2所示曲线 |

图1中曲线②对应的CO2含量逐渐增大的原因为
II.探究Mg与NaHCO3溶液反应比与热水反应快的原因。
小组成员推测可能是溶液中的Na+或HCO
 加快了该反应的发生,对比实验1设计实验如下:
加快了该反应的发生,对比实验1设计实验如下:| 实验序号 | 实验操作 | 实验现象 |
| 4 | 向_______溶液中加入长3 cm的镁条 | 持续快速产生大量气泡,溶液略显浑浊 |
 加快了反应的发生。
加快了反应的发生。①实验4中横线处内容为
②查阅文献可知,Mg(OH)2质地致密,MgCO3质地疏松,请结合必要的文字和化学用语解释HCO
 能加快该反应的原因为
能加快该反应的原因为III.探究固体浑浊物的组成。
文献显示,固体浑浊物为Mg(OH)2和MgCO3的混合物。甲、乙两位同学设计不同方案,测定混合物组成。
(4)甲同学借助下图装置(可重复选用),通过测定固体热分解产物水及二氧化碳的质量,测定其组成。按照该方案,装置的连接顺序为

(5)乙同学只测定了固体浑浊物在热分解前后的质量分别为3.42 g和2.00g,据此计算出固体浑浊物中n[Mg(OH)2]:n[MgCO3]=
您最近一年使用:0次



