X、Y、Z、W是原子序数依次增大的短周期主族元素,X与W位于同主族,Y原子的最外层电子数是内层电子数的3倍,X、Y、W形成的一种化合物M结构式如图所示。下列说法中错误的是


| A.上述四种元素的电负性最大的是Z | B.化合物M的晶体类型为离子晶体 |
| C.Z单质可以与水反应生成Y单质 | D.简单离子半径: |
更新时间:2023-10-25 23:02:57
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】R、X、Y、Z均为短周期主族元素,Y与Z同主族且Z的原子序数大于Y。R和X的原子获得1个电子均可形成稀有气体原子的电子层结构,R的最高化合价为+1。1mol化合物RZY3X含58mol电子。下列说法正确的是
| A.R与X形成的化合物水溶液呈碱性 | B.X是四种元素中原子半径最大的 |
| C.Y单质的氧化性比Z单质的弱 | D.Z的原子最外层电子数为6 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】X、Y、Z为第三周期原子序数依次增大的三种元素,Y是地壳中含量最高的金属元素,三种元素可以形成化合物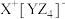 。下列说法不正确的是
。下列说法不正确的是
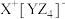 。下列说法不正确的是
。下列说法不正确的是| A.简单离子半径:X>Y>Z | B.基态Y原子最高能级的轨道数为3 |
| C.电负性:X<Y<Z | D.基态Z原子3p轨道上各电子能量相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】现有部分短周期元素的性质或原子结构如下表:
下列说法正确的是
元素编号 | 元素性质或原子结构 |
| 最外层电子数是次外层电子数的2倍 |
|
|
|
|
| 最高正价为+7 |
A. 离子的结构示意图为 离子的结构示意图为 |
B. 的中心原子采取 的中心原子采取 杂化 杂化 |
C.元素 在周期表中表示为 在周期表中表示为 |
D.XZ3为极性分子, 为非极性分子 为非极性分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】W、X、Y和Z为原子序数依次增大的四种短周期元素。W与X组成的某种化合物是一种红棕色有刺激性气味的气体;Y的周期数是族序数的3倍;X、Z同主族。下列叙述正确的是( )
| A.X与其他三种元素均可形成两种或两种以上的二元化合物 |
| B.Y与其他三种元素分别形成的化合物中只含有离子键 |
| C.四种元素的简单离子具有相同的电子层结构 |
| D.W的氧化物对应的水化物均为强酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】短周期主族元素W、X、Y、Z的原子序数依次增大,X的原子半径是短周期主族元素中最大的,W的核外电子数与X、Z的最外层电子数之和相等,Y的原子序数是Z的最外层电子数的2倍,由W、X、Y三种元素形成的化合物M结构如图。下列叙述正确的是
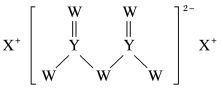

| A.W、X按原子组成比1:1形成的化合物中,阴阳离子数目比为1:1 |
| B.元素非金属性强弱的顺序:W>Z |
| C.Y的最高价氧化物对应水化物的酸性强于Z |
| D.化合物M中W不都满足8电子稳定结构 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】近年来,光催化剂的研究是材料领域的热点方向。如图一种 配合物复合光催化剂,可将
配合物复合光催化剂,可将 转化为
转化为 。下列说法错误的是
。下列说法错误的是

 配合物复合光催化剂,可将
配合物复合光催化剂,可将 转化为
转化为 。下列说法错误的是
。下列说法错误的是
A.该配合物中 的配位数是6,中心离子为 的配位数是6,中心离子为 |
B. 配合物中第二周期元素的电负性由大到小的顺序为 配合物中第二周期元素的电负性由大到小的顺序为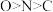 |
C.已知吡啶(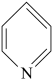 )中所有原子共平面,则吡啶中存在 )中所有原子共平面,则吡啶中存在 大π键 大π键 |
D. 的沸点比 的沸点比 高,主要原因是 高,主要原因是 分子间存在范德华力和氢键,而 分子间存在范德华力和氢键,而 分子间只有范德华力 分子间只有范德华力 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列叙述及相关解释均正确的是
| 选项 | 叙述 | 解释 |
| A | 还原性:HI>HBr | 范德华力:HI>HCl |
| B | 稳定性: | O与S同主族,得电子能力:O<S |
| C | 沸点: | 前者能形成分子内氢键后者能形成分子间氢键 |
| D | 键的极性的强弱:H-O<H-F | 电负性:O<F |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】M、W、X、Y、Z五种短周期非金属元素原子序数依次增大,Z为地壳中含量最高的元素,基态Y原子p轨道上的电子处于半充满状态。由五种元素组成某种电池材料的结构如图所示,下列说法正确的是

| A.简单离子半径:M<X<Y<Z |
| B.简单氢化物沸点:Y<X |
| C.电负性:M<X<Y<Z |
| D.W的最高价氧化物对应水化物为强酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】金属铅的晶粒大小与熔点关系如图所示。下列叙述正确的是
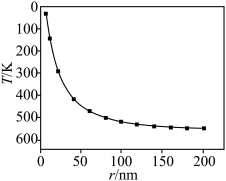

| A.铅与锗位于同主族且单质晶体类型相同 | B.铅晶粒越大,其熔点越低 |
| C.铅晶体中含阳离子,必含阴离子 | D.铅晶体熔点高低与晶粒表面积大小有关 |
您最近一年使用:0次
【推荐2】X、Y、Z、W、Q是周期表中前4周期元素,且原子序数依次增大。X、Z的基态原子2p轨道中均有2个未成对电子,W的最外层电子数是次外层的一半,Q最外层有1个电子,内层电子全部充满。Q2+能与NH3形成[Q(NH3)4]2+,[Q(NH3)4]2+中2个NH3被2个Cl-取代可得两种不同的结构。Q2Z种晶胞如下图所示。
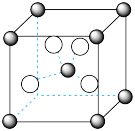
下列说法正确的是

下列说法正确的是
| A.X的一种晶体具有很大的硬度,1 mol该晶体中含有4molX-X键 |
| B.Y2、Z2的晶体类型均为共价晶体 |
| C.[Q(NH3)4]2+的空间构型为正四面体形 |
| D.Q2Z晶胞中,距离每个Q+最近的Z2-有2个 |
您最近一年使用:0次


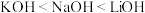
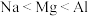

 层有3个未成对电子
层有3个未成对电子
 电子数比
电子数比 电子数多2个
电子数多2个 (金刚石)
(金刚石) 可实现人工合成金刚石。下列关于该反应的说法不正确的是
可实现人工合成金刚石。下列关于该反应的说法不正确的是 与金刚石中的C原子杂化轨道类型不同
与金刚石中的C原子杂化轨道类型不同

