下图是氮单质及其化合物的“价类二维图”。
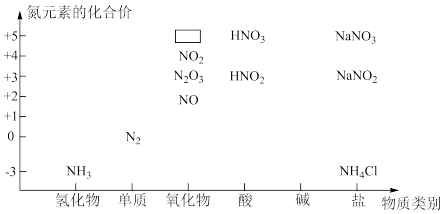
(1)写出氮元素在元素周期表中的位置:_____ 。
(2)图中方框中的化学式为_____ ,氨分子的电子式为_____ ,一水合氨电离可使溶液显碱性,写出一水合氨的电离方程式:_____ 。
(3)向盛有少量NH4Cl溶液的试管中加入NaOH溶液并加热,在试管口放一片湿润的红色石蕊试纸,实验现象是_____ 。
(4)氮的最高价氧化物的水化物为_____ (填写化学式),由于其见光易分解,故常保存在棕色瓶中,其分解的化学方程式为:_____ 。若有4mol该分子发生分解,则过程中转移的电子数目为_____ 。

(1)写出氮元素在元素周期表中的位置:
(2)图中方框中的化学式为
(3)向盛有少量NH4Cl溶液的试管中加入NaOH溶液并加热,在试管口放一片湿润的红色石蕊试纸,实验现象是
(4)氮的最高价氧化物的水化物为
更新时间:2023-10-28 06:03:44
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氮元素是地球大气中含量最多的元素,请完成下列有关问题:
(1)写出氮元素的原子结构示意图:_______ 。
(2)通常情况下,氮气性质不活泼,其原因是__________。
(3)N2的电子式:_______ ,将空气中的氮气转化为氮的化合物的过程称为固氮。下列能实现人工固氮的是_______ 。
A.N2和H2在一定条件下反应生成NH3 B.雷雨闪电时空气中的N2和O2化合生成NO
C.NH3经过催化氧化生成NO D.NH3和HNO3反应生成NH4NO3
(4)氨气的电子式:_______ 。
(5)实验室通常用加热消石灰与氯化铵固体的方法来制取氨气。写出此反应的化学方程式_____ 。
(1)写出氮元素的原子结构示意图:
(2)通常情况下,氮气性质不活泼,其原因是__________。
| A.氮分子是双原子分子 | B.氮元素的非金属性很强 |
| C.氮原子的半径较小 | D.破坏氮分子中的化学键很难 |
A.N2和H2在一定条件下反应生成NH3 B.雷雨闪电时空气中的N2和O2化合生成NO
C.NH3经过催化氧化生成NO D.NH3和HNO3反应生成NH4NO3
(4)氨气的电子式:
(5)实验室通常用加热消石灰与氯化铵固体的方法来制取氨气。写出此反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。回答下列问题:
(1)联氨分子的结构式为___________ 。
(2)美国加利福尼亚大学圣地亚哥的G· N·SChrauzer等人用氮气和水蒸气在触媒上,光照射下合成高能气态联氨初获成功。该反应的热化学方程式为___________ 。
(3)①2O2(g)+N2(g)=N2O4(l) ΔH1
②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) ΔH4=-1048.9kJ·mol-1
上述反应热效应之间的关系式为ΔH4=___________ ;联氨和N2O4可作为火箭推进剂的主要原因为___________ 。
(4)火箭推进器中还可以装联氨和过氧化氢,当它们混合时即产生气体,并放出大量热。已知16 g联氨与足量过氧化氢反应生成氮气和水蒸气,放出321kJ的热量,写出该反应的热化学方程式___________ 。
(5)联氨常由氨气和次氯酸钠溶液反应制得,写出该反应的离子方程式___________ 。
(6)在高温下,N2H4可完全分解为NH3、N2及H2 ,实验测得分解产物中N2与H2的物质的量之比为3:2,则该分解反应的化学方程式为___________ 。
(7)联氨为二元弱碱,在水中的电离方式与氨气相似。写出联氨与过量盐酸反应的离子方程式___________ 。
(1)联氨分子的结构式为
(2)美国加利福尼亚大学圣地亚哥的G· N·SChrauzer等人用氮气和水蒸气在触媒上,光照射下合成高能气态联氨初获成功。该反应的热化学方程式为
| 化学键 | N-H | H-O | O=O | N≡N | N-N |
| 键能/KJ·mol-1 | 391 | 463 | 496 | 946 | 159 |
②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) ΔH4=-1048.9kJ·mol-1
上述反应热效应之间的关系式为ΔH4=
(4)火箭推进器中还可以装联氨和过氧化氢,当它们混合时即产生气体,并放出大量热。已知16 g联氨与足量过氧化氢反应生成氮气和水蒸气,放出321kJ的热量,写出该反应的热化学方程式
(5)联氨常由氨气和次氯酸钠溶液反应制得,写出该反应的离子方程式
(6)在高温下,N2H4可完全分解为NH3、N2及H2 ,实验测得分解产物中N2与H2的物质的量之比为3:2,则该分解反应的化学方程式为
(7)联氨为二元弱碱,在水中的电离方式与氨气相似。写出联氨与过量盐酸反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】Ⅰ.(1)在100 mL 0.8mol/L硝酸溶液中加入足量铜粉,则被溶解的铜的质量为_______ g。
(2)在上述溶液中再加入足量稀硫酸,又有_______ g铜溶解。
Ⅱ. 请回答下列问题:25℃时,浓度均为0.10mol • L﹣1的 ①氨水 ②NH4Cl溶液
(1)NH4Cl溶液显_________ (酸、碱、中)性,原因是(用离子方程式表示)____________________________________ ,若加入少量的氨水,使溶液中c(NH4+)=c(Cl﹣),则溶液的pH_____ 7 (填“>”、“<”或“=”).
(2)氨水显碱性的原因(用离子方程式表示)______________________ ,向氨水中加入NH4Cl固体,氨水的电离程度________ (填“增大”、“减小”或“不变”),溶液的pH将________ (填“增大”、“减小”或“不变”).
(2)在上述溶液中再加入足量稀硫酸,又有
Ⅱ. 请回答下列问题:25℃时,浓度均为0.10mol • L﹣1的 ①氨水 ②NH4Cl溶液
(1)NH4Cl溶液显
(2)氨水显碱性的原因(用离子方程式表示)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.分别只用一种试剂除去下列各组中所含的少量杂质(括号内为杂质),在空格中填上需加入最适合的一种试剂:
(1)FeCl3溶液(FeCl2)________________ ,
(2)FeCl2溶液(FeCl3)________________ ,
(3)Fe 粉末(Al)_______________ ,
Ⅱ.为测定某镁铝合金样品中铝的含量,进行了下列实验:取一定量合金,加入100 mL 0.3 mol·L-1稀硝酸,合金完全溶解,产生的气体在标准状况下体积为560 mL;再加入0.2 mol·L-1 NaOH溶液至沉淀质量恰好不再变化,用去300 mL NaOH溶液。则所取样品中铝的物质的量为___________ ,反应中转移的电子数为______________ 。
(1)FeCl3溶液(FeCl2)
(2)FeCl2溶液(FeCl3)
(3)Fe 粉末(Al)
Ⅱ.为测定某镁铝合金样品中铝的含量,进行了下列实验:取一定量合金,加入100 mL 0.3 mol·L-1稀硝酸,合金完全溶解,产生的气体在标准状况下体积为560 mL;再加入0.2 mol·L-1 NaOH溶液至沉淀质量恰好不再变化,用去300 mL NaOH溶液。则所取样品中铝的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】已知 和
和 在常温下可快速反应生成氮气:
在常温下可快速反应生成氮气: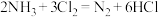 。当
。当 过量时,会发生反应
过量时,会发生反应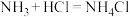 ,产生白烟,因此当
,产生白烟,因此当 和
和 比例不同时,产物有差异。
比例不同时,产物有差异。
(1)若利用该反应处理含有氨气和氯气的尾气,用于制备盐酸,则 和
和 的最佳比例为
的最佳比例为_______ 。该反应可用于检验化工生产中氯气是否泄漏。若氯气有少量泄漏,用氨气检验时有明显现象,此过程中发生反应的 和
和 的体积比范围为
的体积比范围为_______ 。
(2)体积为 ,质量为
,质量为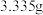 的
的 和
和 的混合气体通过浓氨水后,体积变为
的混合气体通过浓氨水后,体积变为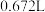 (其中
(其中 体积分数为50%)。两位同学想要根据这些数据计算被氧化的
体积分数为50%)。两位同学想要根据这些数据计算被氧化的 的质量。下面是两位学生从不同角度解题时所列的第一步算式,请判断他们所列未知数X分别表示什么量,并填写在表格内:(单位没列出)
的质量。下面是两位学生从不同角度解题时所列的第一步算式,请判断他们所列未知数X分别表示什么量,并填写在表格内:(单位没列出)
 和
和 在常温下可快速反应生成氮气:
在常温下可快速反应生成氮气: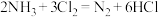 。当
。当 过量时,会发生反应
过量时,会发生反应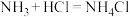 ,产生白烟,因此当
,产生白烟,因此当 和
和 比例不同时,产物有差异。
比例不同时,产物有差异。(1)若利用该反应处理含有氨气和氯气的尾气,用于制备盐酸,则
 和
和 的最佳比例为
的最佳比例为 和
和 的体积比范围为
的体积比范围为(2)体积为
 ,质量为
,质量为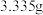 的
的 和
和 的混合气体通过浓氨水后,体积变为
的混合气体通过浓氨水后,体积变为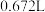 (其中
(其中 体积分数为50%)。两位同学想要根据这些数据计算被氧化的
体积分数为50%)。两位同学想要根据这些数据计算被氧化的 的质量。下面是两位学生从不同角度解题时所列的第一步算式,请判断他们所列未知数X分别表示什么量,并填写在表格内:(单位没列出)
的质量。下面是两位学生从不同角度解题时所列的第一步算式,请判断他们所列未知数X分别表示什么量,并填写在表格内:(单位没列出)| 学生编号 | 所列第一步算式 | 未知数X表示的意义 |
| 甲 | 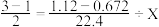 | |
| 乙 | 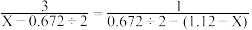 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】高氯酸三碳酰肼合镍(GTN)的组成可表示为[Ni(CHZ3)( ClO4)2],其中CHZ为碳酰肼(结构简式为: )。已知N2H4、NH2OH (羟胺)具有类似于NH3的碱性。
)。已知N2H4、NH2OH (羟胺)具有类似于NH3的碱性。

请用方程式解释羟胺水溶液呈碱性___________ 。工业上常用尿素和NaClO - NaOH溶液反应实现转化2得到N2H4和两种常见钠盐,反应的化学方程式为___________ 。
 )。已知N2H4、NH2OH (羟胺)具有类似于NH3的碱性。
)。已知N2H4、NH2OH (羟胺)具有类似于NH3的碱性。
请用方程式解释羟胺水溶液呈碱性
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】右表是元素周期表的一部分。
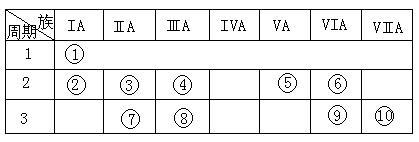
(1)表中元素⑩的氢化物的化学式为__________ ,此氢化物的还原性比元素⑨的氢化物的还原性_____________ (填强或弱)
(2)某元素原子的核外p电子数比s电子数少1,则该元素的元素符号是_____ ,其单质的电子式为________________ 。
(3)已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质。写出元素③的氢氧化物与NaOH溶液反应的化学方程式____________________ ;又如表中与元素⑦的性质相似的不同族元素是___________ (填元素符号)

(1)表中元素⑩的氢化物的化学式为
(2)某元素原子的核外p电子数比s电子数少1,则该元素的元素符号是
(3)已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质。写出元素③的氢氧化物与NaOH溶液反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下列为周期表的一部分,据此回答下列有关问题:
(1)写出元素符号 :①_______ ,⑤________ ,⑦_______ ,⑧________ 。
(2)表中所列元素中,最活泼的金属元素是______ (填元素符号,下同),最活泼的非金属元素是_______ 。
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是_________ (填化学式,下同),碱性最强的是_________ ,呈两性的是_________ 。
 族 周期 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)写出
(2)表中所列元素中,最活泼的金属元素是
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求填空:
(1)某原子含有 6 个质子和 8 个中子,用核素符号表示该原子__________ ;(用元素符号表示)
(2)写电子式:HClO:____ ;NH4+:_____ ;写结构式:CCl4:_____ ;CS2:_____ ;
(3)画出钙原子的原子结构示意图:____ ;画出溴离子的离子结构示意图:____ ;
(4)用电子式表示氯化钠的形成过程:_________________________
(5)按要求排序:
下列离子半径由大到小的顺序是:S2- ;Al3+ ;Na+ ;F- ;______________
下列物质熔沸点由高到低的顺序是:H2O;Na2O;H2Se;I2 ;______________
(1)某原子含有 6 个质子和 8 个中子,用核素符号表示该原子
(2)写电子式:HClO:
(3)画出钙原子的原子结构示意图:
(4)用电子式表示氯化钠的形成过程:
(5)按要求排序:
下列离子半径由大到小的顺序是:S2- ;Al3+ ;Na+ ;F- ;
下列物质熔沸点由高到低的顺序是:H2O;Na2O;H2Se;I2 ;
您最近一年使用:0次

 、S2-
、S2- 



