以软锰矿(主要成分是 ,含有
,含有 、FeO、
、FeO、 等少量杂质)为主要原料,制取高纯
等少量杂质)为主要原料,制取高纯 ,流程如图所示。
,流程如图所示。
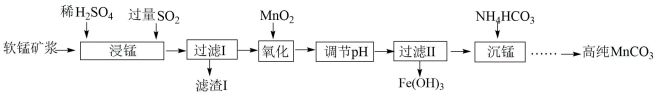
已知: 难溶于水,且不与稀
难溶于水,且不与稀 、
、 反应。
反应。
回答下列问题:
(1)FeO属于___________ (填“酸性”或“碱性”)氧化物,将其在空气中加热能迅速被氧化为___________ 。
(2)“浸锰”步骤中, 与
与 发生反应,在此过程中
发生反应,在此过程中 表现了
表现了___________ (填“氧化性”或“还原性”)。
(3)经“过滤I”后,溶液中所含金属离子为___________ (填离子符号)。
(4)“氧化”步骤中,加入 的作用为
的作用为___________ (用化学方程式表示)。
(5)“沉锰”步骤中,除了生成产品 外,还有气体生成,该反应的离子方程式为
外,还有气体生成,该反应的离子方程式为______ 。
(6)取23.0g所得产品(高纯 )溶于足量的盐酸中,共产生
)溶于足量的盐酸中,共产生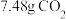 ,计算产品中碳酸锰的质量分数为
,计算产品中碳酸锰的质量分数为___________ %。
 ,含有
,含有 、FeO、
、FeO、 等少量杂质)为主要原料,制取高纯
等少量杂质)为主要原料,制取高纯 ,流程如图所示。
,流程如图所示。
已知:
 难溶于水,且不与稀
难溶于水,且不与稀 、
、 反应。
反应。回答下列问题:
(1)FeO属于
(2)“浸锰”步骤中,
 与
与 发生反应,在此过程中
发生反应,在此过程中 表现了
表现了(3)经“过滤I”后,溶液中所含金属离子为
(4)“氧化”步骤中,加入
 的作用为
的作用为(5)“沉锰”步骤中,除了生成产品
 外,还有气体生成,该反应的离子方程式为
外,还有气体生成,该反应的离子方程式为(6)取23.0g所得产品(高纯
 )溶于足量的盐酸中,共产生
)溶于足量的盐酸中,共产生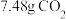 ,计算产品中碳酸锰的质量分数为
,计算产品中碳酸锰的质量分数为
更新时间:2023-12-12 21:06:44
|
【知识点】 物质分离、提纯综合应用解读
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】乙酸乙酯用途广泛,在食品加工中可作为香料原料,现利用如下方法制备和提纯。
Ⅰ.制备
在试管a中先加入3 mL CH3CH2OH,边摇动边缓缓加入2 mL浓硫酸并充分摇匀,冷却后再加入2 mL CH3CO18OH,充分混合后将试管固定在铁架台上,在试管b中加入7 mL饱和碳酸钠溶液。连接好装置,用酒精灯对试管a加热,当观察到试管b中有明显现象时停止加热。
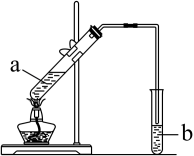
(1)该装置有一处错误,请指出:___________ 。
(2)试管a中生成乙酸乙酯的化学方程式(标记出18O的位置)为___________ 。
(3)加入浓硫酸的作用是___________ 。
Ⅱ.提纯
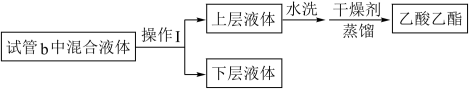
(4)操作1需用到___________ (填仪器名称)。
(5)请根据乙酸乙酯的性质选择合适的干燥剂:___________ (填字母)。
a.氯化钙 b.碱石灰 c.无水硫酸铜
(6)试管b中混合液体在振荡过程中有气泡产生,该反应的化学方程式为___________ 。
Ⅰ.制备
在试管a中先加入3 mL CH3CH2OH,边摇动边缓缓加入2 mL浓硫酸并充分摇匀,冷却后再加入2 mL CH3CO18OH,充分混合后将试管固定在铁架台上,在试管b中加入7 mL饱和碳酸钠溶液。连接好装置,用酒精灯对试管a加热,当观察到试管b中有明显现象时停止加热。

(1)该装置有一处错误,请指出:
(2)试管a中生成乙酸乙酯的化学方程式(标记出18O的位置)为
(3)加入浓硫酸的作用是
Ⅱ.提纯

(4)操作1需用到
(5)请根据乙酸乙酯的性质选择合适的干燥剂:
a.氯化钙 b.碱石灰 c.无水硫酸铜
(6)试管b中混合液体在振荡过程中有气泡产生,该反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】CuCl为白色粉末,微溶于水,溶于浓盐酸或NaCl浓溶液,不溶于乙醇。一种由海绵铜(Cu和少量CuO等)为原料制备CuCl的工艺流程如下:

(1)“溶解浸取”时,下列措施不能提高铜的浸取率的是__________ (填序号)。
a.将海绵铜粉末与水搅拌成浆液b.投料时,NaNO3适当过量
c.缩短浸取时间d.将滤渣1返回再次溶解浸取
(2)“还原,氯化”时,Na2SO3和NaCl的用量对CuCl产率的影响如图-1、图-2所示:
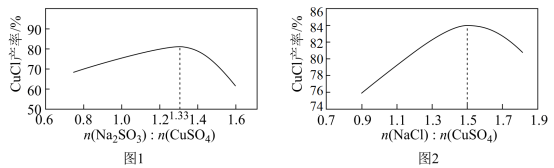
①CuSO4与Na2SO3、NaCl在溶液中反应生成CuCl的离子方程式为__________ 。
②当n(Na2SO3)/n(CuSO4)>1.33时,比值越大CuCl产率越小,其原因是__________ 。
③当1.0<n(NaCl)/n(CuSO4)<1.5时,比值越大CuCl产率越大,其原因是__________ 。
(3)“过滤2”所得滤液中溶质的主要成分为__________ (填化学式)。
(4)用“醇洗”可快速去除滤渣表面的水,防止滤渣被空气氧化为Cu2(OH)3Cl。CuCl被氧化为Cu2(OH)3Cl的化学方程式为__________ 。

(1)“溶解浸取”时,下列措施不能提高铜的浸取率的是
a.将海绵铜粉末与水搅拌成浆液b.投料时,NaNO3适当过量
c.缩短浸取时间d.将滤渣1返回再次溶解浸取
(2)“还原,氯化”时,Na2SO3和NaCl的用量对CuCl产率的影响如图-1、图-2所示:

①CuSO4与Na2SO3、NaCl在溶液中反应生成CuCl的离子方程式为
②当n(Na2SO3)/n(CuSO4)>1.33时,比值越大CuCl产率越小,其原因是
③当1.0<n(NaCl)/n(CuSO4)<1.5时,比值越大CuCl产率越大,其原因是
(3)“过滤2”所得滤液中溶质的主要成分为
(4)用“醇洗”可快速去除滤渣表面的水,防止滤渣被空气氧化为Cu2(OH)3Cl。CuCl被氧化为Cu2(OH)3Cl的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】巴蜀中学某化学兴趣实验小组的同学欲通过某氯化钠样品来获得纯净的氯化钠固体(杂质:含有 少量泥沙、Na2SO4 和碘化钠),该小组的同学设计了如下图所示的实验流程:
【查阅资料】氯气可以从碘化钠溶液中置换出碘单质。
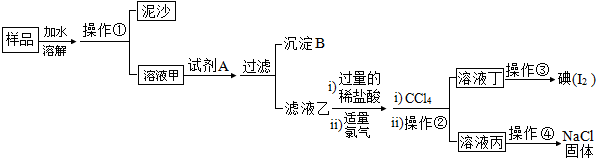
阅读上述实验流程,完成下列填空:
(1)操作①的名称_____ ;操作④的名称_____ 。
(2)在实验室进行操作②时,要用到的玻璃仪器有_____ (填仪器名称)
(3)若沉淀 B 中含有 BaSO4,由上述实验操作流程可知,A 中所包含的化学试剂有_____ (请 按加入的顺序填上相应试剂的化学式),请写出生成 BaSO4 的化学方程式_____ 。
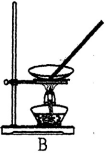
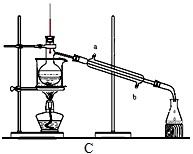
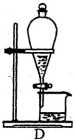
(4)操作③目的是从含碘的 CCl4 溶液中分离出单质碘和回收 CCl4,该步操作应选择的实验装置是_______ 。
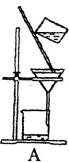
(5)如何检验所得 NaCl 固体中所含杂质 Na2SO4 已经除尽,请简述该实验操作和现象____________ 。
【查阅资料】氯气可以从碘化钠溶液中置换出碘单质。

阅读上述实验流程,完成下列填空:
(1)操作①的名称
(2)在实验室进行操作②时,要用到的玻璃仪器有
(3)若沉淀 B 中含有 BaSO4,由上述实验操作流程可知,A 中所包含的化学试剂有
(4)操作③目的是从含碘的 CCl4 溶液中分离出单质碘和回收 CCl4,该步操作应选择的实验装置是




(5)如何检验所得 NaCl 固体中所含杂质 Na2SO4 已经除尽,请简述该实验操作和现象
您最近一年使用:0次



