某小组以Ba(OH)2、水、H2SO4为实验对象探究离子反应发生的条件
(1)Ba(OH)2与H2SO4在溶液中能发生___________ 反应。
a.复分解反应 b.氧化还原反应 c.置换反应
(2)加H2O后,灯泡变亮的原因是Ba(OH)2发生了___________ 。
(3)用离子方程式解释过程Ⅰ中灯泡变暗的原因___________ 。
(4)实验2:用Na2SO4溶液替代稀H2SO4,重复实验进行对照,加入Na2SO4溶液过程中灯泡不熄灭,原因是___________ 。
通过实验1和2可知:离子反应发生的条件之一是生成沉淀。
(5)在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
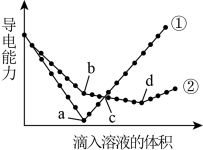
下列说法不正确的是__________
(6)食盐是日常生活的必需品,也是重要的化工原料。粗盐中食盐是日常生活的必需品,也是重要的化工原料。粗盐中常含有少量泥沙及Ca2+、Mg2+、SO 等杂质离子。为除去粗严重的Ca2+、Mg2+、SO
等杂质离子。为除去粗严重的Ca2+、Mg2+、SO 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下:
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下:
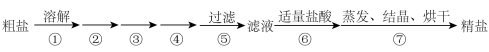
为除去Ca2+、Mg2+、SO ,步骤②~④需加入以下三种溶液(用于沉淀的试剂稍过量);加入的顺序为
,步骤②~④需加入以下三种溶液(用于沉淀的试剂稍过量);加入的顺序为___________ (填字母标号)。
A.Na2CO3 B.BaCl2
| 实验1:向烧杯中依次加入下列试剂,记录灯泡变化 | |
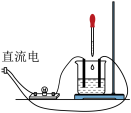 | ①Ba(OH)2粉末:灯泡不亮 ②加入蒸馏水:灯泡变亮 ③逐滴滴加0.1mol/LH2SO4,灯泡变化如下: 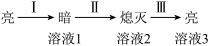 |
(1)Ba(OH)2与H2SO4在溶液中能发生
a.复分解反应 b.氧化还原反应 c.置换反应
(2)加H2O后,灯泡变亮的原因是Ba(OH)2发生了
(3)用离子方程式解释过程Ⅰ中灯泡变暗的原因
(4)实验2:用Na2SO4溶液替代稀H2SO4,重复实验进行对照,加入Na2SO4溶液过程中灯泡不熄灭,原因是
通过实验1和2可知:离子反应发生的条件之一是生成沉淀。
(5)在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。

下列说法不正确的是__________
| A.①代表滴加H2SO4溶液的变化曲线 |
| B.①代表滴加NaHSO4溶液的变化曲线 |
| C.a点对应的溶液显中性 |
| D.b点对应的溶液显中性 |
(6)食盐是日常生活的必需品,也是重要的化工原料。粗盐中食盐是日常生活的必需品,也是重要的化工原料。粗盐中常含有少量泥沙及Ca2+、Mg2+、SO
 等杂质离子。为除去粗严重的Ca2+、Mg2+、SO
等杂质离子。为除去粗严重的Ca2+、Mg2+、SO 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下:
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下:
为除去Ca2+、Mg2+、SO
 ,步骤②~④需加入以下三种溶液(用于沉淀的试剂稍过量);加入的顺序为
,步骤②~④需加入以下三种溶液(用于沉淀的试剂稍过量);加入的顺序为A.Na2CO3 B.BaCl2
更新时间:2023-12-14 12:28:30
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】一种固定烟气中CO2的工艺流程如下:

(1) “反应Ⅰ”中,CO2与过量氨水反应的离子方程式为________ 。
(2) “反应Ⅰ”中,提高烟气中CO2去除率的可行措施有________ (填字母)。
a. 采用高温 b. 加快烟气流速 c. 增大氨水浓度
(3) 若测得滤液中c(CO32-)=10-2 mol·L-1,则Ca2+是否沉淀完全?________ (填“是”或“否”)。[c(Ca2+)<10-5 mol·L-1时视为沉淀完全;Ksp(CaCO3)=4.96×10-9]
(4) “反应Ⅱ”中,溶液的pH和导电能力变化如图1所示,导电能力初始时快速降低,后来逐渐上升的原因是____________________________________________ 。

(5) CaCO3可用于调节废水的pH,以除去其中的Fe3+。溶液pH对除铁效率影响如图2所示。
①除铁时应控制溶液的pH为________ (填字母)。
a. 0.5~1.5 b. 1.5~2.5 c. 2.5~3.5
② 除铁时pH稍大会生成Fe(OH)3胶体,显著降低除铁效率,其原因是________ 。

(1) “反应Ⅰ”中,CO2与过量氨水反应的离子方程式为
(2) “反应Ⅰ”中,提高烟气中CO2去除率的可行措施有
a. 采用高温 b. 加快烟气流速 c. 增大氨水浓度
(3) 若测得滤液中c(CO32-)=10-2 mol·L-1,则Ca2+是否沉淀完全?
(4) “反应Ⅱ”中,溶液的pH和导电能力变化如图1所示,导电能力初始时快速降低,后来逐渐上升的原因是

(5) CaCO3可用于调节废水的pH,以除去其中的Fe3+。溶液pH对除铁效率影响如图2所示。
①除铁时应控制溶液的pH为
a. 0.5~1.5 b. 1.5~2.5 c. 2.5~3.5
② 除铁时pH稍大会生成Fe(OH)3胶体,显著降低除铁效率,其原因是
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐2】完成下列问题。
(1)已知25℃时,两种酸的电离平衡常数如下:
①下列四种离子结合 能力最强的是
能力最强的是________ 。
A. B.
B. C.
C. D.
D.
②请写出次氯酸钠溶液中通入少量二氧化碳的离子方程式:______ 。H3BO3的电离方程式______ ,属于______ 元______ (强/弱)酸。
(2)有c(H+)相同的盐酸、硫酸、醋酸三瓶溶液:(以下用>、<、=表示)
①设盐酸、硫酸、醋酸三种溶液的物质的量浓度依次为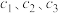 ,则其关系是
,则其关系是________ 。
②取同体积的酸的溶液分别加入足量的锌粉,反应开始放出H2的速率依次为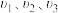 ,则其关系是
,则其关系是___________ 。
③溶液导电能力变化有以下几种
A.弱-强-弱 B.强-弱-强 C.基本不变
下列各项中与A变化趋势一致的是________ (填字母,下同),与B变化趋势一致的是______ ,与C变化趋势一致的是_________ 。
a.向Ba(OH)2溶液中滴入H2SO4溶液至过量
b.向CH3COOH溶液中滴入氨水至过量
c.向澄清石灰水中通入CO2至过量
d.向NH4Cl溶液中逐渐加入适量NaOH固体
(1)已知25℃时,两种酸的电离平衡常数如下:
| 化学式 |  |  | HClO |
 |  | 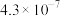 |  |
 | —— | 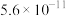 | —— |
 能力最强的是
能力最强的是A.
 B.
B. C.
C. D.
D.
②请写出次氯酸钠溶液中通入少量二氧化碳的离子方程式:
(2)有c(H+)相同的盐酸、硫酸、醋酸三瓶溶液:(以下用>、<、=表示)
①设盐酸、硫酸、醋酸三种溶液的物质的量浓度依次为
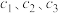 ,则其关系是
,则其关系是②取同体积的酸的溶液分别加入足量的锌粉,反应开始放出H2的速率依次为
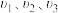 ,则其关系是
,则其关系是③溶液导电能力变化有以下几种
A.弱-强-弱 B.强-弱-强 C.基本不变
下列各项中与A变化趋势一致的是
a.向Ba(OH)2溶液中滴入H2SO4溶液至过量
b.向CH3COOH溶液中滴入氨水至过量
c.向澄清石灰水中通入CO2至过量
d.向NH4Cl溶液中逐渐加入适量NaOH固体
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】根据所学知识,回答下列问题。
(1)有以下几种物质:
① 固体②
固体② ③酒精④
③酒精④ 溶液⑤碳酸钠溶液⑥
溶液⑤碳酸钠溶液⑥ 溶液⑦
溶液⑦ ⑧
⑧ 固体⑨
固体⑨ 固体;
固体;
上述物质中,属于非电解质的是_____ (填序号,下同),属于电解质的是_____ ,可以导电的是_____ 。向上述⑤中逐滴加入⑥,写出发生反应的离子方程式:_____ 。
(2) 通常为晶体,易溶于水。写出
通常为晶体,易溶于水。写出 在熔融状态下的电离方程式:
在熔融状态下的电离方程式:_____ 。 在物质分类中属于
在物质分类中属于_____ (填字母)。
A.钠盐 B.含氧酸 C.酸式盐 D.氧化物
(3) 和
和 性质相似,均可与⑨的水溶液反应,写出
性质相似,均可与⑨的水溶液反应,写出 与⑨的水溶液反应的离子方程式:
与⑨的水溶液反应的离子方程式:_____ 。
(4)某实验小组在对(1)中某些物质进行性质探究实验后,将废液收集得到了澄清的溶液,该澄清溶液中可能含有 、
、 、
、 、
、 、
、 、
、 中的若干种,对该澄清溶液进行以下实验:
中的若干种,对该澄清溶液进行以下实验:
①用pH试纸检验,结果表明溶液呈强酸性,可以排除_____ (填离子符号,下同)的存在。
②取出部分溶液于试管中,逐滴加入 溶液,使溶液从酸性逐渐变为碱性,继续滴加
溶液,使溶液从酸性逐渐变为碱性,继续滴加 溶液,有白色沉淀生成,则可证明
溶液,有白色沉淀生成,则可证明_____ 的存在。
③取部分②中碱性溶液于试管中,滴加 溶液,有白色沉淀生成,证明
溶液,有白色沉淀生成,证明_____ 。
④综上实验分析,该澄清溶液中肯定存在的离子是_____ 。
(1)有以下几种物质:
①
 固体②
固体② ③酒精④
③酒精④ 溶液⑤碳酸钠溶液⑥
溶液⑤碳酸钠溶液⑥ 溶液⑦
溶液⑦ ⑧
⑧ 固体⑨
固体⑨ 固体;
固体;上述物质中,属于非电解质的是
(2)
 通常为晶体,易溶于水。写出
通常为晶体,易溶于水。写出 在熔融状态下的电离方程式:
在熔融状态下的电离方程式: 在物质分类中属于
在物质分类中属于A.钠盐 B.含氧酸 C.酸式盐 D.氧化物
(3)
 和
和 性质相似,均可与⑨的水溶液反应,写出
性质相似,均可与⑨的水溶液反应,写出 与⑨的水溶液反应的离子方程式:
与⑨的水溶液反应的离子方程式:(4)某实验小组在对(1)中某些物质进行性质探究实验后,将废液收集得到了澄清的溶液,该澄清溶液中可能含有
 、
、 、
、 、
、 、
、 、
、 中的若干种,对该澄清溶液进行以下实验:
中的若干种,对该澄清溶液进行以下实验:①用pH试纸检验,结果表明溶液呈强酸性,可以排除
②取出部分溶液于试管中,逐滴加入
 溶液,使溶液从酸性逐渐变为碱性,继续滴加
溶液,使溶液从酸性逐渐变为碱性,继续滴加 溶液,有白色沉淀生成,则可证明
溶液,有白色沉淀生成,则可证明③取部分②中碱性溶液于试管中,滴加
 溶液,有白色沉淀生成,证明
溶液,有白色沉淀生成,证明④综上实验分析,该澄清溶液中肯定存在的离子是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】图中A~K均为中学化学中常见的物质。A是金属单质、C为黄绿色气体单质。常温常压下C、D、F、G、K是气体,A、B、E的焰色试验同为黄色:J具有漂白作用。它们之间有如图转化关系。(反应中生成的部分产物已经略去)请回答下列问题:
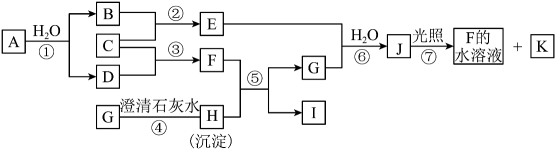
(1)E的电离方程式:
(2)气体C有毒性,不能直接排放到空气中,请写出实验室常用处理尾气C时发生的离子反应方程式
(3)图示物质A~K中,属于非电解质的为
(4)写出反应⑦的化学方程式
 气体K,转移的电子的物质的量为
气体K,转移的电子的物质的量为(5)写出反应⑤的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】27.工业上以废铜为原料经一系列化学反应可生产氯化亚铜(CuCl),其工艺流程如图所示(已知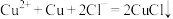 )。
)。
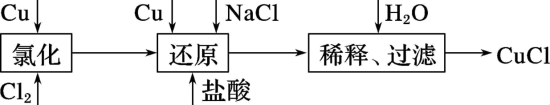
回答下列问题:
(1)氯化亚铜中铜元素的化合价为_______ 。
(2)实验室制备氯气的化学方程式为_______ ;工业生产 时,尾气常用石灰乳吸收,而不用烧碱溶液吸收的原因
时,尾气常用石灰乳吸收,而不用烧碱溶液吸收的原因_______ 。
(3)还原过程中的产物为 ,试写出该反应的化学方程式:
,试写出该反应的化学方程式:_______ 。制备中当氯化过程完成后必须经还原过程再制得CuCl,为什么不用一步法制得CuCl?_______ 。
(4)合成结束后所得产品用酒精淋洗的目的是_______ 。
(5)实验室中在 热溶液中通入
热溶液中通入 气体也可制备白色的CuCl沉淀,试写出该反应的离子方程式:
气体也可制备白色的CuCl沉淀,试写出该反应的离子方程式:_______ 。
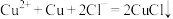 )。
)。
回答下列问题:
(1)氯化亚铜中铜元素的化合价为
(2)实验室制备氯气的化学方程式为
 时,尾气常用石灰乳吸收,而不用烧碱溶液吸收的原因
时,尾气常用石灰乳吸收,而不用烧碱溶液吸收的原因(3)还原过程中的产物为
 ,试写出该反应的化学方程式:
,试写出该反应的化学方程式:(4)合成结束后所得产品用酒精淋洗的目的是
(5)实验室中在
 热溶液中通入
热溶液中通入 气体也可制备白色的CuCl沉淀,试写出该反应的离子方程式:
气体也可制备白色的CuCl沉淀,试写出该反应的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】根据信息书写反应方程式:
(1)以 溶液为原料可以制取磁性氧化铁(
溶液为原料可以制取磁性氧化铁( ),制取流程如下:
),制取流程如下:
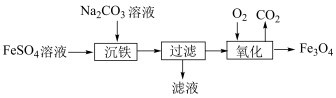
①写出沉铁时反应的离子方程式:____________ 。
②“氧化”的条件为高温。写出该反应的化学方程式:____________ 。
③ 可以溶于盐酸;写出该反应的离子方程式:
可以溶于盐酸;写出该反应的离子方程式:____________ 。
(2)漂白粉中的 在潮湿的空气中与
在潮湿的空气中与 和
和 会发生变质,变质时发生复分解反应,产物之一为
会发生变质,变质时发生复分解反应,产物之一为 。写出该反应的化学方程式:
。写出该反应的化学方程式:__________________ 。
(3)某氧化还原反应包含 、
、 、NaCl、NaClO、NaOH、
、NaCl、NaClO、NaOH、 六种物质,
六种物质, 是产物之一,写出该反应的化学方程式:
是产物之一,写出该反应的化学方程式:____________ 。
(1)以
 溶液为原料可以制取磁性氧化铁(
溶液为原料可以制取磁性氧化铁( ),制取流程如下:
),制取流程如下:
①写出沉铁时反应的离子方程式:
②“氧化”的条件为高温。写出该反应的化学方程式:
③
 可以溶于盐酸;写出该反应的离子方程式:
可以溶于盐酸;写出该反应的离子方程式:(2)漂白粉中的
 在潮湿的空气中与
在潮湿的空气中与 和
和 会发生变质,变质时发生复分解反应,产物之一为
会发生变质,变质时发生复分解反应,产物之一为 。写出该反应的化学方程式:
。写出该反应的化学方程式:(3)某氧化还原反应包含
 、
、 、NaCl、NaClO、NaOH、
、NaCl、NaClO、NaOH、 六种物质,
六种物质, 是产物之一,写出该反应的化学方程式:
是产物之一,写出该反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在,实验室里从海洋植物中提取碘的流程如下:
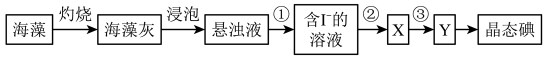
某化学兴趣小组将上述流程②③设计成如图所示实验。
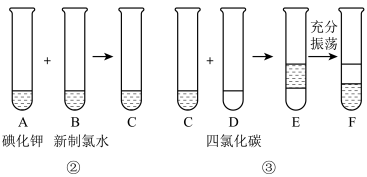
已知:②中发生反应的化学方程式为Cl2+2KI===2KCl+I2。
(1)写出提取流程中①③实验操作的名称:①__________ ,③________ 。
(2)四氯化碳是无色、密度比水大的液体。F中下层液体的颜色为________ 色,上层液体中溶质的主要成分为________ 。
(3)从F中得到碘单质还需进行的操作是________ 。

某化学兴趣小组将上述流程②③设计成如图所示实验。

已知:②中发生反应的化学方程式为Cl2+2KI===2KCl+I2。
(1)写出提取流程中①③实验操作的名称:①
(2)四氯化碳是无色、密度比水大的液体。F中下层液体的颜色为
(3)从F中得到碘单质还需进行的操作是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】金属钛是一种性能优越的结构材料和功能材料,被誉为“太空金属”。以云南富民钛铁精矿(主要成分为TiO2、FeO、Fe2O3,含SiO2、Al2O3等杂质)为原料,制备海绵状金属钛的流程设计如图:
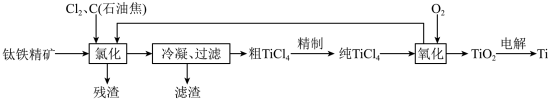
已知:TiCl4及所含杂质氯化物的性质
回答下列问题:
(1)“氯化”过程需在沸腾炉中进行,且需维持在1050℃,若TiO2氯化时生成的CO与CO2的物质的量之比为1:1,则该反应的化学方程式为_______ ;氯化产物冷却至室温,经过滤得到粗TiCl4混合液,则滤渣中含有_______ (填化学式)。
(2)“精制"过程中,粗TiC4经两步蒸馏得纯TiCl4。第一步蒸馏分离出的杂质是_______ (填化学式);再将温度控制在一定的范围内蒸馏分离出纯TiCl4,所控制温度范围是_______ 。
(3)“氧化”过程的产物中可循环利用的是_______ (填化学式)。

已知:TiCl4及所含杂质氯化物的性质
| 化合物 | SiCl4 | TiCl4 | AlCl3 | FeCl3 |
| 沸点/℃ | 58 | 136 | 181(升华) | 316 |
| 熔点/℃ | -69 | -25 | 193 | 304 |
| 在TiCl4中的溶解性 | 互溶 | —— | 微溶 | |
回答下列问题:
(1)“氯化”过程需在沸腾炉中进行,且需维持在1050℃,若TiO2氯化时生成的CO与CO2的物质的量之比为1:1,则该反应的化学方程式为
(2)“精制"过程中,粗TiC4经两步蒸馏得纯TiCl4。第一步蒸馏分离出的杂质是
(3)“氧化”过程的产物中可循环利用的是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐3】废旧锌锰干电池内部的黑色物质A主要含有MnO2、MnOOH、NH4C1、ZnCl2、碳单质,用黑色物质A制备高纯MnCO3的流程如图: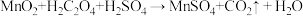 (未配平)。
(未配平)。
(1)第I步操作是为了除去可溶性的_____ (填化学式)。
(2)第I步后在空气中灼烧的目的有两个,一个是将MnOOH转化为MnO2,另一个是_____ 。灼烧时,MnOOH与空气中的氧气反应的化学方程式为_____ 。
(3)第Ⅲ步中为提高反应速率,可以采取的措施有_____ (任写一条),第Ⅲ步过程中加入H2SO4溶液的作用是_____ 。
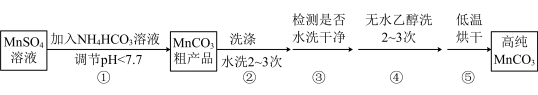
(4)已知:MnCO3难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解;Mn2+在pH大于7.7时,开始转化为Mn(OH)2沉淀。第Ⅳ步中的多步操作可按如图步骤进行:_____ ;操作②中需要的玻璃仪器有_____ ;你认为操作③中检测的方法及现象是_____ 时可继续进行操作④;操作④中用无水乙醇洗涤的目的是_____ (答一条即可)。
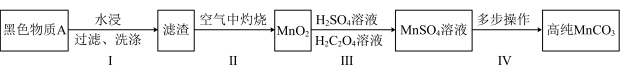
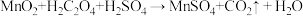 (未配平)。
(未配平)。(1)第I步操作是为了除去可溶性的
(2)第I步后在空气中灼烧的目的有两个,一个是将MnOOH转化为MnO2,另一个是
(3)第Ⅲ步中为提高反应速率,可以采取的措施有
(4)已知:MnCO3难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解;Mn2+在pH大于7.7时,开始转化为Mn(OH)2沉淀。第Ⅳ步中的多步操作可按如图步骤进行:
您最近一年使用:0次



