 标记的乙酸甲酯在足量
标记的乙酸甲酯在足量 溶液中发生水解,部分反应历程可表示为:
溶液中发生水解,部分反应历程可表示为: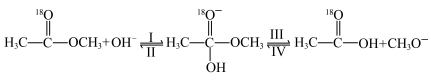 能量变化如图所示。已知
能量变化如图所示。已知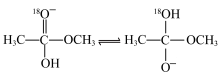 为快速平衡,下列说法正确的是
为快速平衡,下列说法正确的是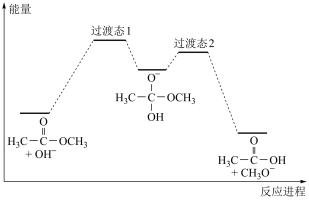
| A.反应Ⅱ、Ⅲ为决速步 |
| B.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓 |
C.反应结束后,溶液中存在 |
D.反应结束后,溶液中存在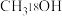 |
更新时间:2023-12-15 15:48:43
|
相似题推荐
【推荐1】相同温度和压强下,关于反应的ΔH,下列判断正确的是
ClO—(aq)+H+(aq) HClO(aq) ΔH1
HClO(aq) ΔH1
H2O(l) H+(aq)+OH—(aq) ΔH2
H+(aq)+OH—(aq) ΔH2
ClO— (aq)+H2O(l) OH—(aq)+HClO(aq) ΔH3
OH—(aq)+HClO(aq) ΔH3
ClO—(aq)+H+(aq)
 HClO(aq) ΔH1
HClO(aq) ΔH1H2O(l)
 H+(aq)+OH—(aq) ΔH2
H+(aq)+OH—(aq) ΔH2ClO— (aq)+H2O(l)
 OH—(aq)+HClO(aq) ΔH3
OH—(aq)+HClO(aq) ΔH3| A.ΔH1>0,ΔH2>0 | B.ΔH3=ΔH1+ΔH2 |
| C.ΔH1>ΔH3 | D.ΔH2<0,ΔH3>0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法中错误的是
| A.在化学反应过程中,发生物质变化的同时伴随着能量变化 |
| B.煤、石油、天然气均为化石能源,均为不可再生能源 |
| C.当生成物具有的总能量大于反应物具有的总能量时,反应吸热,△H<0 |
| D.在热化学方程式中,△H数值的大小与热化学方程式的化学计量数成正比 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某同学按图甲所示装置,探究盐酸与NaOH溶液反应的热效应,测得烧杯中溶液温度随加入a溶液的体积变化关系如图乙所示(图甲烧杯中先滴加2滴酚酞试液,溶液呈红色)。下列说法不正确 的是( )
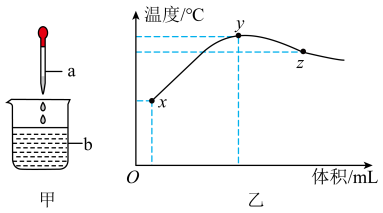

| A.随着a溶液的滴入,烧杯中溶液红色逐渐变浅直至消失 |
| B.y点对应的溶液中,溶质只有NaCl,而x、z点对应的溶液中,溶质均为两种 |
| C.利用该反应放热可以设计成原电池 |
| D.向x、z点对应溶液中分别加入铝粉,都会有气泡产生 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】CO2催化加氢合成CH4的反应为CO2(g)+4H2(g)=CH4(g)+2H2O(g) ΔH
已知:①CH4(g)+2O2(g) CO2(g)+2H2O(g) ΔH=-802.0kJ/mol
CO2(g)+2H2O(g) ΔH=-802.0kJ/mol
②CO2(g)+H2(g) CO(g)+H2O(g) ΔH=+41.2kJ/mol
CO(g)+H2O(g) ΔH=+41.2kJ/mol
③2CO(g)+O2(g) 2CO2(g) ΔH=-566.0kJ/mol
2CO2(g) ΔH=-566.0kJ/mol
下列说法中正确的是
已知:①CH4(g)+2O2(g)
 CO2(g)+2H2O(g) ΔH=-802.0kJ/mol
CO2(g)+2H2O(g) ΔH=-802.0kJ/mol②CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH=+41.2kJ/mol
CO(g)+H2O(g) ΔH=+41.2kJ/mol③2CO(g)+O2(g)
 2CO2(g) ΔH=-566.0kJ/mol
2CO2(g) ΔH=-566.0kJ/mol下列说法中正确的是
| A.CH4的燃烧热为802.0kJ/mol | B.ΔH=-165.2kJ/mol |
| C.该反应为吸热反应 | D.CO的燃烧热为566.0kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】电化学固氮可以在常温常压下实现氮气的还原合成氨,某课题组提出一种全新的电化学固氮机理——表面氢化机理,该机理的示意图如下。
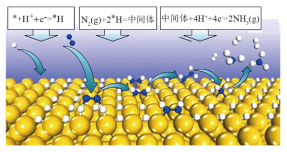
已知:吸附在催化剂表面的物种用*表示
第一步: (快)
(快)
第二步: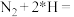 中间体(吸附在催化剂表面)(慢)
中间体(吸附在催化剂表面)(慢)
第三步:中间体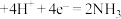 (快)
(快)
下列说法错误的是

已知:吸附在催化剂表面的物种用*表示
第一步:
 (快)
(快)第二步:
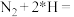 中间体(吸附在催化剂表面)(慢)
中间体(吸附在催化剂表面)(慢)第三步:中间体
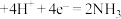 (快)
(快)下列说法错误的是
A.在表面氢化机理中,第一步是 的还原反应 的还原反应 |
| B.上述三步中第二步为决定该化学反应速率的步骤 |
C.使用催化剂可增大活化分子百分数,提高 的平衡转化率 的平衡转化率 |
D.在表面*H原子与催化剂协同作用下, 与表面*H反应生成 与表面*H反应生成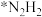 中间体 中间体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某反应的反应机理、能量与反应进程的关系如下图所示,下列说法正确的是
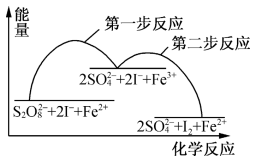

A. 是该反应的催化剂 是该反应的催化剂 |
| B.两步反应都是放热反应 |
C. 在第一步反应中作还原剂* 在第一步反应中作还原剂* |
| D.第一步反应的活化能比第二步反应的小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】为减少对环境造成的影响,发电厂试图采用以下方法将废气排放中的CO进行合理利用,以获得重要工业产品。Burns和Dainton研究发现Cl2与CO合成COCl2的反应机理如下:
①Cl2(g) 2Cl·(g) 快;
2Cl·(g) 快;
②CO(g)+Cl·(g) COCl·(g) 快;
COCl·(g) 快;
③COCl·(g)+Cl2(g) COCl2(g)+Cl·(g) 慢。
COCl2(g)+Cl·(g) 慢。
反应②的速率方程 c(CO)×c(Cl·),
c(CO)×c(Cl·), c(COCl·),
c(COCl·),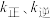 是速率常数。
是速率常数。
下列说法错误 的是
①Cl2(g)
 2Cl·(g) 快;
2Cl·(g) 快;②CO(g)+Cl·(g)
 COCl·(g) 快;
COCl·(g) 快;③COCl·(g)+Cl2(g)
 COCl2(g)+Cl·(g) 慢。
COCl2(g)+Cl·(g) 慢。反应②的速率方程
 c(CO)×c(Cl·),
c(CO)×c(Cl·), c(COCl·),
c(COCl·),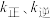 是速率常数。
是速率常数。下列说法
A.反应②的平衡常数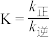 |
| B.反应①的活化能小于反应③的活化能 |
| C.要提高合成COCl2的速率,关键是提高反应③的速率 |
| D.使用合适的催化剂可以增大该反应体系中COCl2(g)的体积分数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】汽车尾气通过系统中的催化转化器可有效减少尾气中的CO、NO等向大气排放。在催化转化器中发生的反应有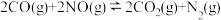 ,
, 。下列有关叙述正确的是
。下列有关叙述正确的是
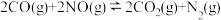 ,
, 。下列有关叙述正确的是
。下列有关叙述正确的是| A.汽车尾气中的CO和NO均来自于汽油的不完全燃烧 |
| B.升高温度时,正反应速率加快,逆反应速率减小 |
| C.使用合适的催化剂,可以改变反应路径,进而改变反应的反应热 |
D.相同条件下,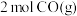 和 和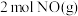 的总能量高于 的总能量高于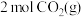 和 和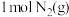 的总能量 的总能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】对于反应可逆反应:2SO2(g)+O2(g) 2SO3(g),下列说法正确的是
2SO3(g),下列说法正确的是
 2SO3(g),下列说法正确的是
2SO3(g),下列说法正确的是| A.达到平衡时SO2的消耗速率等于O2的生成速率 |
| B.使用合适的催化剂可将SO2全部转化为SO3 |
| C.2mol SO2气体和1mol O2气体的总能量大于2mol SO3气体的能量 |
| D.断开2mol SO2和1mol O2中共价键所吸收的能量大于形成2mol SO3中共价键所放出的能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】我国科学家已经成功地利用二氧化碳催化氢化获得甲酸,利用化合物1催化氢化二氧化碳的反应过程如图甲所示,其中化合物2与水反应生成化合物3和 的反应历程如图乙所示,其中TS表示过渡态,Ⅰ表示中间体。下列说法正确的是
的反应历程如图乙所示,其中TS表示过渡态,Ⅰ表示中间体。下列说法正确的是
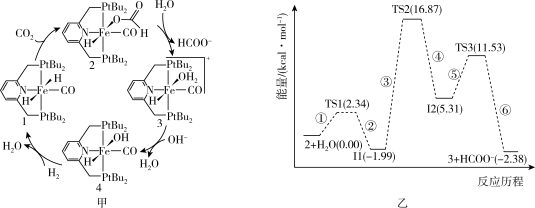
 的反应历程如图乙所示,其中TS表示过渡态,Ⅰ表示中间体。下列说法正确的是
的反应历程如图乙所示,其中TS表示过渡态,Ⅰ表示中间体。下列说法正确的是
| A.化合物2为此反应的催化剂 |
B.从平衡移动的角度看,升高温度可促进化合物2与水反应生成化合物3与 |
C.图乙中形成中间体Ⅰ2的反应为图甲中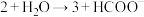 的决速步骤 的决速步骤 |
| D.化合物1到化合物2的过程中不存在极性键的断裂和形成 |
您最近一年使用:0次

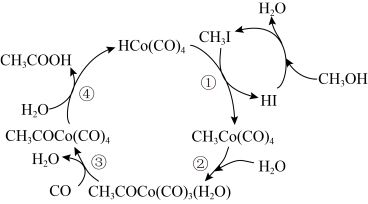
 CH3COOH
CH3COOH 2CO⑧Ba(OH)2·8H2O与固体NH4Cl混合⑨C+H2O(g)
2CO⑧Ba(OH)2·8H2O与固体NH4Cl混合⑨C+H2O(g)

