在能源绿色低碳转型行动中,天然气发挥着重要作用。管道天然气实行“应改尽改、能改全改”,预计到2025年,管道天然气普及率达到95%以上。
(1)天然气的主要成分是_______ (写电子式),该分子的空间构型是_______ 。
(2)将液化石油气(主要成分为C3H8)灶改用天然气为燃料,若进气口保持不变,则需要_______ (填“调小”或“调大”)风门。
(3)CH4在光照条件下与Cl2反应,可得到各种氯代甲烷。某小组同学查阅文献可知,CH4与Cl2反应的机理为自由基(带有单电子的原子或原子团,如·Cl、·CH3)反应,包括以下几步:
I.
Ⅱ.链传递: ,
,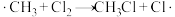 ,……
,……
Ⅲ.链终止: ,
, ……
……
为探究光照对 与
与 反应的影响,实验如下。
反应的影响,实验如下。
①由B和D得出的结论是_______ 。
②根据上述机理,解释C中几乎没有氯代甲烷的原因_______ 。
③早期的有机化合物结构理论认为,有机化合物的分子结构都是平面形的,按照这种理论丙烷_______ (填“有”或“没有”)同分异构体。
(4)丙烷氯代反应中链传递的一步反应能量变化如下。
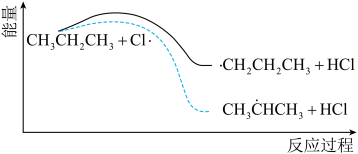
推知断裂 中1molC—H比断裂—CH2—中1molC—H所需能量
中1molC—H比断裂—CH2—中1molC—H所需能量_______ (填“大”或“小”)。
(1)天然气的主要成分是
(2)将液化石油气(主要成分为C3H8)灶改用天然气为燃料,若进气口保持不变,则需要
(3)CH4在光照条件下与Cl2反应,可得到各种氯代甲烷。某小组同学查阅文献可知,CH4与Cl2反应的机理为自由基(带有单电子的原子或原子团,如·Cl、·CH3)反应,包括以下几步:
I.

Ⅱ.链传递:
 ,
,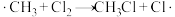 ,……
,……Ⅲ.链终止:
 ,
, ……
……为探究光照对
 与
与 反应的影响,实验如下。
反应的影响,实验如下。| 编号 | 操作 | 结果 |
| A | 将Cl2与CH4混合后,光照 | 得到氯代甲烷 |
| B | 将Cl2先用光照,然后迅速在黑暗中与CH4混合 | 得到氯代甲烷 |
| C | 将Cl2先用光照,然后在黑暗中放置一段时间,再与CH4混合 | 几乎无氯代甲烷 |
| D | 将CH4先用光照,然后迅速在黑暗中与Cl2混合 | 几乎无氯代甲烷 |
②根据上述机理,解释C中几乎没有氯代甲烷的原因
③早期的有机化合物结构理论认为,有机化合物的分子结构都是平面形的,按照这种理论丙烷
(4)丙烷氯代反应中链传递的一步反应能量变化如下。

推知断裂
 中1molC—H比断裂—CH2—中1molC—H所需能量
中1molC—H比断裂—CH2—中1molC—H所需能量
更新时间:2023-12-04 10:20:11
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】氧硫化碳(COS,结构类似于CO2)广泛存在于以煤为原料的各种化工原料气中,能引起催化剂中毒、化学产品质量下降和大气污染。有多种方法可以脱氧硫化碳中的硫,其中氢解和水解反应是两种常用的脱硫方法,其反应式分别为:
①氢解反应:COS(g) +H2(g) H2S(g) + CO(g) ΔH1= +7kJ/mol
H2S(g) + CO(g) ΔH1= +7kJ/mol
②水解反应:COS(g) +H2O(g) H2S(g) +CO2(g) ΔH2=-35kJ/mol
H2S(g) +CO2(g) ΔH2=-35kJ/mol
请回答下列问题:
(1)氧硫化碳的电子式为_____ 。
(2)CO和H2O(g)能反应生成CO2和H2,写出该反应的热化学方程式_______ 。
(3)水解反应达到平衡后,若减小容器的体积,逆反应速率将_____ (填增大、减少或不变,下同),COS的转化率____ 。
(4)某温度下,体积为2L的恒容体系中,物质的量分别为mmol、nmol的COS蒸气和H2气发生氢解,已知COS的转化率为α,则该温度下的平衡常数K=____ (用m、n、α等符号表示)。
(5)某科研小组研究改进催化剂TiO2/Al2O3和温度对COS水解的影响,得到如图

COS水解的最佳温度是________ ;理由是___________ 。
①氢解反应:COS(g) +H2(g)
 H2S(g) + CO(g) ΔH1= +7kJ/mol
H2S(g) + CO(g) ΔH1= +7kJ/mol②水解反应:COS(g) +H2O(g)
 H2S(g) +CO2(g) ΔH2=-35kJ/mol
H2S(g) +CO2(g) ΔH2=-35kJ/mol请回答下列问题:
(1)氧硫化碳的电子式为
(2)CO和H2O(g)能反应生成CO2和H2,写出该反应的热化学方程式
(3)水解反应达到平衡后,若减小容器的体积,逆反应速率将
(4)某温度下,体积为2L的恒容体系中,物质的量分别为mmol、nmol的COS蒸气和H2气发生氢解,已知COS的转化率为α,则该温度下的平衡常数K=
(5)某科研小组研究改进催化剂TiO2/Al2O3和温度对COS水解的影响,得到如图

COS水解的最佳温度是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】高炉炼铁是重要的工业过程,冶炼过程中涉及如下反应:
①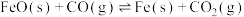
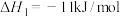
②

③
(1)反应③的
___________ kJ/mol。
(2)在恒温恒容密闭容器中投入足量石墨与 进行反应③,可判定其达到平衡的条件有___________(填序号)。
进行反应③,可判定其达到平衡的条件有___________(填序号)。
(3)反应②的压力平衡常数表达式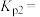
___________ 。
(4)恒容密闭容器中加入足量C、FeO,进行上述反应。改变温度,测得平衡时容器总压的对数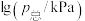 、各气体的物质的量分数
、各气体的物质的量分数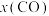 、
、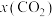 的变化如图所示:
的变化如图所示:
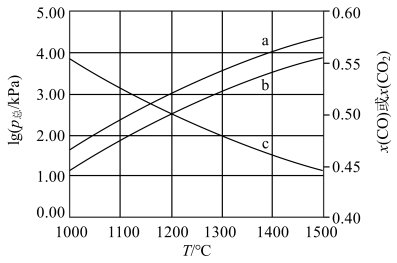
①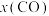 对应的曲线是
对应的曲线是___________ (填序号),判断依据是___________ 。
②在1200℃下进行上述反应,平衡时 分压为
分压为___________ kPa,反应①在此温度下的压力平衡常数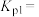
___________ 。
①
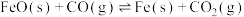
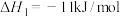
②


③

(1)反应③的

(2)在恒温恒容密闭容器中投入足量石墨与
 进行反应③,可判定其达到平衡的条件有___________(填序号)。
进行反应③,可判定其达到平衡的条件有___________(填序号)。| A.容器总压保持不变 | B.生成 ,同时生成1molCO ,同时生成1molCO |
| C.CO的体积分数保持不变 | D.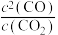 保持不变 保持不变 |
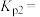
(4)恒容密闭容器中加入足量C、FeO,进行上述反应。改变温度,测得平衡时容器总压的对数
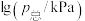 、各气体的物质的量分数
、各气体的物质的量分数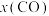 、
、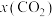 的变化如图所示:
的变化如图所示:
①
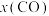 对应的曲线是
对应的曲线是②在1200℃下进行上述反应,平衡时
 分压为
分压为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物)其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。
(1)对PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如表:
根据表中数据判断PM2.5的酸碱性为_______ ,试样的pH=_______ 。
(2)为减少SO2的排放,常采取的措施是将煤转化为清洁气体燃料。已知:
H2(g)+ O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
C(s)+ O2(g)=CO(g)ΔH=-110.5kJ·mol-1
O2(g)=CO(g)ΔH=-110.5kJ·mol-1
则C(s)+H2O(g)=CO(g)+H2(g)的ΔH=________ kJ·mol-1。
(3)汽车尾气中NOx和CO的生成及转化为:
①已知气缸中生成NO的反应为:N2(g)+O2(g) 2NO(g) ΔH>0,若1mol空气含有0.8molN2和0.2molO2,1300℃时在密闭容器内反应达到平衡。测得NO为8×10-4mol,计算该温度下的平衡常数K=
2NO(g) ΔH>0,若1mol空气含有0.8molN2和0.2molO2,1300℃时在密闭容器内反应达到平衡。测得NO为8×10-4mol,计算该温度下的平衡常数K=_______ 。汽车启动后,气缸温度越高,单位时间内NO排放量越大,原因是________ 。
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g)。已知该反应的ΔH>0,简述该设想能否实现的依据:_________ 。
(1)对PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如表:
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
根据表中数据判断PM2.5的酸碱性为
(2)为减少SO2的排放,常采取的措施是将煤转化为清洁气体燃料。已知:
H2(g)+
 O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8kJ·mol-1C(s)+
 O2(g)=CO(g)ΔH=-110.5kJ·mol-1
O2(g)=CO(g)ΔH=-110.5kJ·mol-1则C(s)+H2O(g)=CO(g)+H2(g)的ΔH=
(3)汽车尾气中NOx和CO的生成及转化为:
①已知气缸中生成NO的反应为:N2(g)+O2(g)
 2NO(g) ΔH>0,若1mol空气含有0.8molN2和0.2molO2,1300℃时在密闭容器内反应达到平衡。测得NO为8×10-4mol,计算该温度下的平衡常数K=
2NO(g) ΔH>0,若1mol空气含有0.8molN2和0.2molO2,1300℃时在密闭容器内反应达到平衡。测得NO为8×10-4mol,计算该温度下的平衡常数K=②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g)。已知该反应的ΔH>0,简述该设想能否实现的依据:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】在研究化学反应中的能量变化时,我们通常做下面的实验:在一个小烧杯里,加入20克已研磨成粉末的八水合氢氧化钡,将小烧杯放在事先已滴有3-4滴水的玻璃片(或三合板)上,然后向烧杯内加入约10克氯化铵晶体,根据实验步骤,填写下表,并回答问题
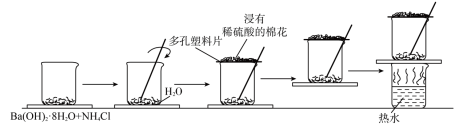
(4)写出实验过程中发生反应的化学方程式__________ 。
(5)实验中要立即用玻璃棒迅速搅拌的原因是:_________________ 。
(6)该反应在常温下就可进行,说明_________ 。

实验步骤 | 实验现象及结论 |
| 将晶体混合,立即快速搅拌 | 有刺激性气味能使湿润的紫色石蕊试纸变蓝的 |
| 用手摸烧杯下部 | 感觉烧杯变凉说明此反应是 |
| 用手拿起烧杯 | 烧杯下面的带有几滴水的玻璃片粘到了烧杯底部 |
| 将粘有玻璃片的烧杯放在盛有热水的烧杯上 | 玻璃片脱离上面烧杯底部 |
| 反应后移走多孔塑料片观察反应物 | 混合物成糊状,证明有 |
(5)实验中要立即用玻璃棒迅速搅拌的原因是:
(6)该反应在常温下就可进行,说明
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】甲醇是重要的化工原料,主要用于精细化工和制造塑料。利用二氧化碳生产甲醇实现CO2资源化,同时减少温室气体的排放。
已知:一定条件下,CO2催化加氢生产甲醇,发生如下反应:
反应i:3H2(g)+CO2(g)⇌CH3OH(g)+H2O(g) ∆H1=-49kJ·mol-1K1
反应ii:H2(g)+CO2(g)⇌CO(g)+H2O(g)△H2=+41kJ·mol-1K2
(1)反应体系中存在反应iii:CO(g)+2H2(g)⇌CH3OH(g)则∆H3=___________ kJ·mol-1;相同条件下,反应iii的平衡常数K3=___________ (用平衡常数K1、K2表示)。
(2)CO2催化加氢生产甲醇的反应历程的能量变化如下图所示(吸附在催化剂表面的物质用*标注,如*CO2表示CO2吸附在催化剂表面;图中*H已省略)。
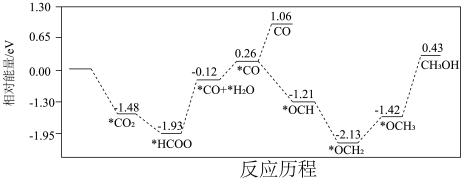
该反应历程中,决定反应速率的步骤所需的活化能为___________ eV。
(3)保持压强为aMPa,将二氧化碳和氢气按照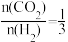 投入密闭容器中,同时发生反应i和ii,一段时间后,体系中CO2平衡转化率及甲醇产率随温度变化关系如下图所示。
投入密闭容器中,同时发生反应i和ii,一段时间后,体系中CO2平衡转化率及甲醇产率随温度变化关系如下图所示。
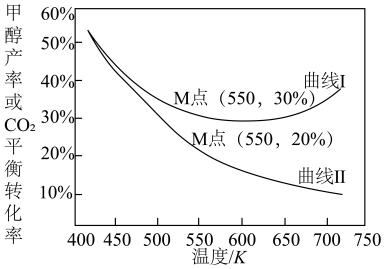
①上图中曲线I表示________ (填“CO2平衡转化率”或“甲醇产率")随温度变化的曲线,请简述理由:___________ 。
②550K时,该平衡体系中CO的物质的量为________ mol,反应i的平衡常数Kp=_______ (MPa)-2(列出计算式)。
已知:一定条件下,CO2催化加氢生产甲醇,发生如下反应:
反应i:3H2(g)+CO2(g)⇌CH3OH(g)+H2O(g) ∆H1=-49kJ·mol-1K1
反应ii:H2(g)+CO2(g)⇌CO(g)+H2O(g)△H2=+41kJ·mol-1K2
(1)反应体系中存在反应iii:CO(g)+2H2(g)⇌CH3OH(g)则∆H3=
(2)CO2催化加氢生产甲醇的反应历程的能量变化如下图所示(吸附在催化剂表面的物质用*标注,如*CO2表示CO2吸附在催化剂表面;图中*H已省略)。

该反应历程中,决定反应速率的步骤所需的活化能为
(3)保持压强为aMPa,将二氧化碳和氢气按照
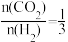 投入密闭容器中,同时发生反应i和ii,一段时间后,体系中CO2平衡转化率及甲醇产率随温度变化关系如下图所示。
投入密闭容器中,同时发生反应i和ii,一段时间后,体系中CO2平衡转化率及甲醇产率随温度变化关系如下图所示。
①上图中曲线I表示
②550K时,该平衡体系中CO的物质的量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A~I分别表示中学化学中常见的一种物质,它们之间相互关系如图所示(部分反应物、生成物没有列出)。且已知G为主族元素的固态氧化物,F是红褐色难溶于水的沉淀,A、B、C、D、E、F六种物质中均含同一种元素。
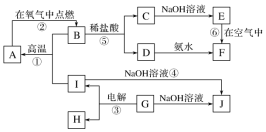
请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含同一种元素是___________ (填元素符号)。
(2)写出C、E、G物质的化学式:C___________ ,E ___________ ,G___________ 。
(3)写出④、⑥反应的化学方程式:反应④:___________ ;反应⑥:___________ 。
(4)从能量变化的角度看,①②③反应中属于吸热反应的是___________ (填序号)。

请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含同一种元素是
(2)写出C、E、G物质的化学式:C
(3)写出④、⑥反应的化学方程式:反应④:
(4)从能量变化的角度看,①②③反应中属于吸热反应的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某研究小组为了探究甲烷和氯气反应的情况,用下图装置收集一量筒甲烷和氯气的混合气体,光照一段时间后,某同学认为有氯化氢生成。回答下列问题:
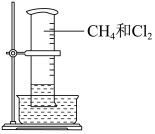
(1)写出该反应中生成氯仿的化学方程式为_______ ,反应类型为_______ (填有机反应类型)。
(2)水槽中盛放的液体最好为饱和食盐水的目的是_______ 。
(3)实验中可观察到的现象:量筒内壁上出现油状液滴,水槽中有少量固体析出,量筒内_______ 等。
(4)不考虑气态物质溶解于油状液滴,该油状液滴中含有的有机产物共有_______ 种。
(5)某烷烃的相对分子质量为72,则该烷烃的分子式为_______ 。
(6)某烷烃放入足量的氧气中燃烧,并使产生的气体全部通入如图装置,得到如表所列的实验数据(U形管中干燥剂只吸收水蒸气且假设产生的气体完全被吸收)。
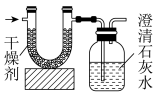
则该烷烃的分子式为_______ 。

(1)写出该反应中生成氯仿的化学方程式为
(2)水槽中盛放的液体最好为饱和食盐水的目的是
(3)实验中可观察到的现象:量筒内壁上出现油状液滴,水槽中有少量固体析出,量筒内
(4)不考虑气态物质溶解于油状液滴,该油状液滴中含有的有机产物共有
(5)某烷烃的相对分子质量为72,则该烷烃的分子式为
(6)某烷烃放入足量的氧气中燃烧,并使产生的气体全部通入如图装置,得到如表所列的实验数据(U形管中干燥剂只吸收水蒸气且假设产生的气体完全被吸收)。

| 实验前 | 实验后 | |
| (干燥剂+U形管)的质量 | 100. 0 g | 101. 8 g |
| (石灰水+广口瓶)的质量 | 312.0g | 315.3g |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】利用甲烷与氯气发生取代反应的副产品生产盐酸的设想在工业上已成为现实。某化学兴趣小组拟在实验室中模拟上述过程,所设计的装置如下图所示:
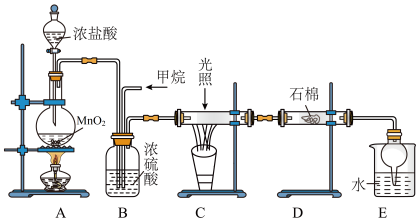
(1)A中制取Cl2反应的化学方程式是_______ 。
(2)B装置有三种功能:①控制气流速度;②均匀混合气体;③_______ 。
(3)在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,写出置换出黑色小颗粒的化学方程式:_______ 。
(4)设V(Cl2)/V(CH4)=x,若理论上欲获得最多的氯化氢,则x值为_______ 。
(5)常温常压下,1.6g甲烷完全燃烧生成二氧化碳和水放出89.03kJ热量,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H =_______ kJ·mol-1
(6)图是某种甲烷燃料电池原理示意图:
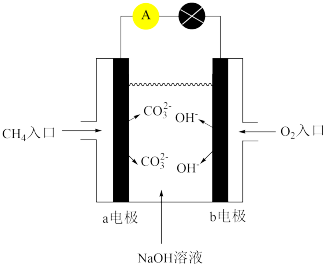
①电池的正极是_______ (填“a”或“b”)电极。
②电池工作一段时间后电解质溶液中c(OH-)_______ (填”增大”“减小”或“不变”)。

(1)A中制取Cl2反应的化学方程式是
(2)B装置有三种功能:①控制气流速度;②均匀混合气体;③
(3)在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,写出置换出黑色小颗粒的化学方程式:
(4)设V(Cl2)/V(CH4)=x,若理论上欲获得最多的氯化氢,则x值为
(5)常温常压下,1.6g甲烷完全燃烧生成二氧化碳和水放出89.03kJ热量,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H =
(6)图是某种甲烷燃料电池原理示意图:

①电池的正极是
②电池工作一段时间后电解质溶液中c(OH-)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如图:

试回答下列问题:
(1)请写出C装置中生成CH2Cl2的化学方程式:_________ 。
(2)B装置有三种功能:①混匀混合气体;②__________ ;③________ 。
(3)D装置的名称为__________ ,其作用是____________ 。
(4)将1mol CH4与Cl2发生取代反应,充分反应后生成的CH3Cl、CH2Cl2、CHCl3、CCl4四种有机产物的物质的量依次增大0.1mol,则参加反应的Cl2的物质的量为______ 。
(5)已知丁烷与氯气的取代反应的产物之一为C4H9Cl,其有______________ 种同分异构体。

试回答下列问题:
(1)请写出C装置中生成CH2Cl2的化学方程式:
(2)B装置有三种功能:①混匀混合气体;②
(3)D装置的名称为
(4)将1mol CH4与Cl2发生取代反应,充分反应后生成的CH3Cl、CH2Cl2、CHCl3、CCl4四种有机产物的物质的量依次增大0.1mol,则参加反应的Cl2的物质的量为
(5)已知丁烷与氯气的取代反应的产物之一为C4H9Cl,其有
您最近一年使用:0次



