已知:
按下图进行实验操作:
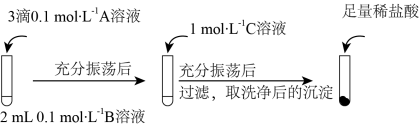
实验现象:
(1)写出 的溶度积常数表达式
的溶度积常数表达式________ 。
(2)实验Ⅰ说明 全部转化为
全部转化为 ,写出此过程的离子方程式
,写出此过程的离子方程式________ ,能说明发生此转化所依据的现象是:加入盐酸后,________ 。
物质(20℃) | BaSO4 | BaCO3 |
溶解度(g/100g水) |
|
|

实验现象:
试剂A | 试剂B | 试剂C | 加入盐酸后的现象 | |
实验Ⅰ |
|
|
| …… |
实验Ⅱ |
|
| 有少量气泡产生,沉淀部分溶解 |
(1)写出
 的溶度积常数表达式
的溶度积常数表达式(2)实验Ⅰ说明
 全部转化为
全部转化为 ,写出此过程的离子方程式
,写出此过程的离子方程式
更新时间:2023-12-21 21:45:48
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】(1)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,反应的化学方程式_____________ 漂白粉的有效成分是__________ (填化学式)。
(2)实验室制取氨气的化学方程式:__________________________________
(3)1.2gRSO4中含0.01molR2+,则RSO4的摩尔质量是______________ ;
(4)实验室制Fe(OH)2一般看不到白色的Fe(OH)2沉淀,原因___________________ 现象是:_________________________ 。反应的化学方程式:__________________________________
(5)碳酸钠水解反应的离子方程式(第一步):_________________________ 。
(6)铅蓄电池的负极反应式:_________________________ 。
(7)硫酸钡的沉淀溶解平衡:__________________________________ 。
(2)实验室制取氨气的化学方程式:
(3)1.2gRSO4中含0.01molR2+,则RSO4的摩尔质量是
(4)实验室制Fe(OH)2一般看不到白色的Fe(OH)2沉淀,原因
(5)碳酸钠水解反应的离子方程式(第一步):
(6)铅蓄电池的负极反应式:
(7)硫酸钡的沉淀溶解平衡:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】滴定是一种重要的定量实验方法:
I.酸碱中和滴定:常温下,用0.1000mol/L NaOH溶液分别滴定20.00mL等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如图所示:
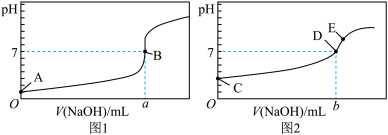
(1)滴定盐酸的曲线是图_______ (填“1”或“2”)
(2)达到B、D状态时,反应消耗的NaOH溶液的体积a_______ b(填“>”“<”或“=”)
Ⅱ.沉淀滴定法是测定粒子浓度的方法之一,为了测定某废水中SCN-的浓度,可用标准AgNO3溶液滴定待测液,已知:
(3)滴定时可选为滴定指示剂的是________ (填编号);
A.NaCl B.K2CrO4 C.KI D.NaCN
(4)如何确定该滴定过程的终点:_______ 。
(5)向 溶液中加入
溶液中加入 盐酸,生成沉淀。试求:沉淀生成后溶液中
盐酸,生成沉淀。试求:沉淀生成后溶液中 为
为_________ ,溶液的pH是_________ 。
I.酸碱中和滴定:常温下,用0.1000mol/L NaOH溶液分别滴定20.00mL等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如图所示:

(1)滴定盐酸的曲线是图
(2)达到B、D状态时,反应消耗的NaOH溶液的体积a
Ⅱ.沉淀滴定法是测定粒子浓度的方法之一,为了测定某废水中SCN-的浓度,可用标准AgNO3溶液滴定待测液,已知:
| 银盐性质 | AgCl | AgI | AgCN | Ag2CrO4 | AgSCN |
| 颜色 | 白 | 黄 | 白 | 砖红 | 白 |
| Ksp | 1.8×10-10 | 8.3×10-17 | 1.2×10-16 | 3.5×10-11 | 1.0×10-12 |
A.NaCl B.K2CrO4 C.KI D.NaCN
(4)如何确定该滴定过程的终点:
(5)向
 溶液中加入
溶液中加入 盐酸,生成沉淀。试求:沉淀生成后溶液中
盐酸,生成沉淀。试求:沉淀生成后溶液中 为
为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】镁、铝及其化合物在生产生活中具有重要的作用。
(1)下列实验能比较镁和铝的金属性强弱的是________ (填字母序号)。
a.测定镁和铝的导电性强弱
b.测定等质量的镁片和铝片与相同浓度的盐酸反应的速率
c.向0.1mol/LAlCl3和0.1mol/LMgCl2中加过量NaOH 溶液
(2)镁铝尖品石(MgAl2O4)常做耐火材料。共沉淀制备尖品石的方法是:用AICl3和MgCl2的混合溶液(用a表示)与过量的氨水(用b表示)反应,再将得到的沉淀高温焙烧。为使Mg2+、Al3+同时生成沉淀,应该把________ (填“a”或“b”)滴入另一溶液中。
(3)AlCl3与NaN3在高温下反应可制得高温结构陶瓷氮化铝(AlN),且生成N2,写出反应化学方程式为_____ 。
(4)聚合铝(PAC)是一种新型高效的无机高分子絮凝剂,广泛用于水的处理。用铝灰、铝土矿、铝渣等为原料(主要成分为Al、Al2O3可制取聚合铝。实验步骤如下:
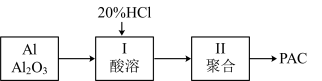
①写出酸溶过程中发生的非氧化还原反应的离子方程式:___________ 。
②聚合铝(PAC)的分子式为[Al2(OH)aCIb]m,聚合铝中OH-与Al3+的比值对净水效果有很大影响,定义盐基度B=n(OH-): 3n(Al3+),当B= 时,b=
时,b=________ 。 (填入合适数字)
③制取聚合铝的方法有多种,若将步骤Ⅰ后的溶液pH直接调制4.2-4.5时,将在过程Ⅱ发生聚合而得到某种聚合铝Alm(OH)nCl3m-n,写出生成该聚合铝的离子反应方程式是__________ 。
(1)下列实验能比较镁和铝的金属性强弱的是
a.测定镁和铝的导电性强弱
b.测定等质量的镁片和铝片与相同浓度的盐酸反应的速率
c.向0.1mol/LAlCl3和0.1mol/LMgCl2中加过量NaOH 溶液
(2)镁铝尖品石(MgAl2O4)常做耐火材料。共沉淀制备尖品石的方法是:用AICl3和MgCl2的混合溶液(用a表示)与过量的氨水(用b表示)反应,再将得到的沉淀高温焙烧。为使Mg2+、Al3+同时生成沉淀,应该把
(3)AlCl3与NaN3在高温下反应可制得高温结构陶瓷氮化铝(AlN),且生成N2,写出反应化学方程式为
(4)聚合铝(PAC)是一种新型高效的无机高分子絮凝剂,广泛用于水的处理。用铝灰、铝土矿、铝渣等为原料(主要成分为Al、Al2O3可制取聚合铝。实验步骤如下:

①写出酸溶过程中发生的非氧化还原反应的离子方程式:
②聚合铝(PAC)的分子式为[Al2(OH)aCIb]m,聚合铝中OH-与Al3+的比值对净水效果有很大影响,定义盐基度B=n(OH-): 3n(Al3+),当B=
 时,b=
时,b=③制取聚合铝的方法有多种,若将步骤Ⅰ后的溶液pH直接调制4.2-4.5时,将在过程Ⅱ发生聚合而得到某种聚合铝Alm(OH)nCl3m-n,写出生成该聚合铝的离子反应方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】大苏打(Na2S2O3·5H2O)、苏打、小苏打被称为“苏氏三兄弟”,它们在生活、生产中有广泛应用。
(1)工业上制备苏打是先制备小苏打,写出我国伟大化学家侯德榜提出的制备小苏打的化学方程式___ ,操作时,往饱和食盐水中先通入气体,先制备小苏打的原因是___ 。
(2)Na2S2O3标准溶液常用于滴定碘的含量,若滴定的溶液呈酸性,测定结果会偏高,用离子方程式表示其原因__ 。
(3)工业上,常用纯碱和盐酸除去锅炉中硫酸钙。先用饱和纯碱溶液浸泡锅垢,然后用盐酸清洗。“浸泡”的目的是__ 。
(4)工业上,将Na2CO3和Na2S以1:2的物质的量之比配成溶液,再通入SO2,可制取Na2S2O3,同时放出CO2。写出该反应的化学方程式__ 。Na2S溶液在空气中久置,会生成浅黄色物质,经测定该物质具有与过氧化钠相似的结构,该物质的化学式为__ 。
(5)在密闭容器中投入一定量的Na2O2和NaHCO3,在300℃下充分反应。若残留固体为纯净物,则起始时 满足的条件是
满足的条件是__ 。
(1)工业上制备苏打是先制备小苏打,写出我国伟大化学家侯德榜提出的制备小苏打的化学方程式
(2)Na2S2O3标准溶液常用于滴定碘的含量,若滴定的溶液呈酸性,测定结果会偏高,用离子方程式表示其原因
(3)工业上,常用纯碱和盐酸除去锅炉中硫酸钙。先用饱和纯碱溶液浸泡锅垢,然后用盐酸清洗。“浸泡”的目的是
(4)工业上,将Na2CO3和Na2S以1:2的物质的量之比配成溶液,再通入SO2,可制取Na2S2O3,同时放出CO2。写出该反应的化学方程式
(5)在密闭容器中投入一定量的Na2O2和NaHCO3,在300℃下充分反应。若残留固体为纯净物,则起始时
 满足的条件是
满足的条件是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】牙齿表面由一层坚硬的、组成为Ca5(PO4)3OH的物质保护着,它在唾液中存在着如下平衡:Ca5(PO4)3OH(固)⇌5Ca2++3PO +OH-。
+OH-。
(1)进食后,细菌和酶作用于食物,产生有机酸,此时,牙齿就会受到腐蚀,其原因是_______ 。
(2)已知Ca5(PO4)3F(s)的溶解度比上面的矿化产物更小,质地更坚固。请用离子方程式表示牙膏配有氟化物添加剂能防止龋齿的原因:___________ 。
(3)根据以上原理,请你提出一种其它促进矿化的方法:__________ 。
 +OH-。
+OH-。(1)进食后,细菌和酶作用于食物,产生有机酸,此时,牙齿就会受到腐蚀,其原因是
(2)已知Ca5(PO4)3F(s)的溶解度比上面的矿化产物更小,质地更坚固。请用离子方程式表示牙膏配有氟化物添加剂能防止龋齿的原因:
(3)根据以上原理,请你提出一种其它促进矿化的方法:
您最近一年使用:0次
【推荐3】完成下列填空
| 序号 | 实验 | 现象 | 解释与结论 | 正误 |
| 1 | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有 无 无 | |
| 2 | 滴加几滴稀 溶液,将湿润红色石蕊试纸置于试管口 溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无 | |
| 3 | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点较低 | |
| 4 | 硝酸银溶液中加入足量 溶液,再加入 溶液,再加入 溶液 溶液 | 先出现白色沉淀,后变为黄色沉淀 | 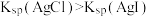 | |
| 5 |  溶液中加4~6滴 溶液中加4~6滴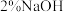 溶液,振荡后加入 溶液,振荡后加入 溶液,加热煮沸 溶液,加热煮沸 | 未出现红色沉淀 | X不含有醛基 | |
| 6 | 等体积 的 的 和 和 两种酸分别与足量的锌反应 两种酸分别与足量的锌反应 | 相同时间内, 收集到的氢气多 收集到的氢气多 |  是强酸 是强酸 | |
| 7 | 将铝片和镁条作为电极,插入 的 的 溶液中 溶液中 | 电流表指针偏向镁片 | 金属铝比镁活泼 | |
| 8 | 向 的 的 溶液中滴加2滴甲基橙 溶液中滴加2滴甲基橙 | 溶液呈黄色 |  溶液呈碱性 溶液呈碱性 | |
| 9 | 向 溶液中加入氯水,再加入淀粉 溶液中加入氯水,再加入淀粉 溶液 溶液 | 溶液变蓝 | 氧化性: | |
| 10 | 将浓硫酸滴到蔗糖表面 | 固体变黑膨胀 | 浓硫酸有脱水性和强氧化性 | |
| 11 | 配制 溶液 溶液 | 将 固体溶解于适量硫酸溶液 固体溶解于适量硫酸溶液 |  抑制 抑制 水解 水解 | |
| 12 | 常温下,相同的铝片分别投入足量的稀、浓硫酸中 | 浓硫酸中铝片先溶解完 | 反应物浓度越大,反应速率越快 | |
| 13 | 向 溶液中通入 溶液中通入 体 体 | 有黑色沉淀 |  不溶于稀硫酸 不溶于稀硫酸 | |
| 14 | 在 溶液中加入 溶液中加入 溶液,再加入苯,振荡 溶液,再加入苯,振荡 | 有白色沉淀生成,苯层呈紫色 | 白色沉淀可能为 | |
| 15 | 向硝酸亚铁溶液中滴入稀硫酸 | 无明显现象 | 硝酸亚铁与硫酸不反应 | |
| 16 | 常温下,用 试纸测定一定浓度的 试纸测定一定浓度的 溶液的 溶液的 | 比对后,测得 |  的水解程度小于其电离程度 的水解程度小于其电离程度 | |
| 17 | 向一定量的浓硫酸中加入过量的锌粒,微热至反应结束 | 产生气泡 | 该气体成分仅为 | |
| 18 | 将澄清石灰水滴入可能混有 的 的 溶液中 溶液中 | 有白色沉淀产生 | 该溶液中一定含有 | |
| 19 | 表面变黑的银器浸泡到盛有食盐水的铝制容器中,银器与铝接触 | 银器变得光亮如新 | 构成原电池,铝作负极,硫化银得电子被还原成单质银 | |
| 20 | 向足量的浓硝酸中加入铁片,一段时间后加入铜粉 | 有气体生成,溶液呈蓝绿色 | 浓硝酸将 氧化成 氧化成 ,生成 ,生成 , , 与 与 反应生成 反应生成 |
您最近一年使用:0次








