无水四氯化锡( )常用作媒染剂和部分有机合成的催化剂。某化学兴趣小组利用如图装置(部分加热装置略)制备
)常用作媒染剂和部分有机合成的催化剂。某化学兴趣小组利用如图装置(部分加热装置略)制备 并测定产品中
并测定产品中 含量。
含量。 熔点为-33℃,沸点为114.1℃,在潮湿空气中极易潮解(水解生成
熔点为-33℃,沸点为114.1℃,在潮湿空气中极易潮解(水解生成 ),且熔融Sn与
),且熔融Sn与 反应生成
反应生成 时放出大量的热。
时放出大量的热。
②Sn熔点为232℃,无水 熔点为246℃、沸点为652℃。
熔点为246℃、沸点为652℃。
回答下列问题:
(1)a管的作用是___________ 。
(2)装置B、C中的试剂分别为___________ 、___________ (填名称)。
(3)为了获得较纯的产品,当D处具支试管中___________ 时,再点燃D处酒精灯。反应制得的产品中可能会含有杂质 ,为加快反应速率并防止产品中混有
,为加快反应速率并防止产品中混有 ,除了通入过量
,除了通入过量 外,还应控制反应的最佳温度范围为
外,还应控制反应的最佳温度范围为___________ 。
(4)甲同学欲证明装置A产生的气体中含有HCl,设计如图装置进行实验。___________ 。
(5)碘氧化法滴定分析产品中 的含量。准确称取ag产品于锥形瓶中,用蒸馏水溶解,淀粉溶液做指示剂,用b
的含量。准确称取ag产品于锥形瓶中,用蒸馏水溶解,淀粉溶液做指示剂,用b  碘标准溶液滴定,发生反应:
碘标准溶液滴定,发生反应: 。滴定终点消耗碘标准溶液V mL,则产品中
。滴定终点消耗碘标准溶液V mL,则产品中 的质量分数为
的质量分数为___________ (用含a、b、V的代数式表示)。
 )常用作媒染剂和部分有机合成的催化剂。某化学兴趣小组利用如图装置(部分加热装置略)制备
)常用作媒染剂和部分有机合成的催化剂。某化学兴趣小组利用如图装置(部分加热装置略)制备 并测定产品中
并测定产品中 含量。
含量。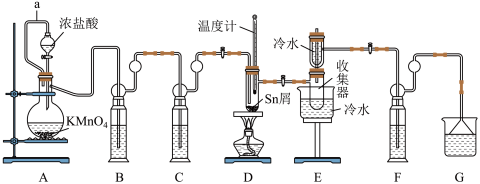
 熔点为-33℃,沸点为114.1℃,在潮湿空气中极易潮解(水解生成
熔点为-33℃,沸点为114.1℃,在潮湿空气中极易潮解(水解生成 ),且熔融Sn与
),且熔融Sn与 反应生成
反应生成 时放出大量的热。
时放出大量的热。②Sn熔点为232℃,无水
 熔点为246℃、沸点为652℃。
熔点为246℃、沸点为652℃。回答下列问题:
(1)a管的作用是
(2)装置B、C中的试剂分别为
(3)为了获得较纯的产品,当D处具支试管中
 ,为加快反应速率并防止产品中混有
,为加快反应速率并防止产品中混有 ,除了通入过量
,除了通入过量 外,还应控制反应的最佳温度范围为
外,还应控制反应的最佳温度范围为(4)甲同学欲证明装置A产生的气体中含有HCl,设计如图装置进行实验。

(5)碘氧化法滴定分析产品中
 的含量。准确称取ag产品于锥形瓶中,用蒸馏水溶解,淀粉溶液做指示剂,用b
的含量。准确称取ag产品于锥形瓶中,用蒸馏水溶解,淀粉溶液做指示剂,用b  碘标准溶液滴定,发生反应:
碘标准溶液滴定,发生反应: 。滴定终点消耗碘标准溶液V mL,则产品中
。滴定终点消耗碘标准溶液V mL,则产品中 的质量分数为
的质量分数为
更新时间:2023-12-05 22:08:56
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】AlCl3是一种催化剂,某校学习小组用下面装置制备少量AlCl3。已知:AlCl3遇到空气中的水蒸气时能剧烈反应生成Al(OH)3和HCl;AlCl3在180℃时升华,根据要求完成下列问题:

(1)a仪器的名称为_______ ;A装置中反应的化学方程式为_______ 。
(2)试剂b为_______ ;C装置的作用为_______ 。
(3)所用d导管较粗的原因是_______ ;E装置的作用为_______ 。
(4)F装置的作用为_______ 。
(5)若上图中的D、E装置改为下面装置,D装置中的现象为_______ ;用离子方程式表示E中的现象变化_______ 。


(1)a仪器的名称为
(2)试剂b为
(3)所用d导管较粗的原因是
(4)F装置的作用为
(5)若上图中的D、E装置改为下面装置,D装置中的现象为

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】硫酰氯(SO2Cl2)是一种化工原料,有如下有关信息:常温下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中“发烟”;100℃以上开始分解,生成二氧化硫和氯气。氯化法是合成硫酰氯的常用方法,实验室合成反应和实验装置如图:
SO2(g)+Cl2(g) SO2Cl2 △H=-97.3kJ/mol
SO2Cl2 △H=-97.3kJ/mol
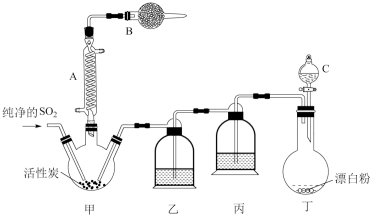
回答下列问题:
(1)仪器A的名称为___ ,甲中活性炭的作用是___ ,B中加入的药品是___ 。
(2)装置丁中发生反应的离子方程式为____ 。用亚硫酸钠固体和浓硫酸制备二氧化硫气体时,如要控制反应速度,图中可选用的发生装置是___ (填写字母)。
a.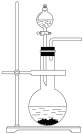 b.
b.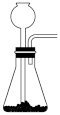 c.
c.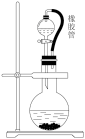 d.
d. 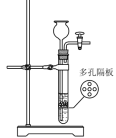
(3)氯磺酸(C1SO3H)加热分解,也能制得硫酰氯与另外一种物质,该反应的化学方程式为___ ,分离产物的方法是___ 。
(4)若缺少装置乙,氯气和二氧化硫可能发生反应的化学方程式为___ 。
SO2(g)+Cl2(g)
 SO2Cl2 △H=-97.3kJ/mol
SO2Cl2 △H=-97.3kJ/mol
回答下列问题:
(1)仪器A的名称为
(2)装置丁中发生反应的离子方程式为
a.
 b.
b. c.
c. d.
d. 
(3)氯磺酸(C1SO3H)加热分解,也能制得硫酰氯与另外一种物质,该反应的化学方程式为
(4)若缺少装置乙,氯气和二氧化硫可能发生反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】硫脲 在药物制备、金属矿物浮选等方面有广泛应用。实验室中先制备
在药物制备、金属矿物浮选等方面有广泛应用。实验室中先制备 ,再与
,再与 合成
合成 ,实验装置(夹持及加热装置略)如图所示。
,实验装置(夹持及加热装置略)如图所示。

已知: 易溶于水,易被氧化,受热时部分发生异构化生成
易溶于水,易被氧化,受热时部分发生异构化生成 。
。
(1)实验前先检查装置气密性,操作为:
①在E中加水至浸没导管末端,…;
②微热A处三颈烧瓶,观察到E处导管末端有气泡冒出,移走酒精灯;
③一段时间后,E处导管末端形成一段水柱,且高度不变。
将操作①补充完整___________ 。
(2)检查气密性后加入药品,打开 。装置B中盛装的试剂为
。装置B中盛装的试剂为___________ 。反应结束后关闭 ,打开
,打开 通
通 一段时间,目的是
一段时间,目的是___________ 。
(3)撤走搅拌器,打开 ,水浴加热D中三颈烧瓶,在80℃时合成硫脲,同时生成一种常见的碱。控制温度在80℃的原因是
,水浴加热D中三颈烧瓶,在80℃时合成硫脲,同时生成一种常见的碱。控制温度在80℃的原因是___________ ,D处合成硫脲的化学方程式为___________ 。
(4)将装置D中的液体过滤后,结晶得到粗产品。
①称取m g产品,加水溶解配成500mL溶液。在锥形瓶中加入足量氢氧化钠溶液和 单质碘,发生反应:
单质碘,发生反应: ,量取25mL硫脲溶液加入锥形瓶,发生反应:
,量取25mL硫脲溶液加入锥形瓶,发生反应: ;
;
②充分反应后加稀硫酸至酸性,发生反应: ,滴加两滴淀粉溶液,用
,滴加两滴淀粉溶液,用
 标准溶液滴定,发生反应:
标准溶液滴定,发生反应: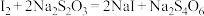 。至终点时消耗标准溶液V mL。
。至终点时消耗标准溶液V mL。
粗产品中硫脲的质量分数:为___________ (用含“m、n、c、V”的式子表示)
已知: 。
。
 在药物制备、金属矿物浮选等方面有广泛应用。实验室中先制备
在药物制备、金属矿物浮选等方面有广泛应用。实验室中先制备 ,再与
,再与 合成
合成 ,实验装置(夹持及加热装置略)如图所示。
,实验装置(夹持及加热装置略)如图所示。
已知:
 易溶于水,易被氧化,受热时部分发生异构化生成
易溶于水,易被氧化,受热时部分发生异构化生成 。
。(1)实验前先检查装置气密性,操作为:
①在E中加水至浸没导管末端,…;
②微热A处三颈烧瓶,观察到E处导管末端有气泡冒出,移走酒精灯;
③一段时间后,E处导管末端形成一段水柱,且高度不变。
将操作①补充完整
(2)检查气密性后加入药品,打开
 。装置B中盛装的试剂为
。装置B中盛装的试剂为 ,打开
,打开 通
通 一段时间,目的是
一段时间,目的是(3)撤走搅拌器,打开
 ,水浴加热D中三颈烧瓶,在80℃时合成硫脲,同时生成一种常见的碱。控制温度在80℃的原因是
,水浴加热D中三颈烧瓶,在80℃时合成硫脲,同时生成一种常见的碱。控制温度在80℃的原因是(4)将装置D中的液体过滤后,结晶得到粗产品。
①称取m g产品,加水溶解配成500mL溶液。在锥形瓶中加入足量氢氧化钠溶液和
 单质碘,发生反应:
单质碘,发生反应: ,量取25mL硫脲溶液加入锥形瓶,发生反应:
,量取25mL硫脲溶液加入锥形瓶,发生反应: ;
;②充分反应后加稀硫酸至酸性,发生反应:
 ,滴加两滴淀粉溶液,用
,滴加两滴淀粉溶液,用
 标准溶液滴定,发生反应:
标准溶液滴定,发生反应: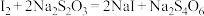 。至终点时消耗标准溶液V mL。
。至终点时消耗标准溶液V mL。粗产品中硫脲的质量分数:为
已知:
 。
。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】过氧化钙常用作杀菌剂及封闭胶泥的快干剂,难溶于水,溶于酸生成过氧化氢。以大理石(含有少量氧化亚铁和氧化铁杂质)为原料制备过氧化钙的工艺流程如图所示。

回答下列问题:
(1)操作Ⅰ的目的是调节溶液的 ,使铁元素完全沉淀,则试剂A最好选用
,使铁元素完全沉淀,则试剂A最好选用_______ (填标号)。
a.盐酸 b.硝酸 c.盐酸和过氧化氢 d.硫酸
(2)测得滤液M中 的物质的量浓度为
的物质的量浓度为 ,若加入等体积的
,若加入等体积的 溶液时
溶液时 开始沉淀,则
开始沉淀,则 的物质的量浓度为
的物质的量浓度为_______ 【已知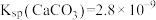 】。
】。
(3)反应Ⅰ是放热反应.不同浓度的 溶液对反应生成
溶液对反应生成 产率的影响如下表:
产率的影响如下表:
分析题给信息,解释 的浓度大于20%后
的浓度大于20%后 产率反而减小的原因:
产率反而减小的原因:_______ 。
(4)制备所得的过氧化钙中常含有 杂质,实验室可按以下步骤测定
杂质,实验室可按以下步骤测定 的质量分数:
的质量分数:
步骤1:准确称取 过氧化钙样品,置于
过氧化钙样品,置于 的锥形瓶中;
的锥形瓶中;
步骤2:加入 蒸馏水和
蒸馏水和 磷酸,振荡使样品完全溶解;
磷酸,振荡使样品完全溶解;
步骤3:用 的酸性
的酸性 溶液滴定至终点,记录数据;
溶液滴定至终点,记录数据;
步骤4:平行测定3次(数据记录见下表),计算试样中 的质量分数。
的质量分数。
已知:上述实验过程中反应关系为 ,
, 。
。
①步骤3判断滴定达到终点的现象是_______ 。
②由表中数据可知,该样品中 的质量分数为
的质量分数为_______ %。若实验时刚洗净的滴定管未用酸性 溶液润洗,则测定的
溶液润洗,则测定的 的质量分数会
的质量分数会_______ (填“偏高”“偏低”或“无影响”)。

回答下列问题:
(1)操作Ⅰ的目的是调节溶液的
 ,使铁元素完全沉淀,则试剂A最好选用
,使铁元素完全沉淀,则试剂A最好选用a.盐酸 b.硝酸 c.盐酸和过氧化氢 d.硫酸
(2)测得滤液M中
 的物质的量浓度为
的物质的量浓度为 ,若加入等体积的
,若加入等体积的 溶液时
溶液时 开始沉淀,则
开始沉淀,则 的物质的量浓度为
的物质的量浓度为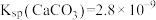 】。
】。(3)反应Ⅰ是放热反应.不同浓度的
 溶液对反应生成
溶液对反应生成 产率的影响如下表:
产率的影响如下表: 的浓度/% 的浓度/% | 5 | 10 | 15 | 20 | 25 | 30 |
 的产率/% 的产率/% | 62.40 | 63.10 | 63.20 | 64.54 | 62.42 | 60.40 |
 的浓度大于20%后
的浓度大于20%后 产率反而减小的原因:
产率反而减小的原因:(4)制备所得的过氧化钙中常含有
 杂质,实验室可按以下步骤测定
杂质,实验室可按以下步骤测定 的质量分数:
的质量分数:步骤1:准确称取
 过氧化钙样品,置于
过氧化钙样品,置于 的锥形瓶中;
的锥形瓶中;步骤2:加入
 蒸馏水和
蒸馏水和 磷酸,振荡使样品完全溶解;
磷酸,振荡使样品完全溶解;步骤3:用
 的酸性
的酸性 溶液滴定至终点,记录数据;
溶液滴定至终点,记录数据;步骤4:平行测定3次(数据记录见下表),计算试样中
 的质量分数。
的质量分数。| 实验 | 1 | 2 | 3 |
V(酸性 溶液)/mL 溶液)/mL | 19.50 | 19.48 | 19.52 |
 ,
, 。
。①步骤3判断滴定达到终点的现象是
②由表中数据可知,该样品中
 的质量分数为
的质量分数为 溶液润洗,则测定的
溶液润洗,则测定的 的质量分数会
的质量分数会
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某化学课外小组为测定空气中CO2的含量,进行了如下实验:
①配制0.1000 mol/L 和0.01000 mol/L的标准盐酸。
②将2~3滴酚酞加入未知浓度的Ba(OH)2溶液10.00 mL中,并用0.1000 mol/L的标准盐酸进行滴定,结果用去盐酸19.60 mL。
③用测定的Ba(OH)2溶液吸收定量空气中的CO2。取Ba(OH)2溶液10.00 mL,放入100 mL容量瓶里加水至刻度线,取出稀释后的溶液放入密闭容器内,并通入10 L标准状况下的空气,振荡,这时生成沉淀。
④过滤上述所得浊液。
⑤取滤液20.00 mL,用0.01000 mol/L的盐酸滴定,用去盐酸34.80 mL。
请回答下列问题:
(1)配制标准盐酸时,需用下列哪些仪器?_____________________ 。
A.托盘天平 B.容量瓶 C.酸式滴定管 D.量筒 E.烧杯 F.胶头滴管 G.玻璃棒
(2)②操作中到达滴定终点时的现象是___________________________________________ 。
(3)Ba(OH)2溶液的物质的量浓度是________ 。
(4)此空气样品中含CO2的体积分数为________ 。
(5)本实验中,若第一次滴定时使用的酸式滴定管未经处理,即注入第二种标准盐酸,并进行第二次滴定,使测定结果________ (填“偏大”“偏小”或“无影响”)。
(6)在第一次滴定的时候未润洗滴定管,会使测定结果_______ (填“偏大”“偏小”或“无影响”)。
①配制0.1000 mol/L 和0.01000 mol/L的标准盐酸。
②将2~3滴酚酞加入未知浓度的Ba(OH)2溶液10.00 mL中,并用0.1000 mol/L的标准盐酸进行滴定,结果用去盐酸19.60 mL。
③用测定的Ba(OH)2溶液吸收定量空气中的CO2。取Ba(OH)2溶液10.00 mL,放入100 mL容量瓶里加水至刻度线,取出稀释后的溶液放入密闭容器内,并通入10 L标准状况下的空气,振荡,这时生成沉淀。
④过滤上述所得浊液。
⑤取滤液20.00 mL,用0.01000 mol/L的盐酸滴定,用去盐酸34.80 mL。
请回答下列问题:
(1)配制标准盐酸时,需用下列哪些仪器?
A.托盘天平 B.容量瓶 C.酸式滴定管 D.量筒 E.烧杯 F.胶头滴管 G.玻璃棒
(2)②操作中到达滴定终点时的现象是
(3)Ba(OH)2溶液的物质的量浓度是
(4)此空气样品中含CO2的体积分数为
(5)本实验中,若第一次滴定时使用的酸式滴定管未经处理,即注入第二种标准盐酸,并进行第二次滴定,使测定结果
(6)在第一次滴定的时候未润洗滴定管,会使测定结果
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】1,2-二氯乙烷(CH2ClCH2Cl,M=99g/mol)是重要的有机化工原料,实验室采用“乙烯液相直接氯化法”制备 1,2-二氯乙烷(该液相体系以预装的1,2-二氯乙烷作为溶剂),相关反应原理和实验装置图如图:  CH2=CH2↑+H2O;
CH2=CH2↑+H2O;
②Cl2(g)+CH2=CH2(g)→CH2ClCH2Cl(l) <0;
<0;
③1,2-二氯乙烷不溶于水,易溶于有机溶剂,沸点为83.5℃。
回答下列问题:
(1)仪器 B 的名称是___________ ,装置甲中橡皮管的作用是___________ 。
(2)甲装置中发生的化学反应方程式为___________ 。
(3)制取 1,2-二氯乙烷的装置接口顺序为___________ (箭头为气流方向,部分装置可重复使用)。
a→___________→___________→___________→___________→b-c←f←e←i←j←d
(4)乙装置中多孔球泡的作用是___________ 。
(5)己装置所加入的试剂为___________ 。
(6)产品纯度的测定:量取 5.5mL 逐出 Cl2 和乙烯后的产品,产品密度为 1.2g/mL,加足量稀NaOH溶液,加热充分反应:CH2ClCH2Cl+2NaOH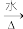 CH2OHCH2OH+2NaCl (其他杂质不参与反应)。所得溶液先用稀硝酸中和至酸性,然后加入 1.0000 mol/L 的 AgNO3 标准溶液至不再产生沉淀,沉降后过滤、洗涤、低温干燥、称量,得到14.35g白色固体,则产品中1,2-二氯乙烷的纯度为
CH2OHCH2OH+2NaCl (其他杂质不参与反应)。所得溶液先用稀硝酸中和至酸性,然后加入 1.0000 mol/L 的 AgNO3 标准溶液至不再产生沉淀,沉降后过滤、洗涤、低温干燥、称量,得到14.35g白色固体,则产品中1,2-二氯乙烷的纯度为___________ %。

 CH2=CH2↑+H2O;
CH2=CH2↑+H2O;②Cl2(g)+CH2=CH2(g)→CH2ClCH2Cl(l)
 <0;
<0;③1,2-二氯乙烷不溶于水,易溶于有机溶剂,沸点为83.5℃。
回答下列问题:
(1)仪器 B 的名称是
(2)甲装置中发生的化学反应方程式为
(3)制取 1,2-二氯乙烷的装置接口顺序为
a→___________→___________→___________→___________→b-c←f←e←i←j←d
(4)乙装置中多孔球泡的作用是
(5)己装置所加入的试剂为
(6)产品纯度的测定:量取 5.5mL 逐出 Cl2 和乙烯后的产品,产品密度为 1.2g/mL,加足量稀NaOH溶液,加热充分反应:CH2ClCH2Cl+2NaOH
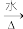 CH2OHCH2OH+2NaCl (其他杂质不参与反应)。所得溶液先用稀硝酸中和至酸性,然后加入 1.0000 mol/L 的 AgNO3 标准溶液至不再产生沉淀,沉降后过滤、洗涤、低温干燥、称量,得到14.35g白色固体,则产品中1,2-二氯乙烷的纯度为
CH2OHCH2OH+2NaCl (其他杂质不参与反应)。所得溶液先用稀硝酸中和至酸性,然后加入 1.0000 mol/L 的 AgNO3 标准溶液至不再产生沉淀,沉降后过滤、洗涤、低温干燥、称量,得到14.35g白色固体,则产品中1,2-二氯乙烷的纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】氨基甲酸铵(H2NCOONH4)是一种易分解、易水解的白色固体,可用于化肥、灭火剂、洗涤剂等。某研究小组用下图所示的实验装置,利用氢氧化钠固体、浓氨水、干冰等作原料制备氨基甲酸铵。主要反应原理:2NH3(g) + CO2(g)=H2NCOONH4(s) ΔH<0。
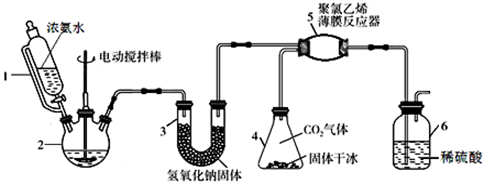
(1)实验室用98%的浓硫酸配制15%的稀硫酸,除量筒外还需使用下列仪器中的____ 。
a.烧杯b.一定容积的容量瓶c.玻璃棒d.滴定管
(2)仪器1恒压分液漏斗,其优点是__________________________ 。
(3)仪器3中NaOH固体的作用是__________________________ 。
(4)仪器6的一个作用是控制原料气按反应计量系数充分反应,若反应初期观察到装置内稀硫酸溶液中产生气泡,应该______ (填“加快”、“减慢”或“不改变”)产生氨气的流速。
(5)另有一种制备氨基甲酸铵的反应器(CCl4与液体石蜡均为惰性介质)如图。生成的氨基甲酸铵小晶体悬浮在四氯化碳中,当悬浮物较多时,停止制备。
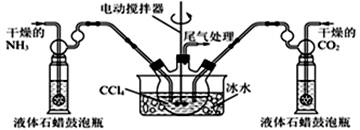
①发生器用冰水冷却的原因是________________________________________ ;
②从反应后混合物中过滤分离出产品。为了得到干燥产品,应采取的方法是_____ (填序号)
a.常压加热烘干b.高压加热烘干c.真空40℃以下烘干
(6)已知氨基甲酸铵可完全水解,其中产物有碳酸氢铵。氨基甲酸铵水解反应的化学方程式为________________________________ 。

(1)实验室用98%的浓硫酸配制15%的稀硫酸,除量筒外还需使用下列仪器中的
a.烧杯b.一定容积的容量瓶c.玻璃棒d.滴定管
(2)仪器1恒压分液漏斗,其优点是
(3)仪器3中NaOH固体的作用是
(4)仪器6的一个作用是控制原料气按反应计量系数充分反应,若反应初期观察到装置内稀硫酸溶液中产生气泡,应该
(5)另有一种制备氨基甲酸铵的反应器(CCl4与液体石蜡均为惰性介质)如图。生成的氨基甲酸铵小晶体悬浮在四氯化碳中,当悬浮物较多时,停止制备。

①发生器用冰水冷却的原因是
②从反应后混合物中过滤分离出产品。为了得到干燥产品,应采取的方法是
a.常压加热烘干b.高压加热烘干c.真空40℃以下烘干
(6)已知氨基甲酸铵可完全水解,其中产物有碳酸氢铵。氨基甲酸铵水解反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】Ⅰ.探究外界条件对反应速率的影响。有关实验记录如下表:
(1)写出该反应的化学方程式_______
(2)反应中微粒在反应前后变化的示意图如下,其中●和○代表不同元素的原子。

下列有关 和
和 混合的反应属于_______(填标号)。
混合的反应属于_______(填标号)。
(3)表中
_______ 、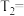
_______
(4)比较 、
、 、
、 、从大到小顺序
、从大到小顺序_______ 。
Ⅱ.探究反应存在一定的限度。
实验步骤:取 溶液,再滴加
溶液,再滴加 溶液;充分反应后,将溶液分成三份;
溶液;充分反应后,将溶液分成三份;
(5)取其中一份,加试剂苯,振荡,分层,上层显_______ 颜色,说明反应生成碘;另取一份,加试剂_______ (填化学式),现象_______ ,说明此反应存在一定的限度。写出该实验反应的离子方程式_______
(6)核内中子数为N的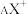 ,
, 它的氯化物中所含电子的物质的量为
它的氯化物中所含电子的物质的量为_______  。
。
| 实验编号 |  质量/g 质量/g |  形态 形态 |  |  | 溶液温度/ | 产生气泡时间/s | |
| 反应前 | 反应后 | ||||||
| 1 | 1.0 | 块状 | 2.0 |  | 20 | 32 |  |
| 2 | 1.0 | 粉状 | 2.0 | 10 |  | 35 |  |
| 3 | 1.0 | 粉状 | 4.0 | 10 | 20 | 35 |  |
| 4 | 1.0 | 粉状 | 2.0 | 10 | 35 | 50 |  |
(2)反应中微粒在反应前后变化的示意图如下,其中●和○代表不同元素的原子。

下列有关
 和
和 混合的反应属于_______(填标号)。
混合的反应属于_______(填标号)。| A.吸热反应 | B.复分解反应 | C.氧化还原反应 | D.可逆反应 |

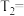
(4)比较
 、
、 、
、 、从大到小顺序
、从大到小顺序Ⅱ.探究反应存在一定的限度。
实验步骤:取
 溶液,再滴加
溶液,再滴加 溶液;充分反应后,将溶液分成三份;
溶液;充分反应后,将溶液分成三份;(5)取其中一份,加试剂苯,振荡,分层,上层显
(6)核内中子数为N的
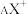 ,
, 它的氯化物中所含电子的物质的量为
它的氯化物中所含电子的物质的量为 。
。
您最近一年使用:0次




