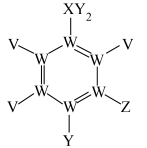
原子序数依次增大的5种短周期元素V、W、X、Y、Z形成的一种化合物的结构如图所示,该物质是生产药物诺氟沙星的中间体,也是制取农药的中间体。下列说法正确的是

A.化合物VWX的电子式为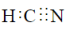 |
| B.基态Y原子核外电子具有5种不同的空间运动状态 |
C.沸点: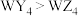 |
D.分子中的键角: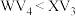 |
更新时间:2023-12-21 23:02:10
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】用NCl3和NaClO2溶液制备绿色消毒剂ClO2气体的离子方程式为NCl3+6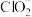 +3H2O=6ClO2↑+3Cl-+3OH-+NH3↑。已知NCl3易发生非氧化还原的水解反应:NCl3(l)+3H2O(l)=NH3(aq)+3HClO(aq)。下列有关说法错误的是
+3H2O=6ClO2↑+3Cl-+3OH-+NH3↑。已知NCl3易发生非氧化还原的水解反应:NCl3(l)+3H2O(l)=NH3(aq)+3HClO(aq)。下列有关说法错误的是
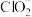 +3H2O=6ClO2↑+3Cl-+3OH-+NH3↑。已知NCl3易发生非氧化还原的水解反应:NCl3(l)+3H2O(l)=NH3(aq)+3HClO(aq)。下列有关说法错误的是
+3H2O=6ClO2↑+3Cl-+3OH-+NH3↑。已知NCl3易发生非氧化还原的水解反应:NCl3(l)+3H2O(l)=NH3(aq)+3HClO(aq)。下列有关说法错误的是A.NCl3的电子式为 | B.制备ClO2的离子反应中NCl3被还原为NH3 |
| C.氧化产物与还原产物的物质的量之比为2:1 | D.ClO2可用于自来水的杀菌消毒和面粉的漂白 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列化学用语表达不正确的是( )
A.Na+的结构示意图: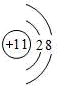 |
B.水的电子式: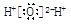 |
| C.二氧化碳的结构简式:O=C=O |
D.碳酸氢钠的电离方程式: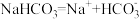 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知短周期主族元素X、Y、Z、W、R,其中X的原子半径在短周期主族元素中最大,Y元素的原子最外层电子数为m,次外层电子数为n,Z元素的原子L层电子数为m+n,M层电子数为m-n,W与Z同主族,R元素原子与Y元素原子的核外电子数之比为2:1。下列叙述错误的是
| A.X与Y形成的两种化合物中阴、阳离子的个数比均为1:2 |
| B.Y的氢化物比R的氢化物稳定,且熔沸点高 |
| C.RY2和WY2通入Ba(NO3)2溶液中均不产生白色沉淀 |
| D.RY2和X2Y2均具有漂白性,均能使品红试液褪色 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】短周期主族元素W、X、Y、Z的原子序数依次增大,W的族序数是周期数的3倍,W、X同周期,W的最外层电子数等于Y、Z的最外层电子数之和,Y的原子半径在短周期主族元素中最大。下列说法正确的是
| A.简单离子半径:Y>X>W |
| B.X、Y形成的化合物水溶液显碱性 |
| C.Y、Z的最高价氧化物对应的水化物不能发生反应 |
| D.W、Y形成的化合物一定只含离子键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是
A. 电子云呈球形,表示电子绕原子核做圆周运动 电子云呈球形,表示电子绕原子核做圆周运动 |
| B.电子云图中的小黑点密度大,说明该原子核外空间电子数目多 |
C.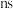 能级的电子云轮廓图可表示为 能级的电子云轮廓图可表示为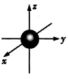 |
D.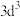 表示 表示 能级有3个轨道 能级有3个轨道 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】氮元素与氢元素可以形成多种分子或离子,如 、
、 、
、 、
、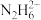 等。下列说法正确的是
等。下列说法正确的是
 、
、 、
、 、
、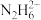 等。下列说法正确的是
等。下列说法正确的是| A.基态N原子中,有7个空间运动状态不同的电子 |
B. 、 、 同种分子间都可形成分子间氢键,但是主要因为 同种分子间都可形成分子间氢键,但是主要因为 的相对分子质量大于 的相对分子质量大于 ,则 ,则 的熔沸点高于 的熔沸点高于 |
C. 、 、 、 、 、 、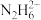 四种微粒中氮原子的杂化方式相同,四种微粒中只有 四种微粒中氮原子的杂化方式相同,四种微粒中只有 、 、 可以做配体 可以做配体 |
D.肼( )作火箭燃料时发生的反应是: )作火箭燃料时发生的反应是: ,若该反应中有4molN-H键断裂,则形成的π键有4mol ,若该反应中有4molN-H键断裂,则形成的π键有4mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】W、X、Y、Z为同一短周期的元素,且原子序数依次增加。其中X、Y、Z相邻,W的核外电子数与X的价层电子数相等,Z2是氧化性最强的单质,X的最简单气态氢化物与其最高价氧化物对应的水化物可以反应生成一种常见的盐。下列说法正确的是
| A.分子的极性:WZ3<XZ3 | B.第一电离能:X<Y<Z |
| C.元素的电负性:Y>Z | D.键能:X2<Y2<Z2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】抗癌药阿霉素与环糊精在水溶液中形成超分子包合物,结构如下图,增大了阿霉素的水溶性,控制了阿霉素的释放速度,从而提高药效。下列说法错误的是
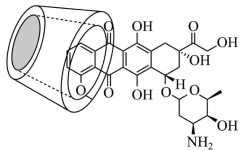
A.阿霉素分子中碳原子的杂化方式为 、 、 |
| B.可以通过晶体的X射线衍射实验获得阿霉素分子的键长和键角 |
C.该超分子包合物中既有 键,又有 键,又有 键 键 |
| D.阿霉素分子中不含手性碳原子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下表是一些键能数据(kJ/mol), 以下说法正确的是
共价键 | 键能 | 共价键 | 键能 | 共价键 | 键能 | 共价键 | 键能 |
H-Cl | 432 | H- H | 436 | H- F | 565 | H-S | 339 |
C- Cl | 330 | C- I | 218 | S- S | 255 |
| A.由表格可得出结论:半径越小的原子形成的共价键往往越牢固(即键能越大) |
| B.预测C-Br键的键能范围为218 kJ/mol<C- Br 键能<330 kJ/mol |
| C.由键能数据可得HF比HCl熔、沸点更高 |
| D.8H2(g) +S8(g)= 8H2S(g) △H= akJ/mol中,a= -104 (S8为八元环状分子) |
您最近一年使用:0次