物质的量是联系宏观和微观的桥梁:
(1)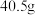 某金属氯化物
某金属氯化物 中含
中含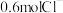 ,则该氯化物的摩尔质量为
,则该氯化物的摩尔质量为________ 。
(2)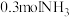 分子中所含原子数与
分子中所含原子数与________ 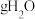 分子中所含原子数相等。
分子中所含原子数相等。
(3)由 两气体组成的混合气体
两气体组成的混合气体 ,标准状况下,体积为
,标准状况下,体积为 ,则
,则 的物质的量之比为
的物质的量之比为________ 。
(4)某溶液中只含有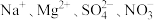 四种离子,已知前三种离子的个数比为2∶3∶1,则溶液中
四种离子,已知前三种离子的个数比为2∶3∶1,则溶液中 和
和 的离子个数比为
的离子个数比为________ 。
(5)碳酸铜和碱式碳酸铜【 】均能在高温下分解生成氧化铜。取一定量上述混合物充分煅烧后,剩余固体质量
】均能在高温下分解生成氧化铜。取一定量上述混合物充分煅烧后,剩余固体质量 。则溶解等质量的的上述混合物,需
。则溶解等质量的的上述混合物,需 硫酸
硫酸________  。
。
(1)
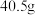 某金属氯化物
某金属氯化物 中含
中含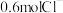 ,则该氯化物的摩尔质量为
,则该氯化物的摩尔质量为(2)
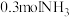 分子中所含原子数与
分子中所含原子数与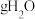 分子中所含原子数相等。
分子中所含原子数相等。(3)由
 两气体组成的混合气体
两气体组成的混合气体 ,标准状况下,体积为
,标准状况下,体积为 ,则
,则 的物质的量之比为
的物质的量之比为(4)某溶液中只含有
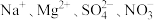 四种离子,已知前三种离子的个数比为2∶3∶1,则溶液中
四种离子,已知前三种离子的个数比为2∶3∶1,则溶液中 和
和 的离子个数比为
的离子个数比为(5)碳酸铜和碱式碳酸铜【
 】均能在高温下分解生成氧化铜。取一定量上述混合物充分煅烧后,剩余固体质量
】均能在高温下分解生成氧化铜。取一定量上述混合物充分煅烧后,剩余固体质量 。则溶解等质量的的上述混合物,需
。则溶解等质量的的上述混合物,需 硫酸
硫酸 。
。
更新时间:2023-12-12 22:12:15
|
相似题推荐
【推荐1】电解饱和食盐水可以生产一系列含氯、含钠的化工产品。
(1)配制饱和食盐水的食盐必须精制,精制过程中需要除去Ca2+、Mg2+、SO 等杂质离子,往往先后加入NaOH、BaCl2、Na2CO3溶液作为除杂试剂,向其中加入Na2CO3后产生的沉淀是
等杂质离子,往往先后加入NaOH、BaCl2、Na2CO3溶液作为除杂试剂,向其中加入Na2CO3后产生的沉淀是____ ,沉淀过滤后往往还要往滤液中加入____ ,随后再将溶液蒸发结晶。
(2)电解饱和食盐水实验时,电解的总反应方程式为_____ 。阳极产物检验所用的试剂是____ ;向两极各加入石蕊溶液,阴极溶液呈现____ 色。
(3)实验测得产生的氢气体积(已折算成标准状况)为5.60mL,电解后溶液的体积恰好为50.0mL,则溶液中NaOH的浓度为____ 。
(1)配制饱和食盐水的食盐必须精制,精制过程中需要除去Ca2+、Mg2+、SO
 等杂质离子,往往先后加入NaOH、BaCl2、Na2CO3溶液作为除杂试剂,向其中加入Na2CO3后产生的沉淀是
等杂质离子,往往先后加入NaOH、BaCl2、Na2CO3溶液作为除杂试剂,向其中加入Na2CO3后产生的沉淀是(2)电解饱和食盐水实验时,电解的总反应方程式为
(3)实验测得产生的氢气体积(已折算成标准状况)为5.60mL,电解后溶液的体积恰好为50.0mL,则溶液中NaOH的浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)写出离子方程式:向Ba(OH)2溶液中滴加NaHSO4溶液至Ba2+刚好沉淀完全________ ;
(2)标况下,将224L氯化氢气体溶于V升水中,所得溶液密度为dg/mL,则此溶液中溶质的物质的量浓度为________ mol/L
(3)使物质的量浓度之比为1:2:3的氯化钠、氯化镁、氯化铝溶液中的Cl-恰好完全沉淀时,若所用相同物质的量浓度的硝酸银溶液的体积比为3:2:3,则上述三种溶液的体积之比是__________ ;
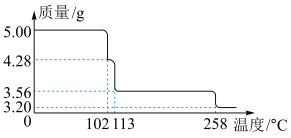
(4)5.00g CuSO4·5H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示,则200℃时所得固体物质的化学式为______________ ;
(5)已知氧化性:Cl2>Fe3+>I2,写出FeI2和Cl2按物质的量之比为7:8反应的总离子方程式_____
(2)标况下,将224L氯化氢气体溶于V升水中,所得溶液密度为dg/mL,则此溶液中溶质的物质的量浓度为
(3)使物质的量浓度之比为1:2:3的氯化钠、氯化镁、氯化铝溶液中的Cl-恰好完全沉淀时,若所用相同物质的量浓度的硝酸银溶液的体积比为3:2:3,则上述三种溶液的体积之比是
(4)5.00g CuSO4·5H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示,则200℃时所得固体物质的化学式为

(5)已知氧化性:Cl2>Fe3+>I2,写出FeI2和Cl2按物质的量之比为7:8反应的总离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ、分类是研究物质组成及其变化的一种常用的科学方法。
(1)现有:①固体 ②稀硫酸③氨气④熔融
②稀硫酸③氨气④熔融 ⑤蔗糖⑥铜;其中能导电的是
⑤蔗糖⑥铜;其中能导电的是_______ (填序号,下同);属于电解质的是_______ 。
(2) 受热分解的化学方程式是
受热分解的化学方程式是_______ ;
(3)除去NaHCO3溶液中混有的少量Na2CO3 ,所用试剂为_______ ,反应的离子方程式为_______ 。
Ⅱ、物质的量是高中化学常用的物理量,请完成以下有关计算:
(4)33.3g某金属氯化物MCl2中含有0.6molCl-,则该氯化物的摩尔质量为_______ 。
(5)在同温同压下,等质量的CO和CO2,其体积之比为_______ 。
(6)某混合盐溶液中含有离子: 、Mg2+、Cl-、
、Mg2+、Cl-、 ,测得
,测得 、Mg2+和Cl-的物质的量浓度依次为:
、Mg2+和Cl-的物质的量浓度依次为: 、
、 、
、 ,则c(
,则c( )=
)=_______  。
。
(1)现有:①固体
 ②稀硫酸③氨气④熔融
②稀硫酸③氨气④熔融 ⑤蔗糖⑥铜;其中能导电的是
⑤蔗糖⑥铜;其中能导电的是(2)
 受热分解的化学方程式是
受热分解的化学方程式是(3)除去NaHCO3溶液中混有的少量Na2CO3 ,所用试剂为
Ⅱ、物质的量是高中化学常用的物理量,请完成以下有关计算:
(4)33.3g某金属氯化物MCl2中含有0.6molCl-,则该氯化物的摩尔质量为
(5)在同温同压下,等质量的CO和CO2,其体积之比为
(6)某混合盐溶液中含有离子:
 、Mg2+、Cl-、
、Mg2+、Cl-、 ,测得
,测得 、Mg2+和Cl-的物质的量浓度依次为:
、Mg2+和Cl-的物质的量浓度依次为: 、
、 、
、 ,则c(
,则c( )=
)= 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求完成下列空白。
(1)2.9gNH4+的物质的量为___ ,其中含电子的数目为___ 。(用NA表示)
(2)同温同压下,同体积的氨气和甲烷气体的质量比为__ ,同质量的氨气和甲烷气体的体积比为__ 。
(3)已知24克A和40克B恰好完全反应生成0.4molC和32克D,则C的摩尔质量为__ 。
(4)某无土栽培营养液中含有NH4+、Cl-、K+、SO42-,测得含0.6mol/LNH4+、0.5mol/LCl-、0.5mol/LK+,则SO42-的物质的量浓度为__ 。
(1)2.9gNH4+的物质的量为
(2)同温同压下,同体积的氨气和甲烷气体的质量比为
(3)已知24克A和40克B恰好完全反应生成0.4molC和32克D,则C的摩尔质量为
(4)某无土栽培营养液中含有NH4+、Cl-、K+、SO42-,测得含0.6mol/LNH4+、0.5mol/LCl-、0.5mol/LK+,则SO42-的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】实验室有一瓶敞口放置一段时间的氢氧化钠固体,为测定该瓶样品中氢氧化钠的质量分数,现取17.3g该样品溶于足量的水中(固体完全溶解),向所得溶液中逐滴加入200g一定溶质质量分数的稀盐酸,实验过程如图所示(不考虑碳酸钠的分步反应)。
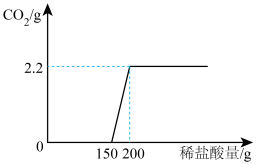
(1)经分析,该氢氧化钠固体_______ (填“部分”或“完全”)变质,恰好完全反应时,产生气体的质量为_______ g。
(2)计算样品中氢氧化钠的质量_______ (写出计算过程)。

(1)经分析,该氢氧化钠固体
(2)计算样品中氢氧化钠的质量
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)含有3.01×1023个H的H2O,其H2O物质的量是________ ;其H2O中含有电子的个数为______________ 。
(2)______ mol H2O中含有的氧原子数与1.5 mol CO2中含有的氧原子数相等。
(3)将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为________ 。
(4)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为__________ 。
(5)标准状况下,密度为0.75 g·L-1的NH3与CH4组成的混合气体中,NH3的体积分数为__________ ,(注:体积分数即为物质的量分数)
(6)已知a g A和b g B恰好完全反应生成0.4mol C和d g D,则C的摩尔质量为________
(7)同温、同压下等质量的SO2气体和CO2气体,体积之比___________ ,原子数目之比为___________ ,密度比为___________ ,氧元素的质量比为__________ 。
(8)某气态氧化物化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为____________ ;R的相对原子质量为_____________ 。
(9)200mL、2.0mol/L的Al2(SO4)3溶液中含Al3+的物质的量为___________ ;从中取出10mL,将这10mL溶液用水稀释到50mL,所得溶液中溶质的物质的量浓度为______________ 。
(2)
(3)将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为
(4)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为
(5)标准状况下,密度为0.75 g·L-1的NH3与CH4组成的混合气体中,NH3的体积分数为
(6)已知a g A和b g B恰好完全反应生成0.4mol C和d g D,则C的摩尔质量为
(7)同温、同压下等质量的SO2气体和CO2气体,体积之比
(8)某气态氧化物化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
(9)200mL、2.0mol/L的Al2(SO4)3溶液中含Al3+的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】水是生命之源,水在工业、农业和日常生活中均发挥着重要作用。
(1)下列关于水的说法,正确的是_________。
(2)为增强水的导电性,通常向纯水中加入适量的NaOH(NaOH不参加反应)。
①某电解水实验开始时,向180g纯水中溶解了4gNaOH。此时溶液中Na+和水分子的个数比是___________ 。
②当实验进行到一段时间,两个石墨电极共收集到的气体质量为3.6g。计算此时被电解的水的物质的量是____________ 。
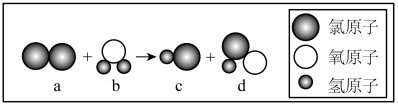
(3)目前,很多自来水厂用氯气杀菌、消毒。仔细观察下图的微观反应过程,写出该化学反应方程式___________ 。
(1)下列关于水的说法,正确的是_________。
| A.2mol水的摩尔质量是36g/mol | B.18g水中含有10个电子 |
| C.1mol水中含2mol氢 | D.一个水分子的质量约是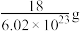 |
①某电解水实验开始时,向180g纯水中溶解了4gNaOH。此时溶液中Na+和水分子的个数比是
②当实验进行到一段时间,两个石墨电极共收集到的气体质量为3.6g。计算此时被电解的水的物质的量是
(3)目前,很多自来水厂用氯气杀菌、消毒。仔细观察下图的微观反应过程,写出该化学反应方程式

您最近一年使用:0次

 是碳的两种重要氧化物.
是碳的两种重要氧化物. 与
与 的体积比为
的体积比为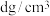 的硝酸钙溶液中含1g
的硝酸钙溶液中含1g ,则
,则

