设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是A.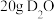 分子中含有的中子数为 分子中含有的中子数为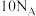 |
B.标准状况下,22.4L NO与 反应生成物的分子数为 反应生成物的分子数为 |
C.电解精炼铜时,阴极质量变化64g时,外电路中理论上转移的电子数为 |
D.在氨的催化氧化反应中,每消耗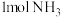 ,生成的水分子数为 ,生成的水分子数为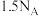 |
更新时间:2023-12-13 08:44:39
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.标准状况下,22.4 L戊烧中非极性键数目为 |
B.0.1 mol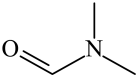 中含有的 中含有的 键数目为 键数目为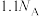 |
C.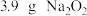 与足量的水反应,转移电子的数目为 与足量的水反应,转移电子的数目为 |
D.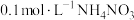 溶液中含有 溶液中含有 数小于 数小于 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】用NA表示阿伏加 德罗常数的值,下列说法中正确的数目是
①12.0g熔融的NaHSO4中含有的阳离子数为0.2NA
②1mol Na2O 和Na2O2混合物中含有的阴、阳离子总数是3NA
③常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA
④7.8g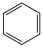 中含有的碳碳双键数目为0.3NA
中含有的碳碳双键数目为0.3NA
⑤用1L1.0 mol/LFeCl3溶液制备氢氧化铁胶体,所得氢氧化铁胶粒的数目为NA
⑥1mol SO2与足量O2在一定条件下充分反应生成SO3,共转移2NA个电子
⑦在反应KIO3+6HI=KI+3I2 +3H2O 中,每生成3molI2转移的电子数为5NA
⑧常温常压下,17 g甲基(-14CH3)中所含的中子数为9NA
①12.0g熔融的NaHSO4中含有的阳离子数为0.2NA
②1mol Na2O 和Na2O2混合物中含有的阴、阳离子总数是3NA
③常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA
④7.8g
 中含有的碳碳双键数目为0.3NA
中含有的碳碳双键数目为0.3NA⑤用1L1.0 mol/LFeCl3溶液制备氢氧化铁胶体,所得氢氧化铁胶粒的数目为NA
⑥1mol SO2与足量O2在一定条件下充分反应生成SO3,共转移2NA个电子
⑦在反应KIO3+6HI=KI+3I2 +3H2O 中,每生成3molI2转移的电子数为5NA
⑧常温常压下,17 g甲基(-14CH3)中所含的中子数为9NA
| A.3 | B.4 | C.5 | D.6 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】以下工业上或实验室中“反应/催化剂”的关系不符合事实的是( )
| A.合成氨/五氧化二钒 | B.乙醇氧化/铜 |
| C.氨催化氧化/三氧化二铬 | D.乙醇脱水/浓硫酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列各组物质中,不能满足如图一步转化关系的选项是


| 选项 | X | Y | Z |
| A | Mg | MgO | MgCl2 |
| B | H2SO4 | SO2 | SO3 |
| C | SiO2 | H2SiO3 | Na2SiO3 |
| D | N2 | NH3 | NO |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】化合物A 是一种重要的医药中间体,由原子序数依次增大的W、X、Y、Z 四种短周期元素组成,其结构如图所示,下列有关说法不正确的是
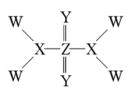

| A.X、Y形成的原子个数之比为1:2的二元化合物有2种 |
| B.X、Y、Z分别形成的简单氢化物中,Y的氢化物沸点最高 |
| C.简单离子半径大小:Z>X>Y |
| D.Z的低价态氧化物能使紫色石蕊试液先变红后褪色 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】如图所示,把NO2和N2O4的混合气体盛在两个连通的烧瓶里,调节左、右两边注射器内活塞,使其高度相等,关闭弹簧夹;同时把一个烧瓶放在热水里,另一个放在冰水里。下列对实验现象的描述错误的是( )。


| A.左边注射器内的活塞高度比右边注射器内的活塞高度要高 |
| B.左边注射器内的活塞与右边注射器内的活塞移动的方向和高度都相同 |
| C.左边烧瓶内的颜色比右边烧瓶内的颜色深 |
| D.两烧瓶内的化学平衡都发生了移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列叙述中不正确的是
| A.电解法精炼铜时将粗铜板作阳极 |
| B.电解法精炼铜时,粗铜中所含Na、Fe、Zn等杂质,电解后以单质形式沉积槽底,形成阳极泥 |
| C.钢铁发生吸氧腐蚀时,正极反应式为O2+2H2O+4e-===4OH- |
| D.电镀铜的过程中硫酸铜溶液中铜离子浓度不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】用NA代表阿伏加德罗常数。下列说法正确的是( )
| A.1molNH3中含有3NA对电子对 |
| B.工业用电解法进行粗铜精炼时,每转移lmol电子,阳极上溶解的铜原子数必为0.5NA |
| C.将2molSO2和lmolO2混合在V2O5存在条件下的密闭容器中,充分反应分子总数等于2NA |
| D.VLamol·L-1的氯化铁溶液中,若Fe3+的数目为NA,则Cl-的数目大于3NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列说法正确的一组是
①按照纯净物、混合物、强电解质、弱电解质和非电解质顺序排列的是CuSO4·5H2O、漂白粉、苛性钠、次氯酸、氮气
②电解质溶液导电的原因是电解质在外界电源的作用下电离出能自由移动的阴阳离子
③NH3键角比PH3的大,是因为NH3的成键电子对间排斥力较大
④由于离子键作用力很强,所以离子晶体的熔点都很高
⑤马口铁(镀锡)表面出现破损时,腐蚀速率会加快
⑥电解精炼铜,阳极为纯铜,阴极为粗铜
⑦Na与HCl反应是放热反应,而NaHCO3与HCl反应是吸热反应
⑧电解硫酸铜溶液一段时间后,向电解后的溶液中加入Cu(OH)2固体,溶液不可能快复到原来浓度
①按照纯净物、混合物、强电解质、弱电解质和非电解质顺序排列的是CuSO4·5H2O、漂白粉、苛性钠、次氯酸、氮气
②电解质溶液导电的原因是电解质在外界电源的作用下电离出能自由移动的阴阳离子
③NH3键角比PH3的大,是因为NH3的成键电子对间排斥力较大
④由于离子键作用力很强,所以离子晶体的熔点都很高
⑤马口铁(镀锡)表面出现破损时,腐蚀速率会加快
⑥电解精炼铜,阳极为纯铜,阴极为粗铜
⑦Na与HCl反应是放热反应,而NaHCO3与HCl反应是吸热反应
⑧电解硫酸铜溶液一段时间后,向电解后的溶液中加入Cu(OH)2固体,溶液不可能快复到原来浓度
| A.①③⑤⑧ | B.②④⑥⑦ | C.③④⑤⑧ | D.②③⑤⑧ |
您最近一年使用:0次

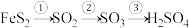 、
、
 。下列说法正确的是
。下列说法正确的是


